Clear Sky Science · pl
Analizy asocjacji w skali całego genomu w autoimmunizacyjnym niedoczynności tarczycy ujawniają wkład układu odpornościowego i specyficzny dla tarczycy oraz odwrotny związek z ryzykiem raka
Dlaczego to ma znaczenie dla zdrowia codziennego
Wiele osób odczuwa zmęczenie, zimno lub mgłę umysłową, nie zdając sobie sprawy, że przyczyną może być tarczyca. Autoimmunizacyjna niedoczynność tarczycy, w której własne mechanizmy obronne stopniowo atakują gruczoł tarczowy, dotyka ponad jedną na dwadzieścia osób. W tym badaniu wykorzystano dane genetyczne setek tysięcy ochotników, aby odpowiedzieć na dwa istotne pytania: jakie dziedziczne zmiany w naszym DNA zwiększają prawdopodobieństwo tej choroby i jak te same zmiany wiążą się z ryzykiem rozwoju nowotworów? Odpowiedzi ujawniają zaskakujący kompromis: układ odpornościowy, który czasem szkodzi tarczycy, może jednocześnie zapewniać dodatkową ochronę przed guzami.
Przegląd całego genomu
Naukowcy połączyli dane medyczne i informacje genetyczne z dwóch dużych projektów populacyjnych: FinnGen w Finlandii oraz UK Biobank w Wielkiej Brytanii. Skoncentrowali się na osobach wymagających długotrwałej substytucji hormonem tarczycy i starannie wykluczyli te przypadki, w których problemy z tarczycą wynikały z operacji, raka lub innych przyczyn niemających podłoża autoimmunologicznego. Uzyskano ponad 81 000 przypadków autoimmunizacyjnej niedoczynności tarczycy i więcej niż 700 000 osób kontrolnych, co czyni to największym jak dotąd badaniem tej choroby. Skanując miliony markerów DNA w całym genomie, badacze odkryli 418 niezależnych sygnałów genetycznych poza głównym klastrem genów odpornościowych, rozproszonych na co najmniej 280 rejonach genomu. Wiele z tych sygnałów dotyczyło rzadkich lub niskoczęstotliwościowych zmian DNA, które modyfikują strukturę białek, dając bezpośrednie wskazówki dotyczące leżącej u podstaw biologii.
Oddzielanie ogólnych efektów immunologicznych od specyficznych dla tarczycy
Autoimmunizacyjna niedoczynność tarczycy leży na styku ogólnej autoimmunologii i unikatowej biologii gruczołu tarczowego. Aby rozdzielić te składniki, zespół porównał swoje wyniki z badaniami genetycznymi innych chorób autoimmunologicznych oraz z poziomami tyreotropiny (TSH) we krwi, kluczowego markera klinicznego stosowanego do wykrywania niedoczynności tarczycy. Korzystając z metody klasyfikacji bayesowskiej, przyporządkowali sygnały genetyczne do grup: wspólnych dla szerokich chorób autoimmunologicznych oraz bardziej specyficznych dla regulacji hormonów tarczycy. Oszacowali, że około 38% sygnałów działa przez ogólne ścieżki immunologiczne wpływające na wiele chorób autoimmunologicznych, podczas gdy około 20% działa głównie poprzez funkcję tarczycy. Warianty ukierunkowane na tarczycę miały tendencję do wpływania na poziomy hormonów i geny aktywne w tkance tarczycy, podczas gdy warianty ogólnoustrojowe były bardziej aktywne w komórkach T, białych krwinkach orkiestrujących odpowiedzi immunologiczne.
Zbliżenie na kluczowy przełącznik immunologiczny
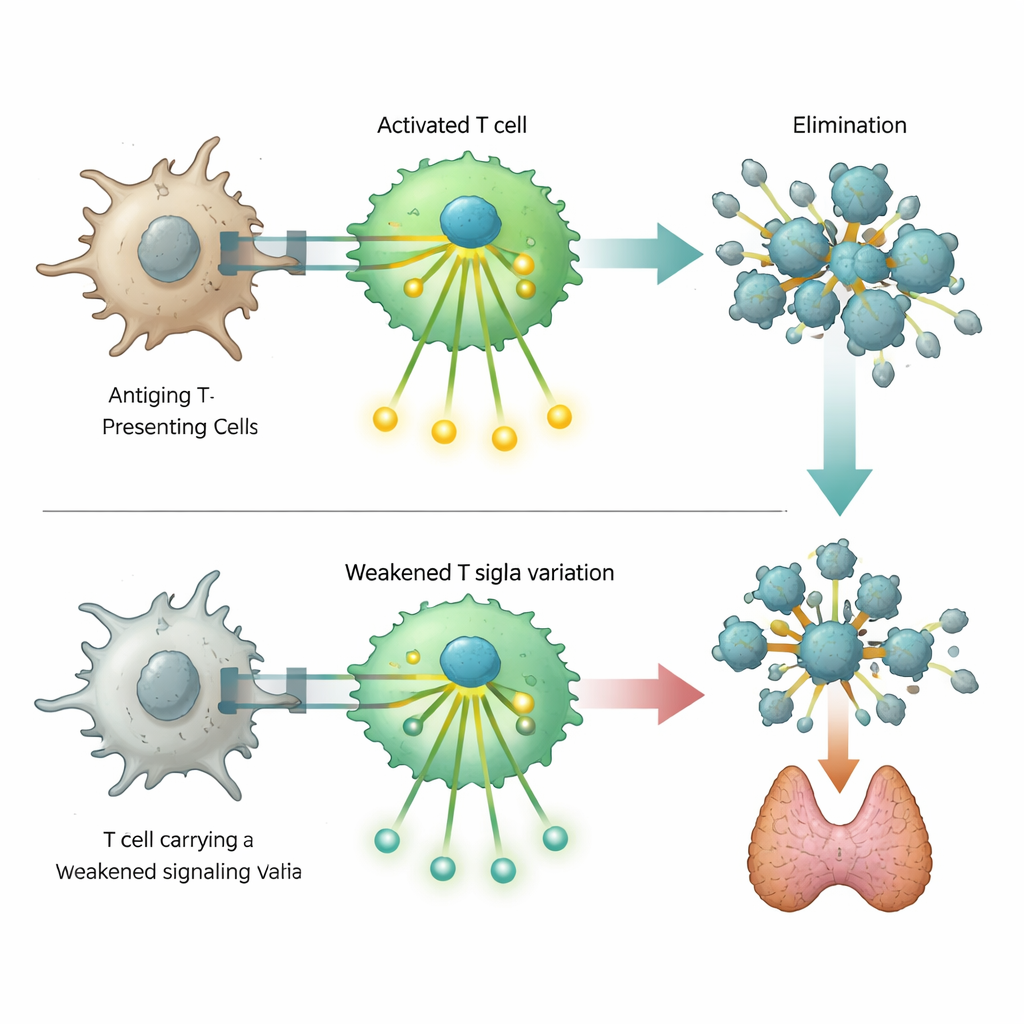
Jedno szczególnie uderzające odkrycie dotyczyło rzadkiej zmiany DNA w genie ZAP70, kodującym ważne białko sygnałowe wewnątrz komórek T. Ciężkie defekty tego białka są znane z wywoływania głębokich niedoborów odporności, lecz zidentyfikowany tutaj wariant powoduje jedynie częściową utratę funkcji. Eksperymenty laboratoryjne w zmodyfikowanych komórkach T wykazały, że zmienione ZAP70 osłabia, ale nie blokuje całkowicie, kaskady sygnałów, które zazwyczaj następują po rozpoznaniu celu. Komórki niosące ten wariant słabiej włączały markery aktywacji i dalsze kroki sygnalizacyjne. Ta stłumiona odpowiedź wydaje się zaburzać delikatną równowagę, która normalnie eliminuje autoreaktywne komórki T, predysponując nosicieli do chorób autoimmunologicznych przy jednoczesnym, umiarkowanym zwiększeniu ryzyka pewnych niedoborów odporności.
Niespodziewane powiązanie z ochroną przed rakiem
Ponieważ te same ścieżki immunologiczne, które napędzają autoimmunologię, mogą także atakować guzy, autorzy zbadali następnie, jak genetyka autoimmunizacyjnej niedoczynności tarczycy wiąże się z ryzykiem raka. Obliczyli poligeniczny wskaźnik ryzyka podsumowujący wrodzoną skłonność każdej osoby do niedoczynności tarczycy i sprawdzili jego powiązania z wieloma chorobami w fińskich danych. Jak można było się spodziewać, wyższy wskaźnik korelował z wyższym ryzykiem różnych chorób autoimmunologicznych. Bardziej zaskakujący był spójny wzorzec niższego ryzyka kilku nowotworów, zwłaszcza raka podstawnokomórkowego i innych nowotworów skóry, ale także raka piersi i prostaty oraz ogólna kategoria „wszystkie nowotwory”. Gdy zespół przeanalizował bezpośrednio wyniki badań genomowych dotyczących raka, około 10% miejsc powiązanych z niedoczynnością tarczycy wpływało także na raka skóry, przy czym ten sam wariant genetyczny zazwyczaj zwiększał autoimmunizację tarczycy, jednocześnie zmniejszając ryzyko raka skóry. Wspólne warianty koncentrowały się w genach związanych z odpornością, w tym w znanych celach leków stosowanych w immunoterapii z użyciem inhibitorów punktów kontrolnych.
Co to oznacza dla pacjentów i medycyny
Z perspektywy popularyzatorskiej wyniki te pokazują, że niektórzy ludzie rodzą się z układami odpornościowymi ustawionymi nieco „na wyższą temperaturę”, co czyni ich bardziej podatnymi na powolne, często ciche uszkodzenia tarczycy, a jednocześnie lepiej przygotowanymi do wykrywania i eliminowania rozwijających się nowotworów. Badanie rozdziela, które zmiany genetyczne działają przez ogólną nadaktywność odpornościową, a które wpływają specyficznie na produkcję hormonów tarczycy, wyjaśniając, dlaczego choroby takie jak zapalenie tarczycy Hashimoto i choroba Gravesa-Basedowa mogą dzielić niektóre geny ryzyka, a jednocześnie popychać funkcję tarczycy w przeciwnych kierunkach. Pomaga też zrozumieć, dlaczego pacjenci rozwijający problemy z tarczycą podczas stosowania leków wzmacniających odporność w terapii przeciwnowotworowej często lepiej reagują na te terapie. Ogólnie rzecz biorąc, wyniki sugerują, że powszechne, naturalne zróżnicowanie w genach punktów kontrolnych i szlakach sygnalizacyjnych odporności kształtuje zarówno autoimmunizacyjną chorobę tarczycy, jak i ryzyko raka w ciągu życia, dając nowe wskazówki do zapobiegania i bardziej spersonalizowanego stosowania immunoterapii.
Cytowanie: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Słowa kluczowe: autoimmunizacyjna niedoczynność tarczycy, choroba tarczycy, ryzyko genetyczne, układ odpornościowy, ochrona przed rakiem