Clear Sky Science · pl
GlycoRNA w kompleksie z heparan sulfatem reguluje sygnalizację VEGF‑A
Jak komórki precyzyjnie dostrajają sygnały dotyczące naczyń krwionośnych
Naczynia krwionośne nie pojawiają się po prostu tam, gdzie występują sygnały wzrostu — muszą być precyzyjnie kontrolowane, by odżywiać tkanki, nie sprzyjając jednocześnie rozwojowi nowotworów ani utracie wzroku. W tej pracy odkryto nieoczekiwany „hamulec” dla głównego sygnału sprzyjającego wzrostowi naczyń, nazwanego VEGF‑A. Autorzy wykazują, że małe fragmenty RNA, umieszczone na zewnątrz komórek we współpracy z cukrami i białkami, mogą tłumić przekaz VEGF‑A, zmieniając nasze rozumienie języka, jakim komórki komunikują się na swojej powierzchni.
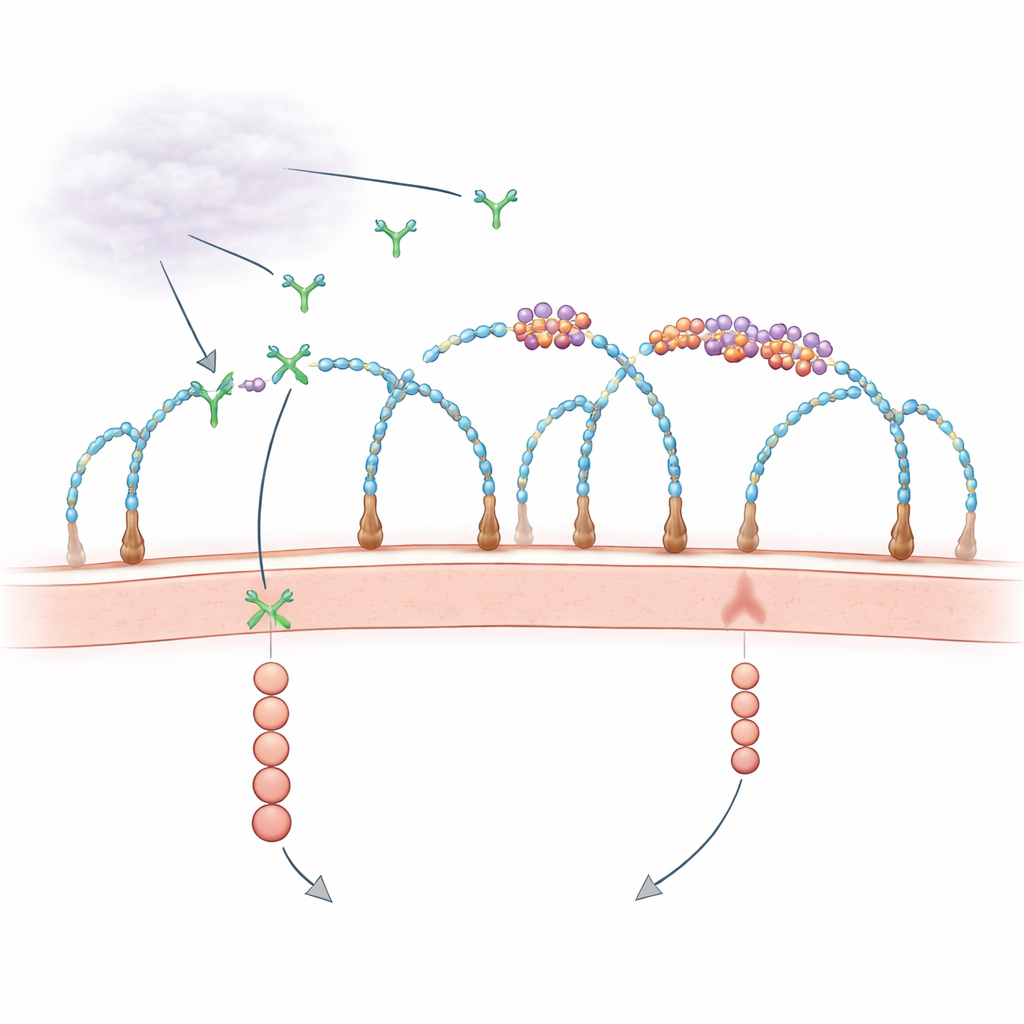
Zaskakująca rola RNA na powierzchni komórki
Przez dekady biolodzy wiedzieli, że zewnętrzna powłoka komórki, bogata w ozdobione cukrami białka zwane proteoglikanami heparan siarczanu, pomaga wychwytywać czynniki wzrostu i przedstawiać je ich receptorom. Równocześnie sporadyczne obserwacje sugerowały, że fragmenty RNA na zewnątrz komórek mogą wpływać na tworzenie naczyń krwionośnych, ale uczestnicy i mechanizmy pozostawały niejasne. Ostatnie badania ujawniły, że niektóre małe RNA są chemicznie połączone ze złożonymi cukrami, tworząc „glycoRNA”, oraz że niektóre białka wiążące RNA również pojawiają się na powierzchni komórki, skupiając się razem z tymi RNA. Nowe badanie stawia konkretne pytanie: czy te maleńkie wyspy RNA–białko w błonie rzeczywiście kontrolują sposób, w jaki odbierane są sygnały wzrostu, takie jak VEGF‑A?
Budowanie skupisk RNA–białko na łańcuchach cukrowych
Wykorzystując szeroko zakrojone ekrany CRISPR i mikroskopię wysokiej rozdzielczości, badacze odkryli, że określone łańcuchy cukrowe — heparan siarczan z konkretnymi grupami siarczanowymi — są niezbędnymi rusztowaniami do składania tych klastrów RNA–białko, które nazwali rybonukleoproteinami na powierzchni komórki (csRNP). Gdy usunięto kluczowe enzymy syntetyzujące lub sulfatyzujące heparan siarczan, klastry glycoRNA i ich towarzyszące białka zniknęły z powierzchni komórki, mimo że RNA i białka wciąż występowały wewnątrz komórek. Enzymy odcinające łańcuchy heparan siarczanu od powierzchni lub chemiczne blokowanie sulfatacji dawały ten sam efekt. Wyniki te pokazują, że nienaruszone, prawidłowo sulfowane łańcuchy heparan siarczanu organizują csRNP w nanoskalowe wyspy w błonie.
Skupiska RNA działają jako hamulec dla silnego sygnału wzrostu naczyń
Zespół zwrócił się następnie do ludzkich komórek śródbłonka, które wyściełają naczynia krwionośne i reagują na VEGF‑A. Stwierdzili, że te komórki również prezentują kotwiczone heparan siarczanem klastry csRNP. Leczenie żywych komórek RNazami, enzymami degradującymi RNA, usunęło składnik RNA bez naruszenia podstawowych łańcuchów cukrowych. W takich warunkach najczęstsza forma VEGF‑A wiążąca heparan (VEGF‑A165) wywołała znacznie silniejszą aktywację szlaku sygnałowego ERK, podczas gdy krótsza forma pozbawiona ogona wiążącego heparan (VEGF‑A121) pozostała bez zmian. Po usunięciu RNA na powierzchni związano więcej cząsteczek VEGF‑A165, choć poziomy receptorów pozostały takie same. W trójwymiarowych układach mikrofluidycznych komórki śródbłonka traktowane RNazą rosły głębiej w żelach kolagenowych i tworzyły rurkowate struktury bardziej intensywnie, co wskazuje, że zniszczenie powierzchniowego RNA uwalnia pro‑angiogenne zachowanie.
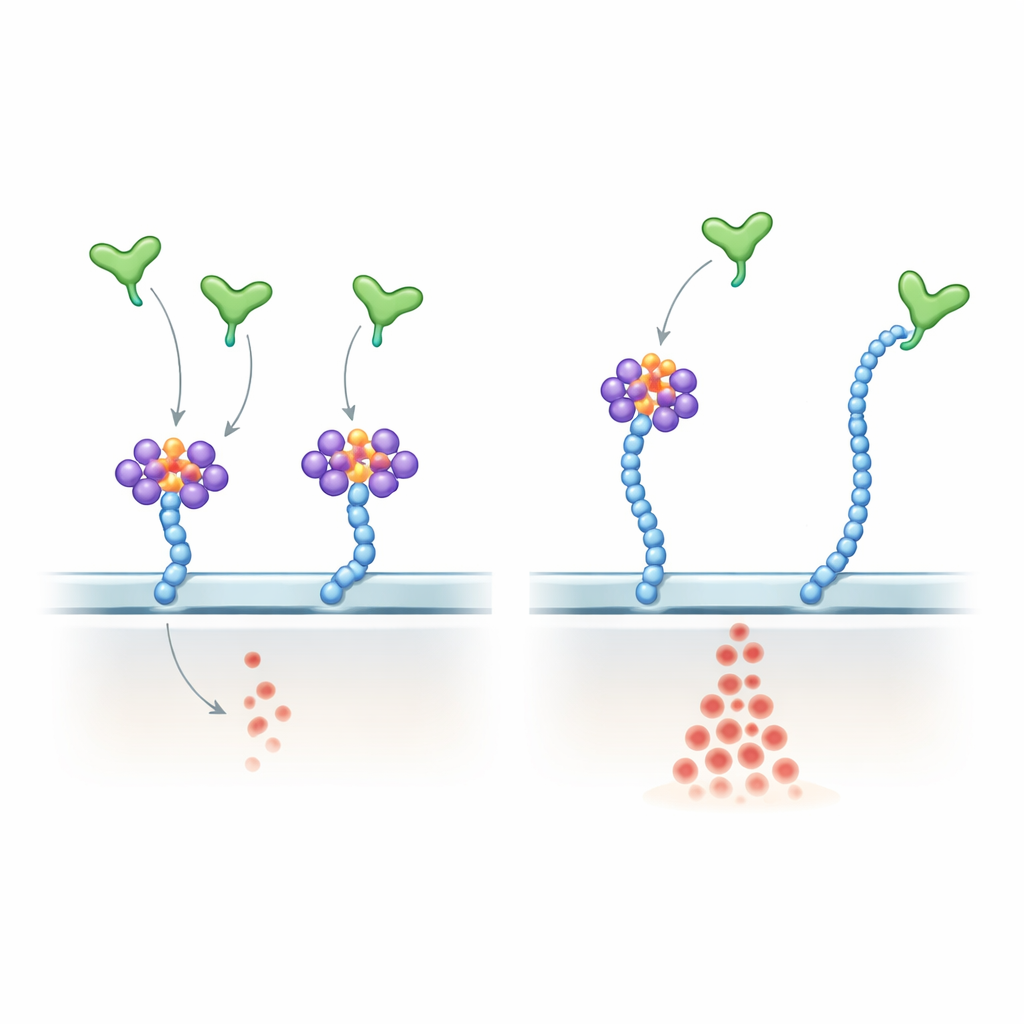
Rozkład mechanizmu: jak VEGF‑A rozróżnia RNA i cukry
Aby zbadać mechanizm, autorzy pokazali, że VEGF‑A165 wiąże bezpośrednio wybrane małe RNA, w tym wiele znanych glycoRNA, poprzez swoją dodatnio naładowaną część C‑terminalną — tę samą, która wiąże heparan siarczan. Skonstruowali subtelną wersję VEGF‑A165, w której kluczowe reszty argininy w tym ogonie zamieniono na lizyny. Ten mutant zachował ogólny dodatni ładunek i nadal wiązał łańcuchy heparan siarczanu, ale słabo wiązał glycoRNA i stał się w dużej mierze niewrażliwy na działanie RNazy. W komórkach śródbłonka mutant wywoływał silniejszą i bardziej odporną na RNazę aktywację ERK niż normalny VEGF‑A165, co wiernie naśladowało efekt usunięcia RNA z powierzchni komórki. U żywych myszy wstrzyknięcie mutanta do oka spowodowało bardziej bujny wzrost naczyń siatkówki niż normalne białko. U zarodków danio pręgowanego nadekspresja zmutowanej wersji Vegfa zaburzała normalne wzorce naczyń i zwiększała liczbę komórek śródbłonka.
Od mechanizmu podstawowego do szerszych implikacji
Na koniec autorzy pokazali, że przyłączenie ogona wiążącego heparan z VEGF‑A do niepowiązanego białka sygnałowego, Wnt3a, może przekierować aktywność Wnt: dołączenie normalnego ogona zmniejszało Wnt‑zależne zmiany rozwojowe, podczas gdy dołączenie ogona niewrażliwego na RNA je wzmacniało. Razem te eksperymenty wspierają model, w którym klastry csRNP, zakotwiczone przez specyficznie sulfowany heparan siarczan, wiążą VEGF‑A i pokrewne czynniki, aby złagodzić ich aktywność. Gdy składnik RNA zostaje usunięty lub gdy czynniki wzrostu tracą zdolność wykrywania RNA, równowaga przesuwa się w stronę silniejszej sygnalizacji i zmienionego rozwoju naczyń u wielu gatunków.
Dlaczego to ma znaczenie dla zdrowia i przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy komunikat jest taki, że komórki wykorzystują nie tylko białka i cukry, ale także małe RNA wystawione na swojej powierzchni, aby precyzyjnie dostrajać potężne sygnały wzrostu, takie jak VEGF‑A. Te RNA–białkowe klastry zakotwiczone w cukrach działają jak regulowane hamulce formowania naczyń, pomagając zapewnić, że nowe naczynia wyrastają tam i wtedy, gdzie są potrzebne. Zakłócenie tej równowagi — przez degradację powierzchniowego RNA lub zmianę właściwości wiążących RNA czynników wzrostu — może albo wzmacniać, albo błędnie skierowywać wzrost naczyń. Zrozumienie tej nowo ujawnionej warstwy kontroli może otworzyć drogę do terapii, które precyzyjniej będą zwiększać lub hamować angiogenezę w raku, chorobach oczu, gojeniu ran i medycynie regeneracyjnej, poprzez celowanie w powierzchniowe RNA, ich cukrowe rusztowania lub regiony wykrywające RNA w czynnikach wzrostu.
Cytowanie: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Słowa kluczowe: angiogeneza, czynnik wzrostu śródbłonka naczyniowego, heparan siarczan, RNA na powierzchni komórek, glycoRNA