Clear Sky Science · pl
Zbieżność i rozbieżność rozwojowa w ludzkich modelach komórek macierzystych autyzmu
Dlaczego te badania mają znaczenie dla rodzin i społeczeństwa
Spektrum zaburzeń autystycznych jest znane ze swojej złożoności: setki różnych genów powiązano ze zwiększonym ryzykiem, a mimo to wiele osób z autyzmem ma podobne wyzwania w komunikacji, interakcjach społecznych i zachowaniu. W tym badaniu postawiono pozornie proste pytanie o dalekosiężnych implikacjach: czy bardzo różne zmiany genetyczne prowadzą ostatecznie do podobnych zaburzeń w rozwijającym się ludzkim mózgu? Wykorzystując maleńkie, laboratoryjnie hodowane modele kory mózgowej utworzone z komórek pacjentów, badacze śledzą, w jaki sposób wczesne usterki w aktywności genów mogą napływać do wspólnych szlaków, które zmieniają proces powstawania, dojrzewania i łączenia się komórek mózgowych.
Hodowla miniaturowej tkanki mózgowej człowieka w laboratorium
Aby odpowiedzieć na to pytanie, zespół pobrał komórki skóry lub krwi od 55 osób: niektóre miały dobrze scharakteryzowane rzadkie mutacje silnie powiązane z autyzmem, inne miały autyzm bez znanej dużej mutacji, a jeszcze inne były grupą kontrolną bez zaburzeń. Komórki te przeprogramowano do indukowanych pluripotencjalnych komórek macierzystych, które mogą przekształcić się niemal w każdy typ komórki. Naukowcy następnie skierowali je do tworzenia trójwymiarowych „organoidów korowych” – maleńkich kulek tkanki naśladujących wczesny rozwój kory mózgowej człowieka. W ciągu 100 dni organoidy przechodziły od głównie progenitorów o cechach komórek macierzystych do sieci bogatych w młode neurony. W czterech punktach czasowych (dni 25, 50, 75 i 100) zespół mierzył, które geny są włączane lub wyłączane w setkach organoidów, tworząc szczegółowy film molekularnych zmian podczas wczesnego rozwoju mózgu.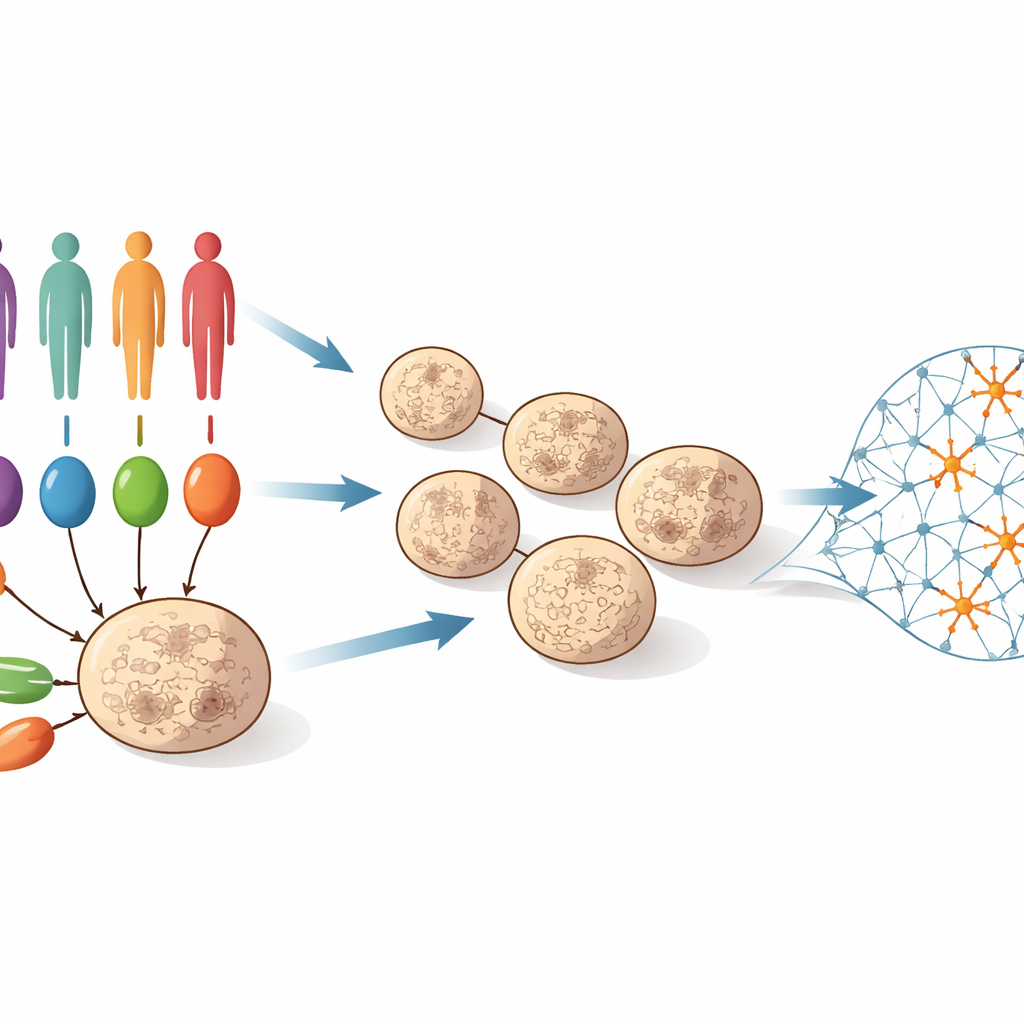
Wiele genetycznych ścieżek, wspólne wczesne odchylenia
Mimo że mutacje powiązane z autyzmem były bardzo różne – obejmowały duże brakujące lub zduplikowane fragmenty DNA oraz konkretne zmiany genów – organoidy niosące tę samą mutację wykazywały wysoce powtarzalne wzorce aktywności genów. We wczesnym stadium rozwoju, zwłaszcza około 25. dnia, każda mutacja dawała wyraźny sygnaturowy wzór: setki, a nawet ponad tysiąc genów były niewłaściwie regulowane w porównaniu z kontrolami. Nawet na tym wczesnym etapie kilka mutacji zmieniało nakładające się zestawy genów zaangażowanych w to, jak DNA jest pakowane i odczytywane w komórkach. Te wspólne zmiany dotyczyły znanych genów wysokiego ryzyka autyzmu i innych genów związanych z zaburzeniami rozwoju neurologicznego, co sugeruje, że różne mutacje bardzo wcześnie zaczynają zaburzać podobne mechanizmy komórkowe w formowaniu mózgu.
Zbieżność w miarę dojrzewania modelu mózgu
W miarę jak organoidy rozwijały się w kierunku bardziej dojrzałych neuronów (do dni 75 i 100) obraz uległ zmianie. Różnice specyficzne dla poszczególnych mutacji stały się mniej wyraźne, natomiast podobieństwa nasiliły się. We niemal wszystkich badanych genetycznych formach autyzmu zaobserwowano zmniejszoną aktywność genów istotnych dla sygnalizacji elektrycznej w synapsach – punktach komunikacji między neuronami – oraz zwiększoną aktywność genów związanych z wzrostem komórek i produkcją białek. Pojawiły się subtelne przesunięcia w proporcjach i stadiach dojrzewania różnych typów komórek, wskazujące na zmiany w czasie narodzin i dojrzewania neuronów, a nie na masowe ubytki konkretnych komórek. Na ostatnim punkcie czasowym tysiące genów wykazywały wspólny wzorzec zaburzeń regulacji w różnych rzadkich mutacjach, mimo że same mutacje dotyczyły różnych początkowych genów.
Centralny hub regulacyjny łączący wiele genów autystycznych
Dzięki głębszej analizie sieciowej zespół pogrupował geny, które miały tendencję do włączania i wyłączania się razem, w „moduły”. Jeden moduł, oznaczony M5, wyróżniał się szczególnie. Jego geny są najbardziej aktywne we wczesnym rozwoju i są silnie wzbogacone w geny ryzyka autyzmu, zwłaszcza te kontrolujące, jak inne geny są włączane lub wyłączane oraz jak pakowane jest DNA. W organoidach z kilku grup mutacji autystycznych moduł ten był konsekwentnie wyciszony. Badacze pokazali, że wiele białek wchodzących w skład M5 fizycznie ze sobą współdziała, tworząc hub regulacyjny. Używając narzędzi opartych na CRISPR do selektywnego wygaszenia 26 z tych regulatorów M5 w ludzkich progenitorach nerwowych, potwierdzili, że ten hub bezpośrednio kontroluje duże zestawy genów downstream, w tym wiele dodatkowych genów ryzyka autyzmu i zaburzeń rozwojowych, oraz że jego zaburzenie może zmieniać szlaki związane z powstawaniem neuronów i funkcją synaps.
Co to oznacza dla zrozumienia autyzmu
Praca ta sugeruje spójny obraz: rzadkie, silne mutacje powiązane z autyzmem zaczynają od zaburzania różnych fragmentów genomu, ale ich efekty rozchodzą się naprzód poprzez wspólną wczesną sieć kontrolną, która reguluje, jak powstają i są łączone neurony korowe. Z czasem te fale zbiegają się w wspólne wyniki – opóźnione lub zmienione dojrzewanie neuronów oraz zaburzone programy synaptyczne – mimo że początkowe przyczyny genetyczne są różne. Dla rodzin oznacza to, że bardzo różne diagnozy na poziomie DNA mogą wpływać na nakładające się ścieżki biologiczne w rozwijającym się mózgu. Dla naukowców i klinicystów zidentyfikowana sieć regulacyjna oferuje skoncentrowany zestaw molekularnych celów dla przyszłych terapii mających na celu przywrócenie bardziej typowych wzorców rozwoju mózgu w szerokim spektrum genetycznych stanów związanych z autyzmem.
Cytowanie: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Słowa kluczowe: zaburzenie ze spektrum autyzmu, organoidy mózgu, modele komórek macierzystych, regulacja genów, neuro‑rozwój