Clear Sky Science · pl
Komunikacja guz–mózg hamuje odporność przeciwnowotworową przez oś sensoryczno‑sympatyczną
Jak nerwy pomagają guzom się ukryć
Nowotwór zwykle opisuje się jako walkę między zbuntowanymi komórkami a układem odpornościowym, ale to badanie ujawnia zaskakującego trzeciego uczestnika: układ nerwowy. Naukowcy pokazują, że guzy płucne potrafią wykorzystać obwód nerwowy sensoryczno‑współczulny łączący płuca z mózgiem, a następnie używać tego obwodu do osłabiania naturalnej obrony organizmu przed rakiem. Zrozumienie tego ukrytego „przewodu” między guzami a mózgiem może otworzyć nowe drogi leczenia raka płuca przez celowanie w nerwy i ich sygnały, a nie tylko w same komórki nowotworowe. 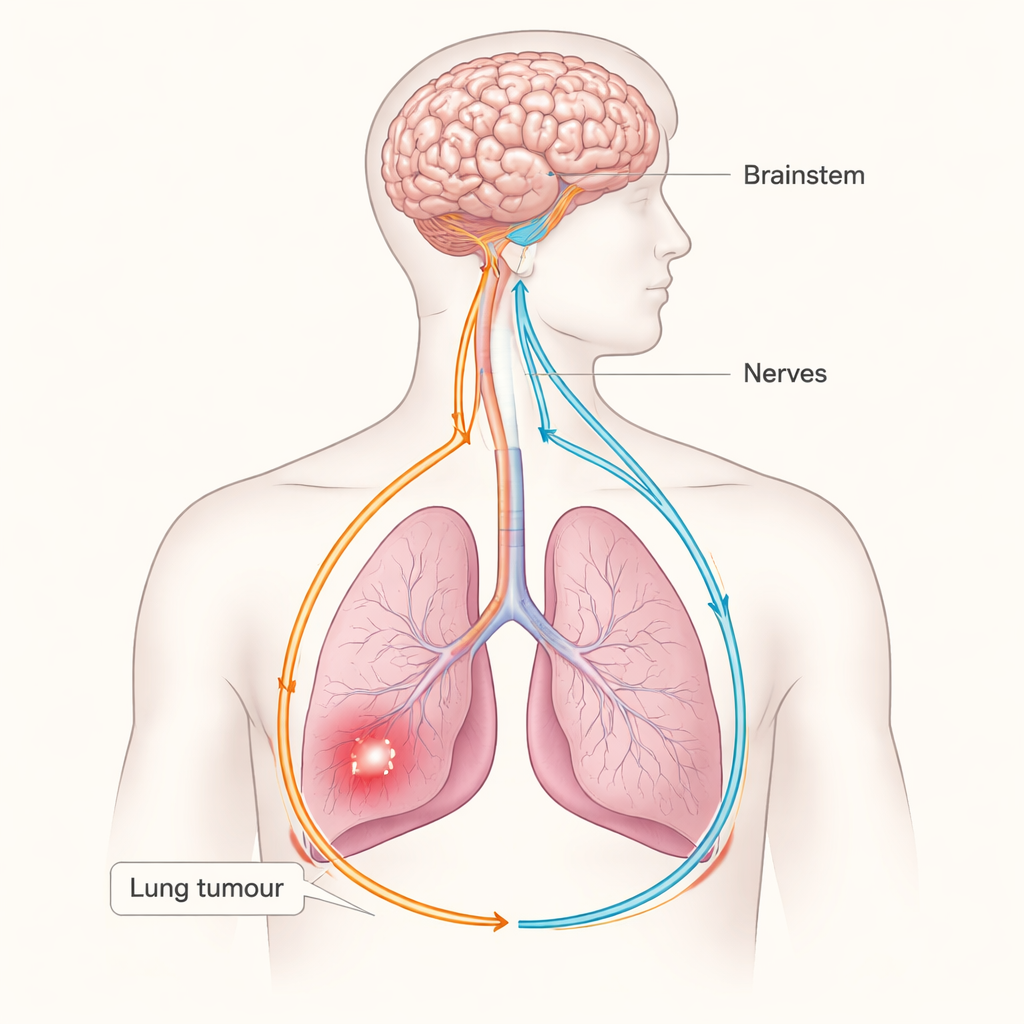
Nerwy wnikające do guza
Zespół badał gruczolakoraka płuca, częstą postać raka płuca, w zaawansowanych modelach mysich wiernie odzwierciedlających chorobę u ludzi. Dzięki trójwymiarowemu obrazowaniu całego narządu i genetycznemu znakowaniu odkryli, że guzy w płucach są intensywnie unerwione włóknami nerwowymi. Te włókna nie pojawiają się przypadkowo: wiele z nich pochodzi z określonej grupy komórek sensorycznych w nerwie błędnym, który normalnie przekazuje mózgowi informacje o stanie narządów. Zaobserwowano, że komórki guza wydzielają białka promujące wzrost, takie jak czynnik wzrostu nerwów, które pobudzają rozrost i inwazję tych włókien czuciowych błędnych do guza. Równocześnie same neurony sensoryczne zmieniały aktywność genową, co sugeruje, że guz przeprogramowuje je, aby reagowały inaczej niż w zdrowej tkance płucnej.
Jednokierunkowe wzmocnienie sygnałów sprzyjających guzowi
Nie wszystkie neurony sensoryczne związane z nerwem błędnym brały udział w tym procesie. Badacze wyodrębnili podtyp oznaczony dwoma cząsteczkami, NPY2R i TRPV1, jako głównych uczestników. Neurony te były liczne w obszarach guza, lecz w dużej mierze nieobecne w pobliskich zdrowych częściach płuca. Gdy naukowcy selektywnie usunęli lub wyciszyli grupę NPY2R/TRPV1 — używając sztuczek genetycznych, celowanych toksyn lub receptorów projektowanych, które można wyłączyć lekiem — guzy płuc znacząco się zmniejszyły, a myszy żyły dłużej, zachowując lepszą masę ciała i zachowanie. W przeciwieństwie do tego, usunięcie innej podgrupy sensorycznej unerwiającej inne struktury płuca nie spowolniło wzrostu guza, co podkreśla, że tylko konkretny „kanał” sensoryczny jest włączony w kontrolę nowotworu. 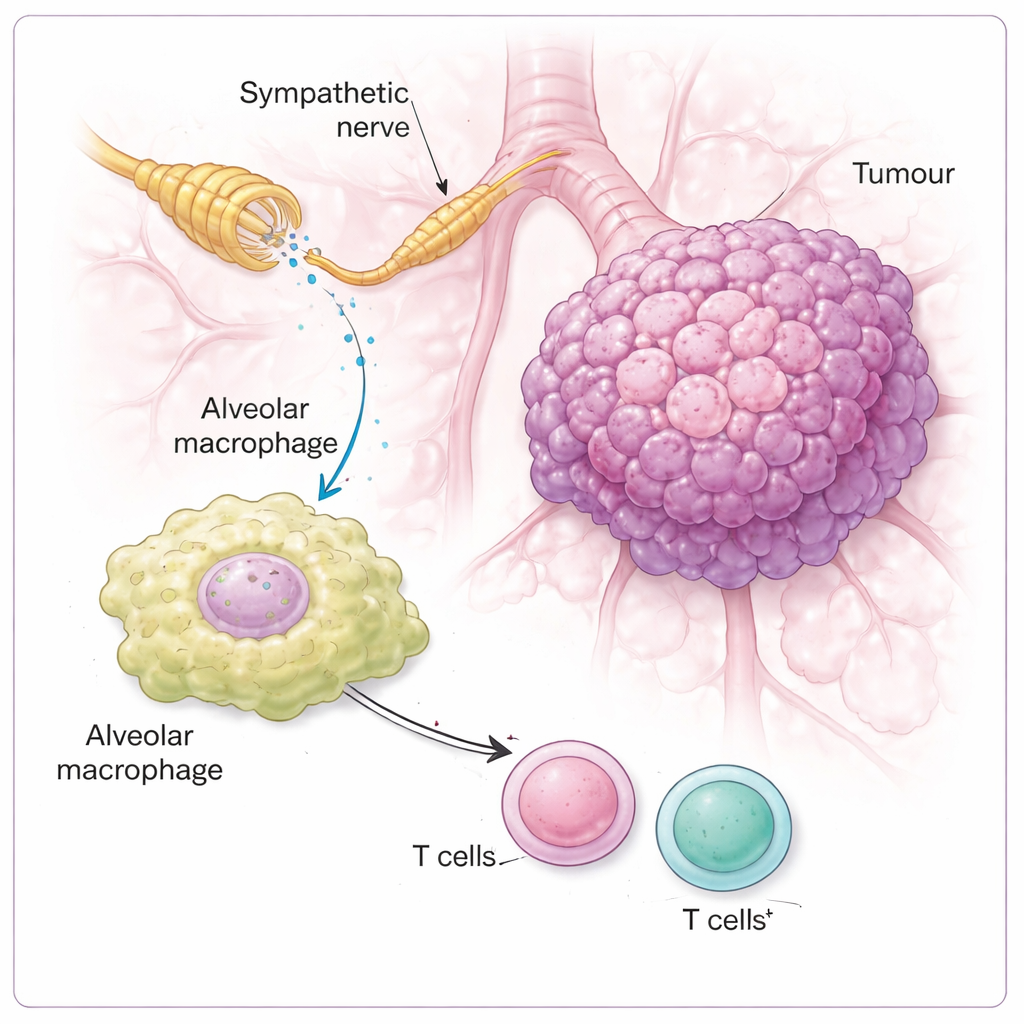
Od pnia mózgu do sygnałów przypominających stres w płucu
Aby zobaczyć, jak te sygnały sensoryczne są przetwarzane przez mózg, zespół prześledził obwód w kierunku ośrodkowym. Markery aktywności wykazały, że w obecności guzów płuc zapalały się rejony pnia mózgu otrzymujące włókna błędne, zwłaszcza obszar zwany przednio‑boczno‑przyśrodkową częścią rdzenia przedłużonego (rostral ventrolateral medulla), ważny węzeł zwiększający współczulny wypływ „walcz lub uciekaj”. Wyłączenie neuronów sensorycznych NPY2R/TRPV1 uciszyło tę aktywność pnia mózgu i zmniejszyło liczbę włókien współczulnych oraz poziomy przekaźnika stresu noradrenaliny w okolicy guza. Wyciszenie samego węzła pnia mózgu również spowalniało wzrost guza. Razem wyniki te opisują zamkniętą pętlę: guz pobudza nerwy sensoryczne błędne, pień mózgu odpowiada zwiększeniem współczulnego wypływu, a nerwy współczulne oddziałują na środowisko płuca w sposób sprzyjający nowotworowi.
Wyłączanie komórek odpornościowych przez miejscowych pośredników
Badanie następnie pytało, które komórki w otoczeniu guza rzeczywiście „słyszą” sygnały współczulne. Ku zaskoczeniu, noradrenalina miała niewielki bezpośredni wpływ na wzrost komórek nowotworowych in vitro. Kluczowymi responderami okazały się komórki odpornościowe, zwłaszcza makrofagi pęcherzykowe — strażnicze komórki zlokalizowane w pęcherzykach płucnych. Makrofagi te miały wysoki poziom receptora zwanego receptorem β2‑adrenergicznym, który wyczuwa noradrenalinę. Gdy ten receptor był nieobecny lub gdy sygnalizacja noradrenaliny została zablokowana, guzy rosły wolniej, a atak przez komórki T był silniejszy. U myszy z nienaruszonym obwodem nerwowym noradrenalina przesuwała makrofagi w kierunku stanu bardziej supresyjnego, oznaczanego wyższym poziomem enzymu ARG1, znanego z hamowania aktywności limfocytów T. Gdy makrofagi zostały przeprogramowane w ten sposób, pobliskie limfocyty CD4 i CD8 — na ogół podstawowe komórki zabójcze przeciwko rakowi — miały mniejszą zdolność do zainicjowania silnej odpowiedzi.
Dlaczego to ma znaczenie dla leczenia raka
Mówiąc wprost, autorzy pokazują, że guzy płucne potrafią „rozmawiać” z mózgiem przez nerw błędny i otrzymywać szkodliwą odpowiedź przez nerwy współczulne, które nakazują miejscowym makrofagom uciszyć limfocyty T. Przerwanie dowolnego istotnego ogniwa tej pętli — wejścia sensorycznego, przekaźnika w pniu mózgu, wypływu współczulnego lub sygnalizacji β2‑adrenergicznej w makrofagach — wystarczało, by przywrócić silniejszą odporność przeciwnowotworową i spowolnić rozwój raka u myszy. Dane od pacjentów z rakiem płuca dodatkowo sugerują, że pacjenci, których guzy wykazują wyższe sygnatury tych szlaków nerwowych, mają gorsze rokowanie i mniej komórek zabójczych T w guzach. Praca ta stawia hipotezę, że leki już stosowane w chorobach serca i lęku, takie jak beta‑blokery, lub przyszłe terapie ukierunkowane na konkretne obwody nerwowe, mogłyby zostać ponownie wykorzystane lub dopracowane, by „przetnąć przewody”, których guzy używają, by uciec przed atakiem odpornościowym.
Cytowanie: Wei, H.K., Yu, C.D., Hu, B. et al. Tumour–brain crosstalk restrains cancer immunity via a sensory–sympathetic axis. Nature 650, 1007–1016 (2026). https://doi.org/10.1038/s41586-025-10028-8
Słowa kluczowe: neuronauka nowotworowa, odporność przy raku płuca, nerw błędny, układ współczulny, mikrośrodowisko guza