Clear Sky Science · pl
Spersonalizowane szczepionki mRNA wywołują trwałą odporność komórkową po leczeniu uzupełniającym w TNBC
Nowa nadzieja po leczeniu raka piersi
Dla wielu kobiet z agresywną postacią raka piersi zwaną potrójnie ujemnym (TNBC) strach nie kończy się wraz z zakończeniem chemioterapii i zabiegu. Ten typ nowotworu ma wysokie ryzyko nawrotu i przerzutów, często już w ciągu kilku lat. Opisane tutaj badanie testuje wysoce spersonalizowaną szczepionkę, zbudowaną na podstawie mutacji guza konkretnej pacjentki, aby sprawdzić, czy potrafi wyszkolić układ odpornościowy do wieloletniego czuwania i zmniejszyć ryzyko nawrotu po zakończeniu standardowego leczenia.
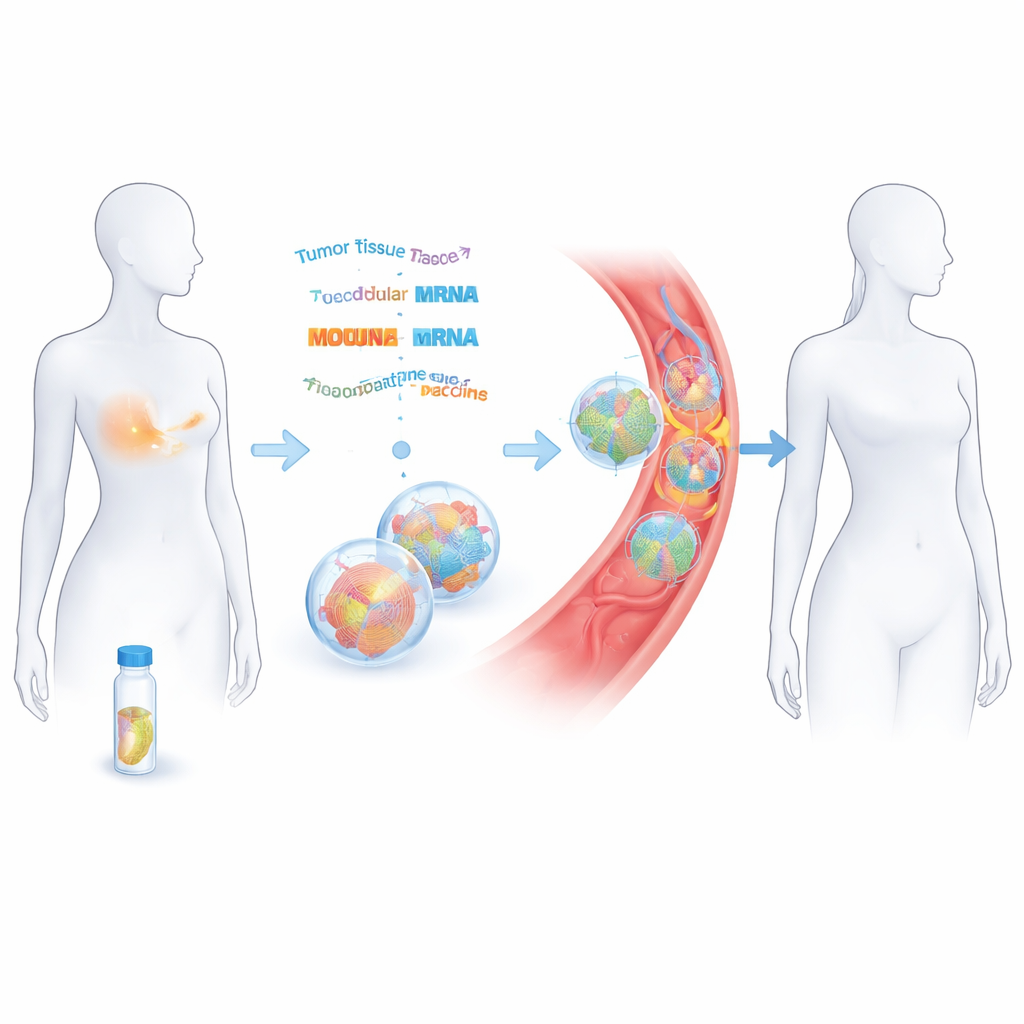
Przekształcanie usuniętego guza w szczepionkę na zamówienie
Naukowcy współpracowali z 14 kobietami z wczesnym stadium potrójnie ujemnego raka piersi, które przeszły już zabieg i chemioterapię z zamiarem wyleczenia. Z pobranego materiału guza odczytali DNA i RNA, aby skatalogować unikatowe mutacje nowotworu. Za pomocą narzędzi komputerowych przewidzieli, które z tych zmian mogą być rozpoznane przez komórki odpornościowe jako obce. Do 20 takich "neoantygenów" połączono następnie w długie sekwencje i zaszyfrowano w dwóch niciach mRNA — podobnie w zasadzie jak w szczepionkach przeciw COVID‑19, ale dopasowanych do każdej pacjentki. Te nici mRNA zapakowano w maleńkie pęcherzyki lipidowe i podawano dożylnie w ośmiu dawkach przez około dwa miesiące.
Jak szczepionka pobudza obrońców odpornościowych
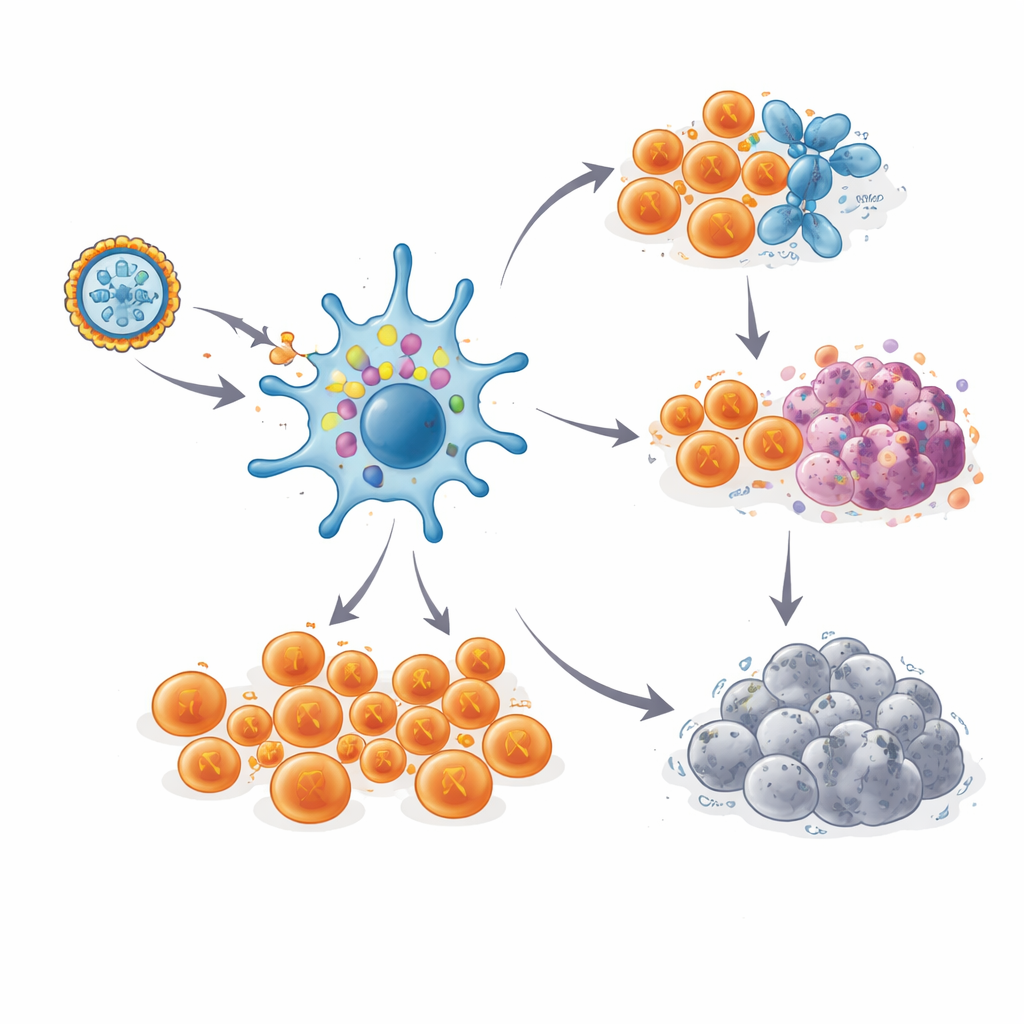
Po dostaniu się do organizmu mRNA instruuje komórki dendrytyczne — strażników układu odpornościowego — by przez krótki czas wytworzyły białka neoantygenów i zaprezentowały ich fragmenty na swojej powierzchni. Działa to jak list gończy dla komórek T, głównej siły zabijającej komórki nowotworowe. Zespół pobierał krew przed szczepieniem i w kilku punktach po nim, by sprawdzić, czy pojawiły się komórki T specyficzne dla neoantygenów i jak silne były te odpowiedzi. Dzięki czułym testom laboratoryjnym stwierdzono, że każda pacjentka rozwinęła nowe lub wzmocnione odpowiedzi komórkowe przeciw przynajmniej jednej wybranej mutacji, a większość reagowała na kilka. W wielu przypadkach duże ułamki krążących komórek T — poziomy zwykle obserwowane jedynie przy silnych terapiach komórkowymi — były teraz wyspecjalizowane do rozpoznawania celów specyficznych dla guza.
Trwała pamięć immunologiczna
Co istotne, te odpowiedzi komórek T nie wygasały szybko. U większości pacjentek silne odpowiedzi osiągały szczyt podczas okresu szczepień, nieznacznie opadały, a następnie utrzymywały się na wysokim poziomie przez jeden do trzech i pół roku, nawet bez dawek przypominających. Śledząc unikatowe „kody kreskowe” receptorów poszczególnych klonów komórek T, naukowcy mogli obserwować konkretne komórki reagujące na neoantygeny przez okres do sześciu lat u jednej pacjentki, która pozostała bez nawrotu choroby. Szczegółowe analizy pojedynczych komórek wykazały dwa główne losy tych komórek. Wiele z nich przekształciło się w silnie uzbrojone komórki T‑zabójcy, gotowe niszczyć każdą komórkę niosącą dany neoantygen. Inne rozwinęły się w rzadszą, przypominającą komórki macierzyste pulę pamięci, z markerami samoodnawiania, sugerującą rezerwuar zdolny do generowania nowych fal komórek atakujących, jeśli komórki nowotworowe nawrócą.
Co się stało z pacjentkami
Po medianie nieco ponad pięciu lat obserwacji od pierwszej dawki szczepionki jedenaście z czternastu kobiet nie doświadczyło nawrotu choroby; jedna z nich zmarła z przyczyn niezwiązanych z rakiem, będąc wciąż w remisji. U trzech kobiet wystąpił nawrót, a ich przypadki rzucają światło na to, dlaczego spersonalizowana szczepionka czasem zawodzi. Jedna pacjentka wytworzyła jedynie słabą odpowiedź komórek T i później odniosła korzyść z innego leku immunoterapeutycznego, przeciwciała anty‑PD‑1, zanim ostatecznie zmarła z powodu szeroko rozsianej choroby. Druga pacjentka miała dziedziczne ryzyko i guzy w obu piersiach; zaszczepiono tylko na podstawie jednego guza, a późniejsze dowody pokazały, że nawrót pochodził z genetycznie odrębnego, niezaszczepionego guza. Trzecia pacjentka miała silne komórki T wywołane przez szczepionkę, które napłynęły do nawrotowego guza, ale komórki nowotworowe w dużej mierze utraciły kluczowe molekuły potrzebne do prezentacji neoantygenów na swojej powierzchni, skutecznie chowając się przed atakiem immunologicznym.
Dlaczego ta praca ma znaczenie na przyszłość
To wczesnofazowe badanie było niewielkie i nie miało grupy kontrolnej, więc nie dowodzi, że sama szczepionka zapobiegła nawrotom. Niemniej jednak pokazuje, że zbudowanie złożonej, spersonalizowanej szczepionki mRNA na podstawie guza pacjentki jest wykonalne w rutynowych warunkach szpitalnych, jest zwykle dobrze tolerowane i może wywołać potężne, długo utrzymujące się armie komórek T przeciw wielu nowotworowo‑specyficznym celom. Wyniki wskazują też drogi ucieczki, z których nowotwory mogą korzystać — na przykład utratę mechanizmów prezentacji antygenów lub powstawanie z niecelowanych zmian — co sugeruje kombinacje z innymi terapiami immunologicznymi i bardziej rozległe sekwencjonowanie guzów. Dla pacjentek z potrójnie ujemnym rakiem piersi ta praca sugeruje, że szyta na miarę szczepionka, podana po standardowym leczeniu, mogłaby w przyszłości pomóc zapobiegać nawrotom, zamieniając ich własny układ odpornościowy w trwałą, wysoce specyficzną linię obrony.
Cytowanie: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Słowa kluczowe: rak piersi potrójnie ujemny, szczepionki przeciwnowotworowe mRNA, immunoterapia neoantygenowa, odporność komórek T, nawroty guza