Clear Sky Science · pl
Starzenie sprzyja gromadzeniu się w mikrogleju powoli degradowanych białek synaptycznych
Dlaczego oczyszczanie białek w mózgu ma znaczenie wraz z wiekiem
Większość z nas chce zachować jasny umysł na starość, a jednak wiek jest największym czynnikiem ryzyka choroby Alzheimera i innych demencji. W badaniu zadano pozornie proste pytanie: co dzieje się z codziennym „porządkiem” białek wewnątrz komórek mózgu wraz z upływem lat? Tworząc nowe molekularne narzędzia u myszy do śledzenia świeżo wytworzonych białek neuronalnych w czasie, badacze śledzą, jak białka są odnawiane, jak zlepiają się w agregaty i jak komórki odpornościowe mózgu, mikroglej, pomagają usuwać te pozostałości. Ich odkrycia ujawniają szerokie spowolnienie mechanizmów oczyszczania białek skupione na synapsach — miejscach łączących neurony — co może częściowo wyjaśniać utratę pamięci związaną z wiekiem.
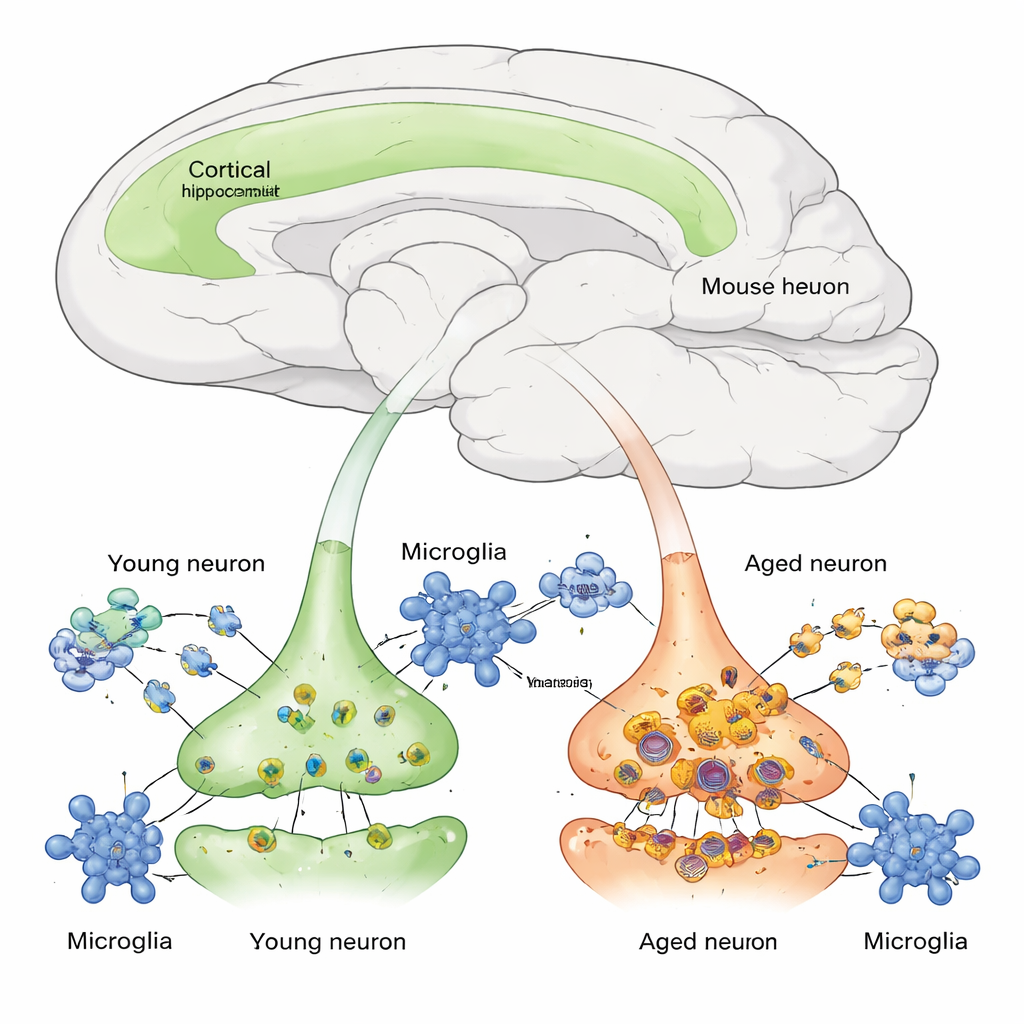
Śledzenie nowych białek w żywych komórkach mózgu
Białka w naszych komórkach są nieustannie syntetyzowane i rozkładane — równowaga ta znana jest jako proteostaza. Do tej pory trudno było zmierzyć ten proces w konkretnych typach komórek w żywym mózgu ssaka. Autorzy opracowali myszy z genetycznym systemem „znakowania” zwanym BONCAT, który powoduje, że tylko określone neurony — te korzystające z promotora Camk2a, głównie pobudzające neurony kory i hipokampa — włączają specjalny, „klikalny” aminokwas do nowo syntetyzowanych białek. Po podaniu myszy tego aminokwasu przez krótki okres zespół mógł wyizolować i zidentyfikować za pomocą spektrometrii mas jedynie świeżo wytworzone białka neuronalne, a następnie obserwować, jak ich poziomy malały w czasie w miarę degradacji.
Jak starzenie spowalnia obrót białek
Używając wirusowej wersji narzędzia znakującego, badacze oznaczyli neurony u młodych (4 miesiące), w średnim wieku (12 miesięcy) i starych (24 miesiące) myszy. Następnie śledzili tysiące białek w kilku obszarach mózgu — korze sensorycznej i wzrokowej, hipokampie i podwzgórzu — podczas dwutygodniowego okresu „śledzenia” po zaprzestaniu znakowania. Modelując te krzywe zaniku, oszacowali okres półtrwania każdego białka, czyli czas, w którym połowa z niego zostaje usunięta. Średnio okres półtrwania białek neuronalnych zwiększył się około dwukrotnie między młodymi a starymi myszy, przy czym większość spowolnienia pojawiła się po średnim wieku. Efekt różnił się w zależności od regionu, a niektóre zbiory białek ulegały degradacji w silnie skoordynowany sposób, co wskazuje, że całe szlaki — na przykład te kontrolujące sygnalizację synaptyczną — mają podobne, zależne od wieku kinetyki.
Zlepiające się białka i wrażliwe synapsy
Wolniejsze tempo rozkładu zwiększa ryzyko, że białka źle się złożą i będą się sklejać. Zespół wyizolował detergento‑niezmywalne agregaty ze starych mózgów myszy i, wykorzystując znakowanie neuronalne, zdefiniował „agregom” składający się z 1726 białek neuronalnych, które trafiają do tych grudek. Prawie połowa białek wykazujących wiekowo obniżoną degradację pojawiła się także w agregatach, a wiele z nich było powiązanych w poprzednich badaniach genetycznych z zaburzeniami neurorozwojowymi lub neurodegeneracyjnymi. Na wyróżnienie zasługiwały białka synaptyczne: elementy maszynerii przed‑ i postsynaptycznej, połączeń komórkowych oraz składniki mitochondrialne w synapsach były silnie wzbogacone zarówno wśród białek wolno degradowanych, jak i agregujących. Mikroskopia potwierdziła, że specyficzne białka, takie jak RTN3 i SRSF3, tworzyły przypominające agregaty punkty w starzejącym się hipokampie myszy, a nie w mózgach młodych. Ten skoncentrowany na synapsach defekt proteostazy wpisuje się w długotrwałe dowody, że utrata synaps jest ciasno związana z pogorszeniem funkcji poznawczych.
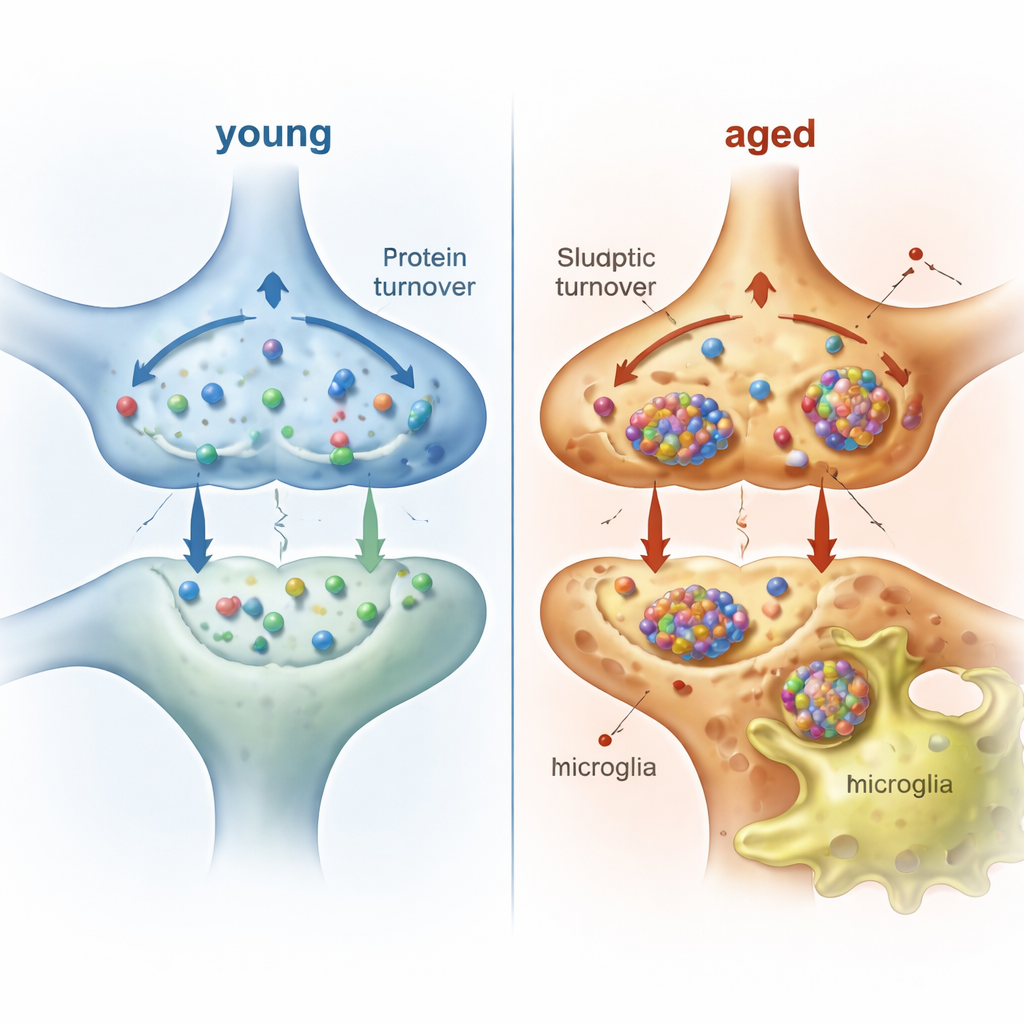
Mikroglej jako ekipa sprzątająca mózgu
Neurony nie radzą sobie z tym obciążeniem samotnie. Mikroglej, rezydujące komórki odpornościowe mózgu, nieustannie nadzorują i przycinają synapsy. Aby zobaczyć, jakie materiał pochodzący od neuronów mikroglej faktycznie pochłania u żywych zwierząt, autorzy znakowali białka neuronalne przez tydzień u młodych i starych myszy, a potem oczyszczali setki tysięcy mikroglejów i izolowali wszelkie oznakowane białka w ich wnętrzu. Wykryto setki białek neuronalnych w mikrogleju, z silną reprezentacją składników synaptycznych, błonowych i mitochondrialnych. Wiele z tych białek ma sekwencje sygnałowe lub jest znane jako ładunek egzosomów, co sugeruje wydzielanie jako jedną z dróg transferu, podczas gdy inne wynikały z pochłaniania przez mikroglej elementów synaptycznych. U starszych myszy mikroglej zawierał więcej rodzajów i większe ilości białek pochodzenia neuronalnego niż u myszy młodych, choć proporcja elementów przed‑ i postsynaptycznych pozostała podobna.
Gdy sprzątanie zawodzi, mózg ponosi konsekwencje
Przecinając trzy zbiory danych — białka, których degradacja zwalnia z wiekiem; białka występujące w neuronalnych agregatach; oraz białka kumulujące się w mikrogleju starych mózgów — badanie zidentyfikowało 166 białek leżących na styku tych procesów. Ponad połowa wszystkich białek pochodzenia neuronalnego wzbogaconych w mikrogleju starych mózgów wykazywała jakiś rodzaj wiekowego zaburzenia proteostazy. Wiele z nich jest kodowanych przez geny wcześniej wskazywane jako czynniki ryzyka choroby Alzheimera, Parkinsona i innych zaburzeń mózgu. Razem wyniki te szkicują kaskadę: wraz z wiekiem obrót białek neuronalnych zwalnia, zwłaszcza w synapsach; wrażliwe białka częściej ulegają niepoprawnemu fałdowaniu i agregacji; a mikroglej coraz intensywniej usuwa te uszkodzone składniki, prawdopodobnie poprzez pochłanianie zestresowanych synaps. W krótkim okresie może to chronić neurony, ale przez dziesięciolecia może przyczyniać się do utraty synaps i pogorszenia funkcji poznawczych. Zrozumienie i ostateczne przywrócenie zdrowej proteostazy neuronalnej może zatem być kluczową strategią zachowania odporności mózgu w późniejszym życiu.
Cytowanie: Guldner, I.H., Wagner, V.P., Moran-Losada, P. et al. Ageing promotes microglial accumulation of slow-degrading synaptic proteins. Nature 650, 930–941 (2026). https://doi.org/10.1038/s41586-025-09987-9
Słowa kluczowe: starzenie mózgu, obieg białek, synapsy, mikroglej, neurodegeneracja