Clear Sky Science · pl
Ochrona metaboliczna zależna od poliamin reguluje alternatywny splejzing
Jak maleńkie cząsteczki pomagają komórkom czytać geny
W każdej komórce ten sam zapis DNA można odczytywać na wiele sposobów, co pozwala niewielkiej liczbie genów wytwarzać ogromną różnorodność białek. Ta elastyczność zależy od procesu zwanego alternatywnym splejzingiem, który edytuje komunikaty RNA przed ich przetłumaczeniem na białka. Artykuł ten ujawnia, że małe, dodatnio naładowane cząsteczki zwane poliaminami dyskretnie kierują tym etapem edycji, działając jak rodzaj ochronnej osłony, która pomaga komórkom decydować, które wersje RNA tworzyć. Ponieważ alternatywny splejzing odgrywa kluczową rolę w raku, funkcjonowaniu mózgu i komórkach macierzystych, odkrycie tej ukrytej warstwy kontroli ma dalekosiężne implikacje dla zdrowia i chorób.
Małe naładowane pomocniki w każdej komórce
Poliaminy to niewielkie, elastyczne cząsteczki niosące wiele ładunków dodatnich. Komórki syntetyzują je z podstawowych składników odżywczych i od dawna wiadomo, że wspierają wzrost i przetrwanie, zwłaszcza w szybko dzielących się komórkach, takich jak guzy. Autorzy postawili pytanie, czy poliaminy służą także jako sygnały, a nie tylko jako „paliwo”. Poprzez częściowe zablokowanie produkcji poliamin w komórkach raka prostaty i u myszy zmierzyli, jak zmieniają się białka i RNA w czasie. Odkryli, że długo zanim całkowity poziom poliamin znacząco spadł, wystąpiła silna fala zmian w fosforylacji białek — chemicznych znacznikach włączających lub wyłączających przełączniki białkowe — szczególnie na składnikach maszynerii edycji RNA, spliceosomu.
Ponowne okablowanie „edytora” RNA w komórce
Skupiając się konkretnie na RNA, zespół wykorzystał głębokie sekwencjonowanie, aby śledzić alternatywny splejzing po zahamowaniu syntezy poliamin. Setki fragmentów RNA były pomijane lub włączane w inny sposób, zarówno w liniach komórkowych raka, jak i w normalnych typach komórek oraz tkankach myszy. Zmiany te nie były prostym efektem ubocznym spowolnionego podziału komórek ani innego znanego procesu zależnego od poliamin, zwanego hypusynacją. Zamiast tego, gdy badacze uzupełnili komórkom poliaminy z zewnątrz, wiele przesunięć w splejzingu wróciło w kierunku stanu normalnego. Zarówno leki, jak i narzędzia genetyczne obniżające poziom poliamin wywołały podobne wzory splejzingu, a dalsze obniżenie poliamin kombinacją leków wzmocniło te zmiany, potwierdzając silne powiązanie efektu z dostępnością poliamin.
Ukryty cel: moduł SF3 splajsinowy
Aby określić, gdzie w maszynerii splejzingu działają poliaminy, autorzy porównali sygnaturę splejzingu spowodowaną obniżeniem poliamin z dużą mapą referencyjną stworzoną przez indywidualne wyciszanie ponad 300 znanych czynników splejzingu. Najbliższe dopasowanie wskazało na konkretną część spliceosomu zwaną podkompleksem SF3, która pomaga rozpoznawać kluczowe sygnały w RNA. Analiza obliczeniowa publicznych danych o wiązaniu białko–RNA wspierała to powiązanie: RNA, których splejzing został zmieniony przez utratę poliamin, były szczególnie często wiązane przez białka SF3. Gdy zespół częściowo wyłączył komponenty SF3 genetycznie lub przy użyciu leku, efekty splejzingu związane z deplecją poliamin zostały w dużej mierze zlikwidowane, co pokazuje, że nienaruszona aktywność SF3 jest wymagana dla tej nowej ścieżki regulacyjnej. 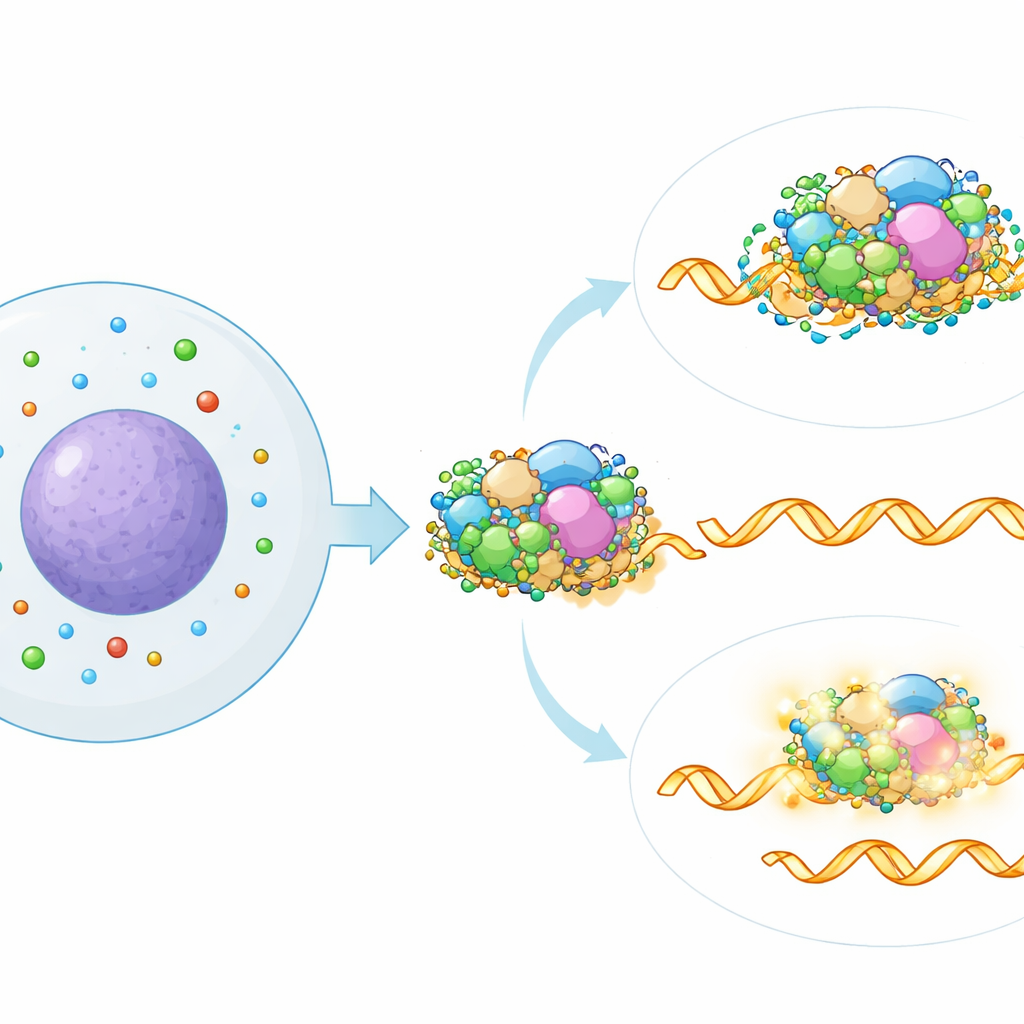
Ochrona metaboliczna: jak poliaminy blokują znakowanie białek
Głębiej analizując mechanizm, badacze zauważyli, że najsilniej dotknięte miejsca fosforylacji w białkach SF3 skupiały się w krótkich odcinkach bogatych w aminokwasy o ładunku ujemnym. Modele molekularne i eksperymenty z rezonansu magnetycznego wykazały, że poliaminy wpasowują się w te zasadowe (kwasowe) łatki, tworząc wielokrotne kontakty elektrostatyczne i częściowo przykrywając pobliskie reszty seryny, gdzie zwykle przyłączane są grupy fosforanowe. To fizyczne „objęcie” zmniejsza dostępność tych miejsc dla kinaz białkowych — enzymów przyłączających fosforany. W eksperymentach in vitro dodanie poliamin bezpośrednio blokowało kinazę CK1 przed fosforylowaniem białek SF3. W komórkach hamowanie CK1 i jego bliskiego odpowiednika CK2 tłumiło zmiany splejzingu wywołane utratą poliamin, a specjalnie zaprojektowane myszy, których białko SF3A3 pozbawiono trzech kluczowych miejsc fosforylacji, stały się w dużej mierze niewrażliwe na przesunięcia splejzingu zależne od poliamin. 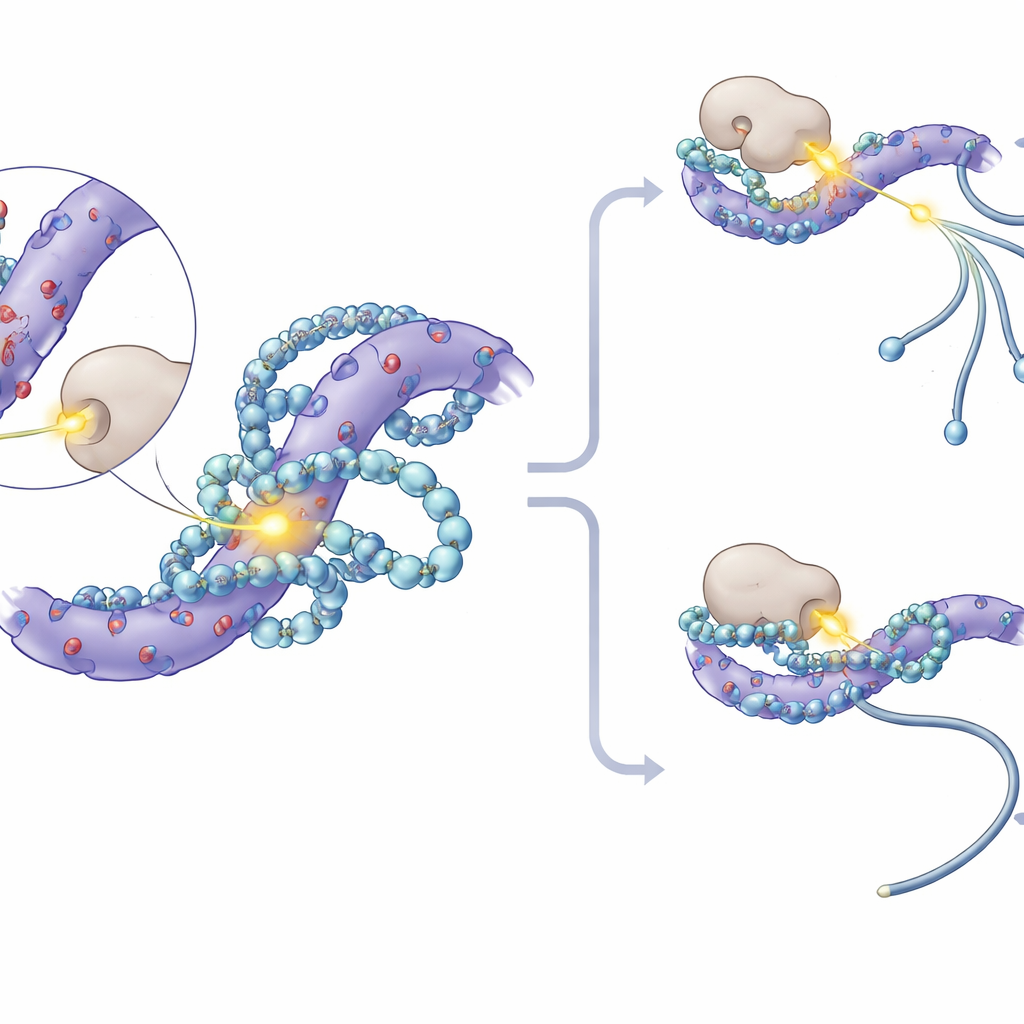
Projektowana cząsteczka oddzielająca role
W badaniu wprowadzono również lek podobny do poliaminy, BENSpm, który ma silniejszy ładunek dodatni, ale jednocześnie hamuje własną produkcję poliamin przez komórkę. BENSpm wiązał się mocno z kwaśnymi łatkami SF3 i blokował działanie kinaz, podobnie jak naturalne poliaminy, jednak nie przywracał wzrostu komórek, gdy brakowało prawdziwych poliamin. To umożliwiło autorom rozdzielenie klasycznych funkcji poliamin (wspierania wzrostu i metabolizmu) od nowo zdefiniowanej roli ochronnej. W embrionalnych komórkach macierzystych myszy deplecja poliamin skłaniała komórki do utraty markera „stemness” Nanog i zmieniała ich krajobraz splejzingu. BENSpm przywracał zarówno profil splejzingu, jak i ekspresję Nanog pomimo trwającego tłumienia normalnej syntezy poliamin, co wskazuje, że ochrona metaboliczna jest kluczowym wymogiem dla utrzymania tożsamości komórek macierzystych.
Dlaczego to odkrycie ma znaczenie
Mówiąc obrazowo, praca ta pokazuje, że poliaminy działają jak maleńkie ochronne rękawiczki wokół wrażliwych części kluczowych białek splejzingu. Gdy rękawiczki są na miejscu, kinazy nie mogą łatwo chwycić i oznakować tych miejsc, a edycja RNA przebiega zgodnie z planem. Gdy poliamin jest mało, rękawiczki znikają, fosforylacja narasta, a wzory splejzingu przesuwają się, z konsekwencjami dla komórek nowotworowych i komórek macierzystych. Poprzez zdefiniowanie tego mechanizmu „ochrony metabolicznej” oraz dostarczenie narzędzia w postaci cząsteczki go naśladującej, badanie otwiera drogę do nowych sposobów modulowania odczytu genów bez zmiany samego DNA, potencjalnie inspirując przyszłe terapie celujące w splejzing w onkologii i medycynie regeneracyjnej.
Cytowanie: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Słowa kluczowe: poliaminy, alternatywny splejzing, przetwarzanie RNA, sygnalizacja metaboliczna, regulacja komórek macierzystych