Clear Sky Science · pl
Trajektorie aktywacji zależne od ligandu determinują sygnalizację GPCR w komórkach
Jak jeden receptor może zachowywać się jak wiele przełączników
Wiele współczesnych leków działa na dużą rodzinę białek znajdujących się na powierzchni komórek, zwanych receptorami sprzężonymi z białkiem G, czyli GPCR. Receptory te wpływają na częstość akcji serca, nastrój, oddychanie i niezliczone inne funkcje organizmu. Przez dekady traktowano je jak proste przełączniki włącz/wyłącz: lek wiąże się, przełącznik zostaje odwrócony i sygnał trafia do wnętrza komórki. Ten artykuł pokazuje jednak, że rzeczywistość jest znacznie bogatsza. Wykorzystując nowy rodzaj fluorescencyjnego „szpiega” wbudowanego bezpośrednio w receptor, autorzy obserwują w żywych komórkach, jak różne leki prowadzą ten sam receptor różnymi ścieżkami aktywacji — jak wybieranie różnych tras przez miasto — co skutkuje różnymi wzorcami sygnalizacji. Zrozumienie tych ukrytych tras może pomóc w projektowaniu leków, które dają pożądany efekt przy jednoczesnym unikaniu skutków ubocznych.
Obserwowanie „dzwonka do drzwi” komórki w czasie rzeczywistym
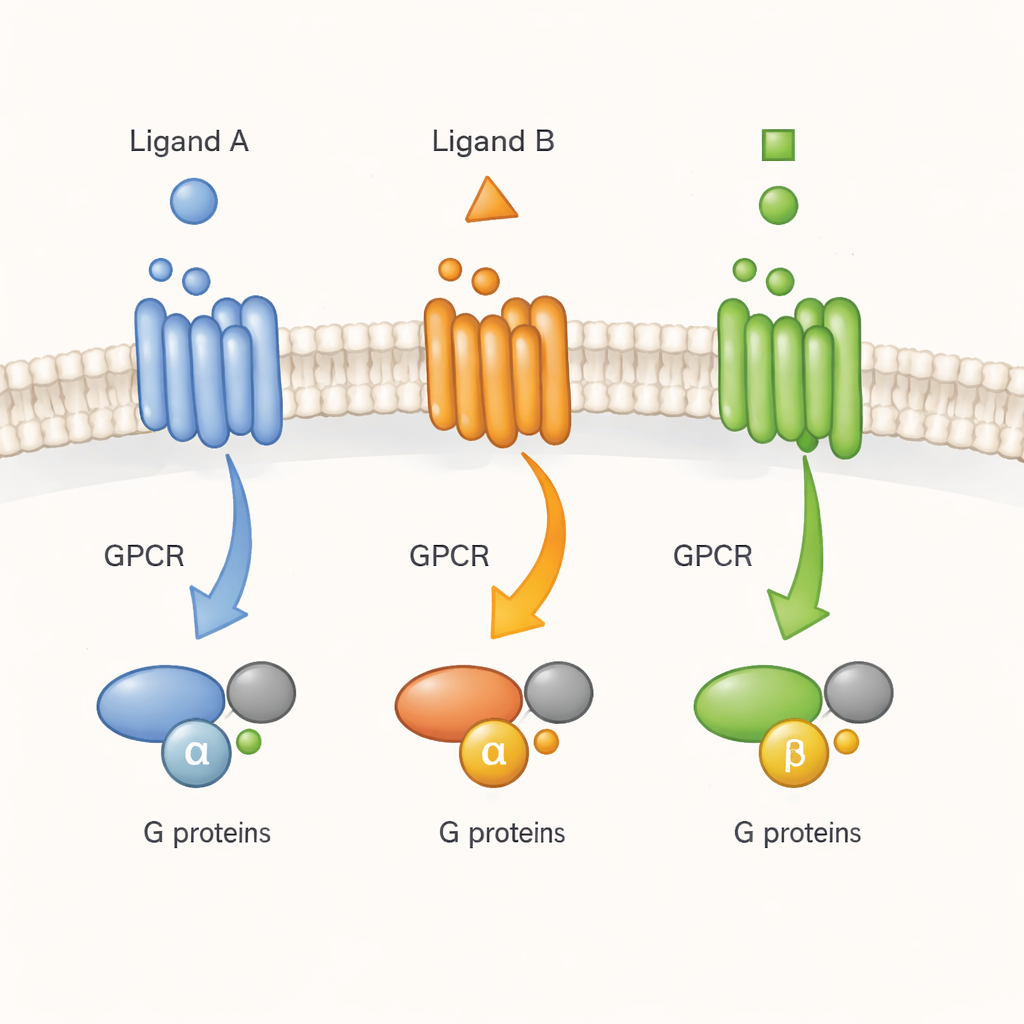
GPCR bywa opisany jako molekularny dzwonek do drzwi: cząsteczka sygnałowa (ligand) dzwoni z zewnątrz, a receptor przekazuje wiadomość do białek G wewnątrz komórki. Wcześniejsze badania z oczyszczonymi receptorami w detergentach sugerowały, że GPCR nie przełączają się po prostu między jednym stanem nieaktywnym a jednym aktywnym. Zamiast tego próbkują wiele kształtów, które leki mogą stabilizować w różnym stopniu. Nie było jednak jasne, czy ta złożoność istnieje również w zatłoczonym, dynamicznym środowisku żywej komórki. W tej pracy autorzy skupili się na jednym reprezentatywnym receptorze, muskarynowym receptorze acetylocholiny M2, ważnym regulatorze pracy serca i aktywności nerwowej, i zadali pytanie, czy różne ligandy napędzają go do odmiennych aktywnych form, które mają znaczenie dla rzeczywistej sygnalizacji komórkowej.
Budowanie maleńkich świetlnych reporterów na powierzchni receptora
Aby śledzić ruchy receptora bez zakłócania jego normalnej funkcji, zespół zastosował rozszerzenie kodu genetycznego, technologię pozwalającą wstawić specjalny zaprojektowany aminokwas w wybranych pozycjach na zewnętrznej powierzchni receptora. Ten chemiczny „kotwica” może zostać połączona z małą barwną substancją fluorescencyjną w żywych komórkach. Przeskanowawszy 72 pozycje i zachowując tylko te, które wciąż zachowywały się jak normalne receptory, zbudowali panel siedmiu wariantów receptora M2, z których każdy nosił pojedynczy barwnik w innym miejscu pętli zewnętrznej. Po zastosowaniu naturalnego przekaźnika, acetylocholiny, jasność barwnika w tych miejscach rosła lub malała w charakterystyczny sposób, ujawniając, jak każda część zewnętrznej powierzchni receptora zmieniała się w miarę rozpoczynania się sygnalizacji. Co kluczowe, te znakowane receptory wciąż potrafiły aktywować białka G i przechodzić normalną internalizację, co pokazuje, że sensory były wierne, a nie zakłócające.
Leki zostawiają odrębne „odciski konformacyjne”
Naukowcy porównali następnie kilka leków, które wszystkie uruchamiają receptor M2, lecz z różną siłą: własna acetylocholina organizmu, bardzo silny syntetyczny agonista iperoks, oraz dwóch słabszych agonistów częściowych, arekolina i pilokarpina. Każdy lek wywołał unikalny wzór zmian fluorescencji w siedmiu miejscach reporterowych — odcisk konformacyjny. W większości pozycji wielkość przemieszczenia korelowała z siłą, z jaką lek aktywował receptor. Jednak w dwóch miejscach relacja była odwrócona: silniejsze zmiany wywoływały słabsze leki, a najsilniejszy lek prawie ich nie wywoływał. Takie zachowanie nie da się wyjaśnić pojedynczym stanem aktywnym. Wskazuje ono raczej, że ten sam receptor w żywych komórkach może przyjmować kilka odrębnych aktywnych kształtów — niektóre preferowane przez silne leki, inne przez słabe.
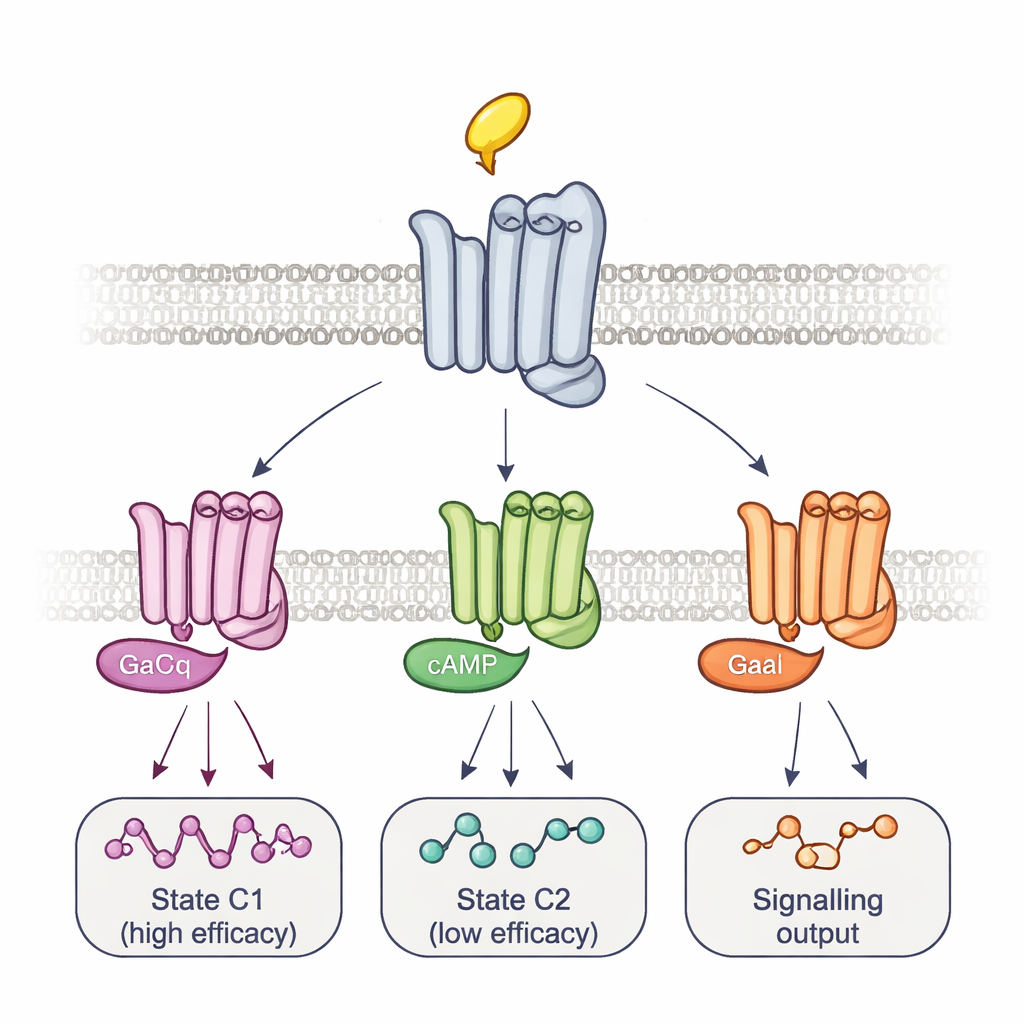
Wiele kompleksów i czasowe trasy do sygnalizacji
Aby powiązać te kształty z rzeczywistą sygnalizacją, zespół zmodyfikował same białka G. Nadmierna ekspresja mutanta białka G, które tworzy bardzo silne, długotrwałe kompleksy z receptorami, selektywnie wymazała sygnał z niektórych miejsc reporterowych, wzmacniając jednocześnie inne. Ten wzór, razem z czasowaniem zmian fluorescencji, ujawnił co najmniej dwa główne kompleksy receptor–białko G: szybko tworzący się kompleks o wysokiej skuteczności oraz wolniejszy o niskiej skuteczności. Różne leki przesuwały równowagę między tymi kompleksami, a nawet korzystały z różnych pośrednich kroków, by do nich dojść, śledząc specyficzne dla leku trajektorie aktywacji. W osobnym teście bioluminescencyjnym monitorującym panel 14 podtypów białek G autorzy pokazali, że te równowagi pomagają określić nie tylko jak silnie lek aktywuje sygnalizację ogólnie, ale które dokładnie białka G zostają włączone. Na przykład arekolina preferencyjnie aktywowała pewne białka Go, podczas gdy pilokarpina silnie faworyzowała kompleks o niskiej skuteczności.
Dlaczego to ma znaczenie dla lepszych leków
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że pojedynczy receptor nie jest jednym przełącznikiem, lecz zbiorem powiązanych przełączników, z których każdy jest osiągalny różnymi ścieżkami i każdy połączony z nieco odmiennymi efektami położonymi dalej w kaskadzie. To badanie dostarcza bezpośredniego wglądu w te ścieżki i stany w nienaruszonych komórkach, zamiast w uproszczonych systemach probówkowych. Mapując, jak konkretne leki stronnicują receptor ku określonym kompleksom i partnerom białek G, badacze otrzymują plan projektowania „mądrzejszych” leków — związków, które skłaniają receptory do stanów wywołujących korzystne sygnały, unikając tych związanych ze skutkami ubocznymi. Opracowana tu strategia fluorescencyjnych biosensorów powinna być adaptowalna do wielu innych receptorów, otwierając okno na choreografię działania leków w czasie rzeczywistym w żywych komórkach.
Cytowanie: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Słowa kluczowe: sygnalizacja GPCR, skuteczność ligandu, białka G, biosensory konformacyjne, poszukiwanie leków