Clear Sky Science · pl
Mikrobiota‑indukowana plastyczność limfocytów T umożliwia immunologiczną kontrolę nowotworu
Jak przyjazne mikroby jelitowe mogą pomóc w walce z rakiem
Immunoterapia nowotworów zrewolucjonizowała leczenie wielu pacjentów, lecz tylko część z nich obserwuje zmniejszenie guzów i trwałą remisję. To badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: czy konkretne bakterie jelitowe mogą „wyszkolić” komórki odpornościowe w taki sposób, by leki blokujące punkty kontrolne, na przykład terapia anty–PD‑1, działały lepiej? Śledząc wędrówkę komórek odpornościowych od jelita cienkiego do guzów u myszy, autorzy ujawniają bezpośrednie, możliwe do przetestowania powiązanie między pojedynczym mikrobiem jelitowym a skuteczną kontrolą nowotworu.
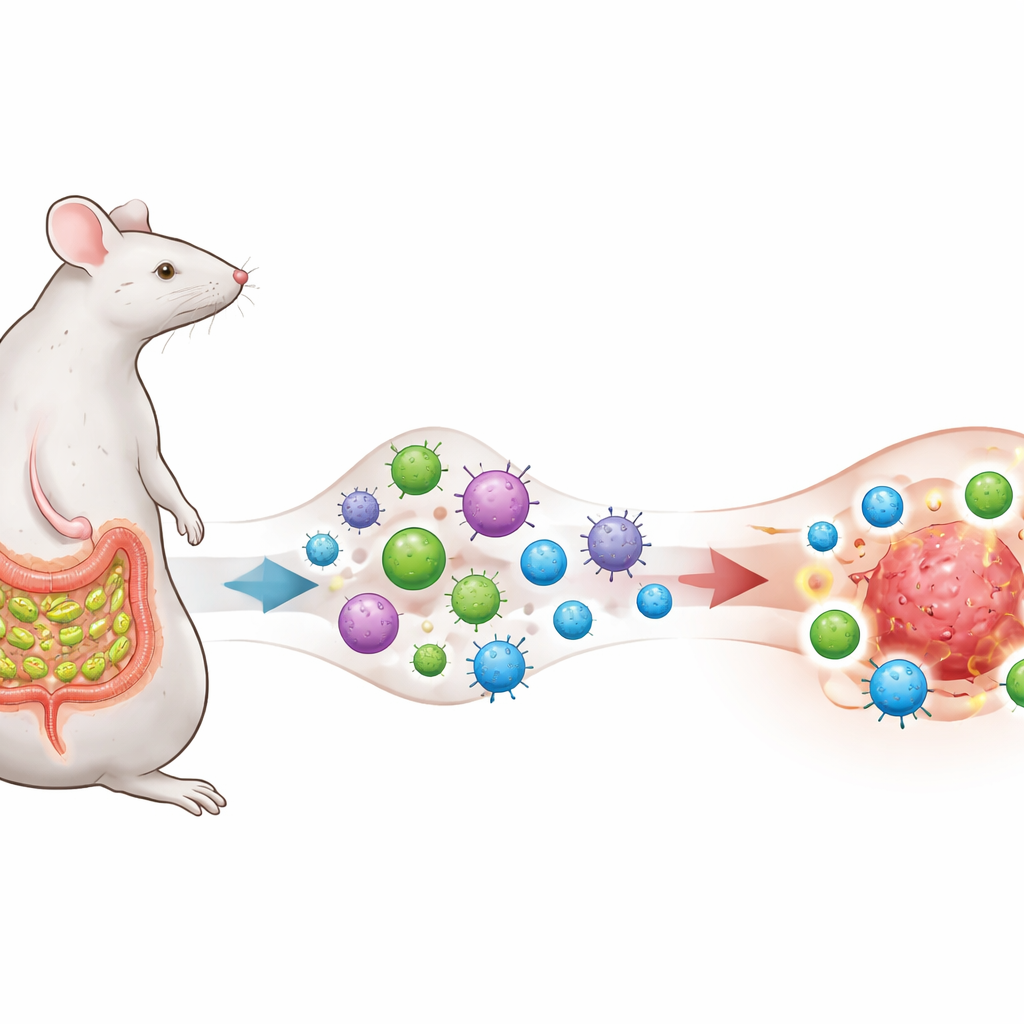
Mikrob, który szkoli układ odpornościowy
Naukowcy skupiają się na bakterii jelitowej zwanej segmentowanymi bakteriami nitkowatymi (SFB), znanej z bytowania blisko nabłonka jelita cienkiego u myszy i z wywoływania silnej, lecz zwykle homeostatycznej odpowiedzi pomocniczych limfocytów T typu 17 (TH17). Inżynierują komórki czerniaka, raka płuca i jelita tak, aby prezentowały fragment białka występujący również w SFB, tworząc celowo „nakładanie antygenów” między mikrobiem a guzami. Myszy pozostają albo wolne od SFB, albo są skolonizowane tym mikrobem, a wszystkie otrzymują terapię anty–PD‑1, powszechnie stosowane przeciwciało blokujące punkty kontrolne, mające zdjąć hamulec z limfocytów T.
Komórki uwarunkowane przez jelito zamieniają guzy z „zimnych” w „gorące”
Terapia anty–PD‑1 sama w sobie lub obecność SFB bez zmian niewiele zmniejsza wzrost guzów. Jednak gdy guzy niosą antygen pochodzący od SFB, a myszy są skolonizowane SFB, anty–PD‑1 nagle staje się wysoce skuteczne: guzy ulegają skurczeniu, przeżywalność się poprawia, a przeżywające zwierzęta odrzucają późniejsze ponowne wszczepienie guza bez dodatkowego leczenia, co wskazuje na trwałą pamięć immunologiczną. U tych pomyślnych myszy guzy wypełniają agresywne CD8 „zabójcze” limfocyty T produkujące interferon‑γ i inne toksyczne cząsteczki, podczas gdy supresyjne komórki regulatorowe stanowią mniejszy udział w populacji odpornościowej. Krótko mówiąc, lokalne środowisko wokół nowotworu zostaje przekształcone z relatywnie „zimnego” i nieodpowiadającego w „gorące” i zapalne.
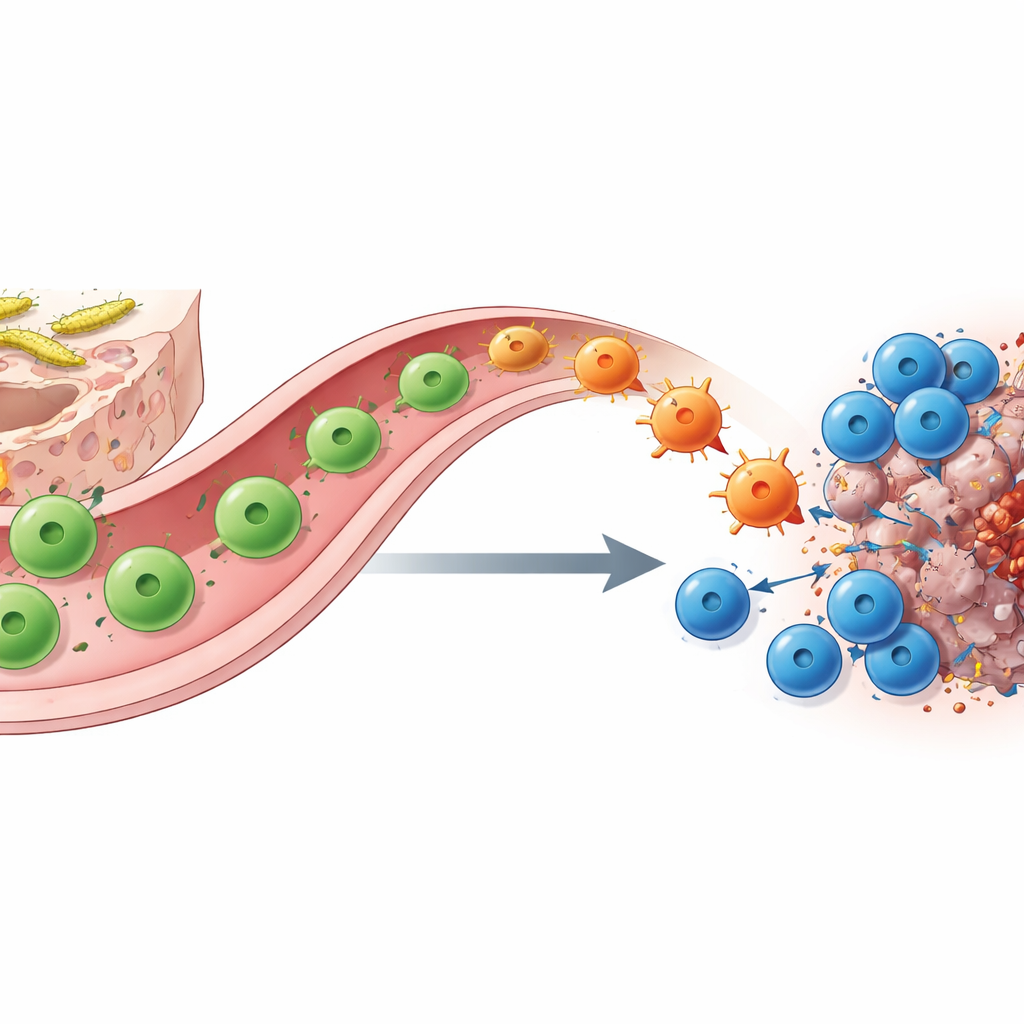
Helpery T o zmiennej formie łączą jelito z guzem
Jak kolonizacja SFB wywołuje tę zmianę? Dzięki zastosowaniu molekularnego kodowania, sekwencjonowania pojedynczych komórek i sprytnemu śledzeniu genetycznemu autorzy pokazują, że kluczowymi graczami są swoiste dla SFB pomocnicze limfocyty CD4. W jelicie cienkim komórki te zaczynają jako TH17 wspierające funkcję bariery i normalnie produkujączączą cząsteczkę IL‑17A. Gdy napotykają dopasowany antygen w guzie w obecności blokady punktów kontrolnych, migrują z jelita do miejsca guza i „re‑specjalizują się” w komórki podobne do TH1, które zamiast tego wydzielają duże ilości interferonu‑γ i TNF. Te przekształcone „byłe TH17” wspierają prezentację antygenu i wydzielają chemotaktyczne sygnały, przyciągając i wzmacniając CD8 zabójcze limfocyty T. Usunięcie zarówno pomocniczych, jak i zabójczych limfocytów T lub genetyczne usunięcie komórek linii IL‑17A, które służą jako prekursor, w dużym stopniu znosi korzyść z anty–PD‑1, podkreślając ich współdziałanie.
Nie wszystkie mikroby dają pomocne instrukcje
Aby sprawdzić, czy wystarczy każdy mikroorganizm jelitowy z nakładającymi się antygenami, zespół powtórzył eksperyment z innym drobnoustrojem komensalnym, Helicobacter hepaticus. Ten organizm również wywołuje silne odpowiedzi T, ale przeważnie rozszerza populacje komórek o charakterze regulatorowym, które tłumią zapalenie. Gdy guzy są zaprojektowane tak, by prezentować antygen H. hepaticus, a myszy są skolonizowane tym bakterią, terapia anty–PD‑1 nie poprawia wyników. Chociaż wiele pomocniczych limfocytów swoistych dla H. hepaticus trafia do guza, zachowują one charakter regulatorowy i produkują niewiele interferonu‑γ, nie aktywując skutecznie komórek zabójczych. To porównanie pokazuje, że to jakość i plastyczność programów limfocytów T indukowanych przez mikroby — nie tylko dopasowanie antygenu — decydują, czy mikrobiota pomoże, czy przeszkodzi immunoterapii nowotworów.
Co to może znaczyć dla przyszłej opieki onkologicznej
Podsumowując, praca dostarcza bezpośredniego dowodu u zwierząt, że określony mikroorganizm jelitowy może wcześniej „wytrenować” pomocnicze limfocyty T w jelicie, wysłać je do guzów dzielących antygen i, w warunkach blokady punktów kontrolnych, sprawić, że zmienią role i staną się potężnymi komórkami walczącymi z nowotworem. Wyjaśniając ten obwód jelito→guz, badanie sugeruje, że starannie dobrane lub zaprojektowane mikroby mogłyby w przyszłości być stosowane obok immunoterapii, aby przekształcić guzy większej liczby pacjentów w podatne na leczenie, zapalne cele — pod warunkiem że te mikroby indukują właściwy, elastyczny, prozapalny program limfocytów T, a nie uspokajający, regulatorowy.
Cytowanie: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
Słowa kluczowe: mikrobiota jelitowa, immunoterapia nowotworów, plastyczność limfocytów T, blokada punktów kontrolnych, mikrośrodowisko guza