Clear Sky Science · pl
Dwukierunkowe ekrany CRISPR odszyfrowują zależny od GLIS3 obwód komórek fibrotycznych
Kiedy gojenie zamienia się w szkodliwe bliznowacenie
Nasze jelita mają zdolność samonaprawy po każdym otarciu i podrażnieniu. W chorobach przewlekłych, takich jak choroba Crohna i wrzodziejące zapalenie jelita grubego, proces ten może wymknąć się spod kontroli, prowadząc do grubienia i stwardnienia tkanki łącznej, zwężenia jelita i konieczności operacji. W badaniu tym odkryto ukrytą rozmowę między komórkami odpornościowymi a komórkami strukturalnymi jelita, która napędza to bliznowacenie, oraz zidentyfikowano główny przełącznik — gen GLIS3 — który może być nową dźwignią do przerwania tego cyklu.
Ukryta sieć w zapalnych jelitach
Aby zrozumieć, dlaczego niektórzy pacjenci rozwijają uporczywe zapalenie i włóknienie (bliznowacenie), badacze stworzyli komórkowy „atlas” ludzkiego jelita. Połączyli sekwencjonowanie RNA pojedynczych komórek, które odczytuje aktywne geny w poszczególnych komórkach, z profilowaniem przestrzennym, które mapuje położenie tych komórek w rzeczywistych wycinkach tkanki. Na próbkach od osób z chorobą Crohna, wrzodziejącym zapaleniem jelita grubego i od osób kontrolnych sporządzili mapę ponad czterech milionów komórek w obrębie ściany jelita. W tym tłumie wyróżniła się jedna podgrupa fibroblastów: fibroblasty związane z zapaleniem, oznaczone jako IAF. Komórki te skupiały się w obszarach aktywnego i przewlekłego zapalenia jelita i nosiły sygnaturę genową związaną z opornością na standardowe terapie anty–TNF, co sugeruje, że odgrywają kluczową rolę w trudnoleczalnej postaci choroby. 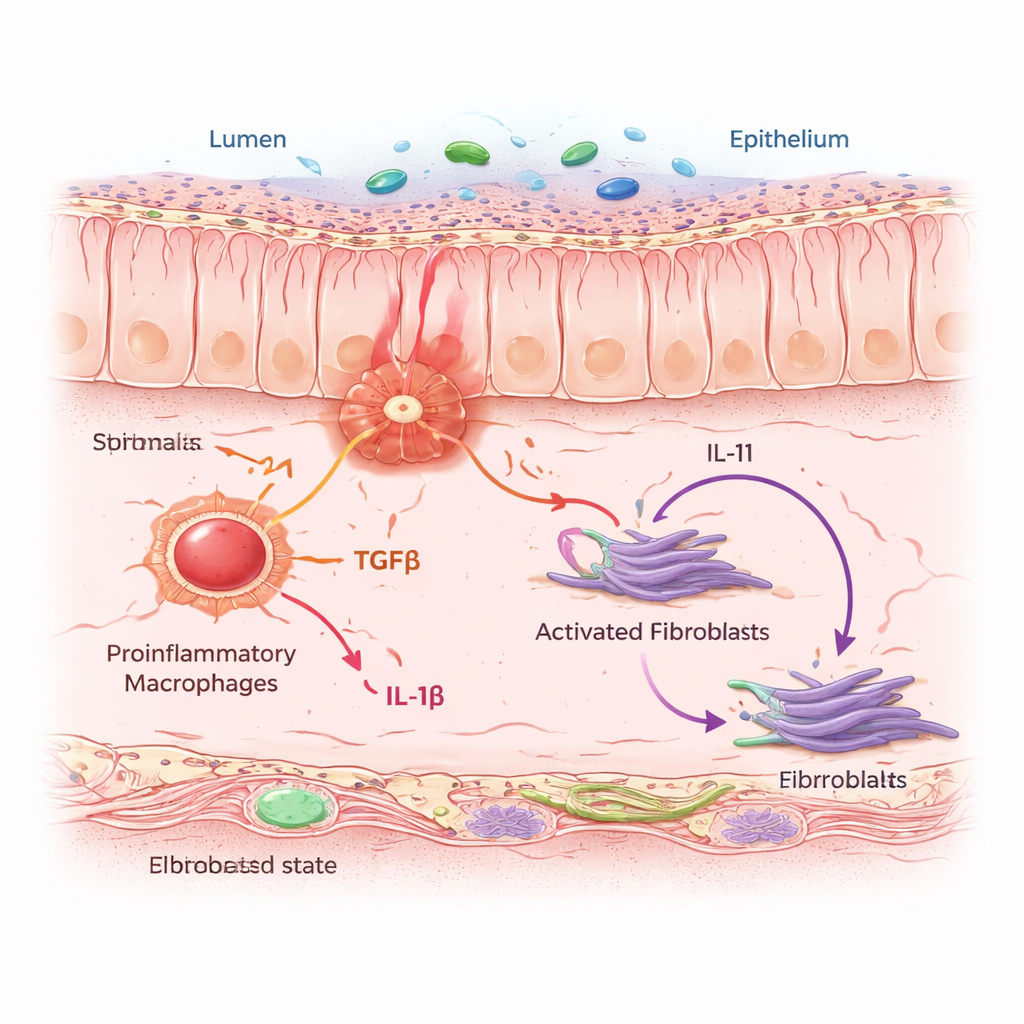
Makrofagi szepczą, fibroblasty bliznowacieją
IAF nie działały w izolacji. Skupiały się w „sąsiedztwach” gęstych w prozapalne makrofagi — komórki odpornościowe, które wykrywają zagrożenie i uwalniają sygnały alarmowe. Dzięki modelom obliczeniowym i eksperymentom współhodowli komórek zespół wykazał, że gdy makrofagi zostają napędzone w stan zapalny, wydzielają dwa kluczowe białka sygnalizacyjne: TGFβ i IL-1β. Okoliczne fibroblasty odbierają te sygnały przez specyficzne receptory. Gdy oba sygnały docierają jednocześnie, fibroblasty przełączają się w stan IAF i zaczynają produkować IL-11 — cytokinę podejrzewaną o promowanie włóknienia — wraz z kolagenem i innymi białkami macierzy, które pogrubiają i usztywniają ścianę jelita. U myszy wystawionych na przewlekły model kolitis blokada IL-11 lub jego selektywne usunięcie w fibroblastach zmniejszała gromadzenie kolagenu, nie zapobiegając jednak początkowemu zapaleniu, co pokazuje, że IL-11 jest kluczowym motorem fazy bliznowacenia.
GLIS3: główny przełącznik w fibroblastach włókniejących
Aby przejść od korelacji do mechanizmów, autorzy użyli potężnych narzędzi CRISPR obejmujących cały genom. Zmodyfikowali ludzkie fibroblasty tak, by produkcję IL-11 można było monitorować za pomocą fluorescencyjnego markera, a następnie przeprowadzili równoległe ekrany, które albo wyłączały geny, albo je aktywowały w całym genomie. Sortując komórki, które produkowały wyjątkowo dużo lub bardzo mało IL-11 po stymulacji TGFβ i IL-1β, zidentyfikowali geny kontrolujące tę odpowiedź. Wśród wielu składników szlaków sygnałowych wyróżnił się jeden czynnik transkrypcyjny — GLIS3. Gdy GLIS3 był wyłączony, fibroblasty produkowały znacznie mniej IL-11; gdy był wzmocniony, poziomy IL-11 rosły. Dalsze eksperymenty wykazały, że GLIS3 przemieszcza się do jądra fibroblastów w odpowiedzi na sygnały od makrofagów, wiąże się bezpośrednio z DNA w pobliżu genu IL11 i innych oraz uruchamia szeroki program genów zapalnych i włóknieniowych, w tym kolagenów i czynników przyciągających kolejne komórki odpornościowe. 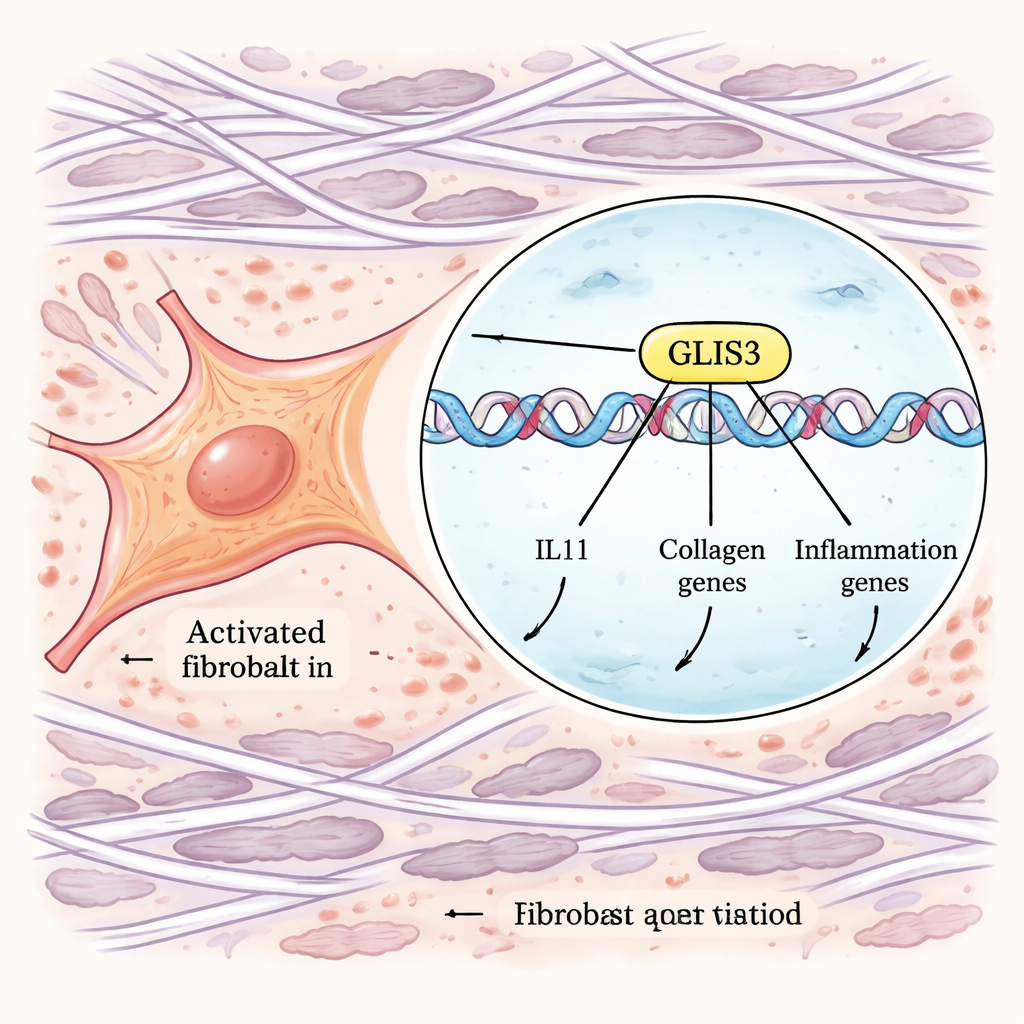
Od modeli mysich do nasilenia u pacjentów
Zespół zapytał następnie, czy program zależny od GLIS3 ma znaczenie w organizmach żywych. U myszy stworzyli linię, w której GLIS3 można było usunąć wyłącznie z fibroblastów. Gdy zwierzęta te były poddane przewlekłemu modelowi kolitis, rozwijały mniejsze bliznowacenie jelita, miały niższe poziomy kolagenu i ekspresji genów włóknieniowych oraz wykazywały zmniejszone zapalenie w porównaniu z normalnymi myszami. Mapowanie przestrzenne potwierdziło, że myszy pozbawione GLIS3 miały mniej fibroblastów produkujących IL-11 oraz mniej pobliskich aktywowanych makrofagów i neutrofili, co wskazuje, że zakłócenie GLIS3 osłabia cały obwód zapalno‑włóknieniowy. Analiza dużej kohorty pediatrycznej z wrzodziejącym zapaleniem jelita grubego pozwoliła autorom wyodrębnić „sygnaturę” GLIS3 obejmującą 50 genów i wykazać, że jej aktywność w biopsjach okrężnicy ściśle koreluje z ciężkością choroby oraz obfitością IAF i aktywowanych makrofagów, łącząc ten szlak bezpośrednio z wynikami u pacjentów.
Przerwać cykl zapalenia i bliznowacenia
Dla odbiorcy niezwiązanego ze specjalistyczną dziedziną sedno jest takie: praca ta ujawnia samonapędzającą się pętlę — zapalne makrofagi pobudzają fibroblasty do przejścia w formę IAF tworzącą blizny; te IAF, pod kontrolą GLIS3, wytwarzają IL-11, kolagen i inne czynniki, które przebudowują tkankę i przyciągają kolejne komórki zapalne. Standardowe leki, które szeroko tłumią układ odpornościowy, mogą nie zrywać tej pętli w pełni, co tłumaczy, dlaczego wielu pacjentów ostatecznie zawodzi terapie istniejące obecnie. Identyfikując GLIS3 i populację fibroblastów produkujących IL-11 jako centralne węzły w obwodzie zapalenie–włóknienie, badanie wskazuje na bardziej celowane strategie — ukierunkowane na fibroblasty, a nie wyłącznie na komórki odpornościowe — które mogłyby w przyszłości zapobiegać lub odwracać bliznowacenie w chorobach zapalnych jelit i być może w innych przewlekłych stanach zapalnych.
Cytowanie: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
Słowa kluczowe: choroba zapalna jelit, zwłóknienie jelit, fibroblasty, makrofagi, GLIS3