Clear Sky Science · pl
Stres kontroluje dziedziczenie heterochromatyny poprzez ubikwitynację histonu H3
Jak komórki pamiętają stres
Nasze komórki potrzebują mechanizmów „pamiętania” przebytego stresu — takiego jak wysoka temperatura, brak składników odżywczych czy ekspozycja na leki — aby móc reagować szybciej przy następnej okazji. Jednym z potężnych systemów pamięciowych jest heterochromatyna, ciasno upakowane DNA, które utrzymuje wyciszenie pewnych genów przez wiele podziałów komórkowych. Artykuł bada, jak komórki aktywnie regulują tę pamięć w odpowiedzi na stres, ujawniając molekularne centrum łączące sygnały środowiskowe z długotrwałymi zmianami aktywności genów. Zrozumienie tego mechanizmu może pomóc wyjaśnić, jak grzyby rozwijają oporność na leki i jak stres przekształca epigenetyczny krajobraz naszych własnych komórek.
Zamek na genomie
Heterochromatynę można sobie wyobrazić jako molekularny zamek na odcinkach DNA, który utrzymuje pobliskie geny w stanie ciszy. Ten zamek budowany jest z chemicznych znaków na białkach histonowych, zwłaszcza oznaczenia zwanego H3K9me3. Gdy się ustanowi, potrafi kopiować się przy każdej replikacji DNA, co umożliwia dziedziczenie wzorców represji genów bez zmiany sekwencji DNA. Do tej pory większość badań sugerowała, że to samo‑kopiowanie opiera się głównie na pętli sprzężenia zwrotnego „czytaj–pisz”: kompleks enzymatyczny rozpoznaje istniejące markery H3K9me3 i dodaje ten sam znak do sąsiednich histonów, stopniowo rozszerzając domenę wyciszenia. Jednak ten model nie tłumaczył w pełni, w jaki sposób warunki środowiskowe przyspieszają, spowalniają lub kierują rozprzestrzenianie się heterochromatyny.
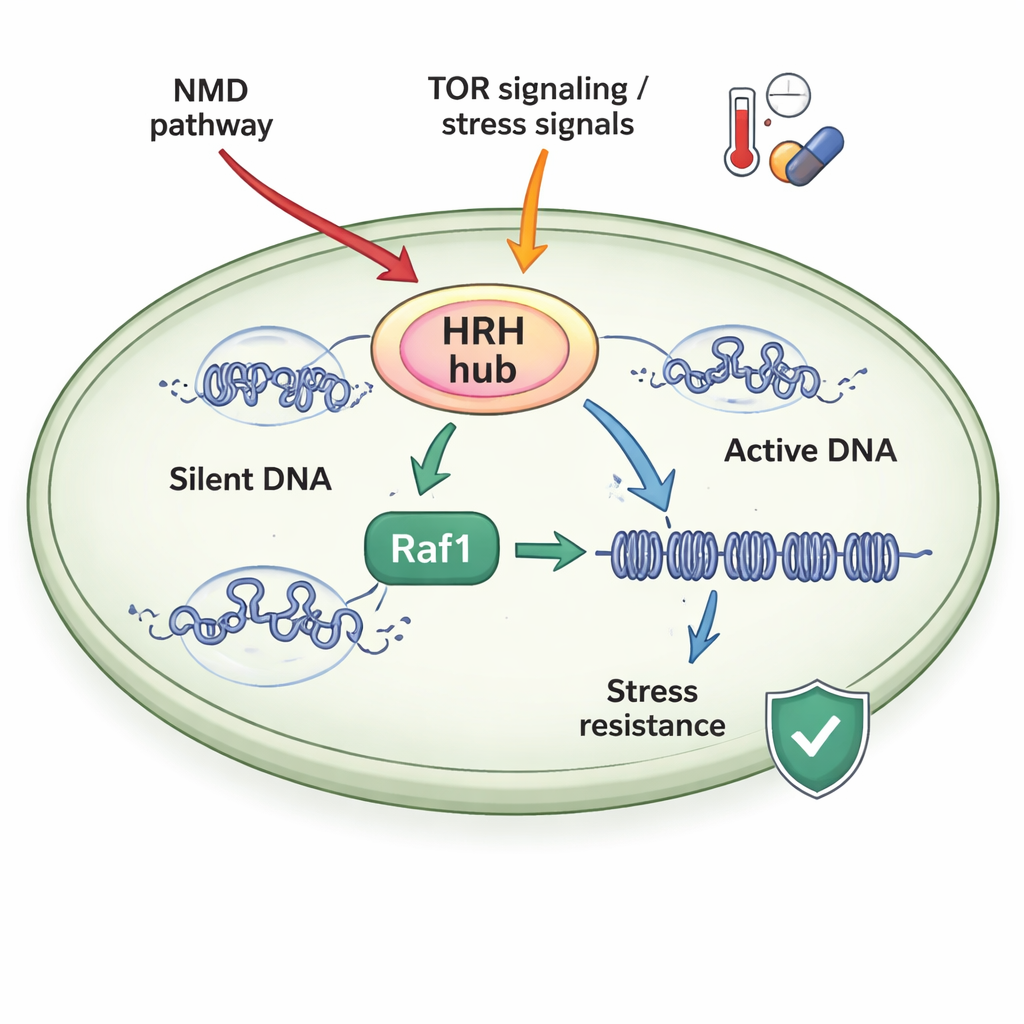
Centrum kontroli wrażliwe na stres
Autorzy badali drożdże podziałowe, prosty organizm modelowy, którego maszyny chromatynowe przypominają te u organizmów wyższych. Skupili się na kompleksie zwanym ClrC, który zarówno „pisze” znak H3K9me3, jak i przyłącza małe białko ubikwitynę w innym miejscu histonu H3 (H3K14ub). Kluczowa podjednostka ClrC, Raf1, działa jako ograniczający „strażnik”: gdy Raf1 jest w niewielkiej ilości, większość głównego enzymu (Clr4) krąży wolno zamiast dołączać do kompleksu na chromatynie, a domeny wyciszenia nie rozszerzają się. Gdy Raf1 jest obfity, więcej kompleksów ClrC formuje się i trwale wiąże z DNA, co pozwala znakom H3K14ub i H3K9me3 rozciągać się wzdłuż chromosomów i wzmacniać wyciszenie genów.
Dostrajanie zamka za pomocą ubikwityny
Mapując markery chromatyny w całym genomie, zespół wykazał, że H3K14ub jest silnie wzbogacony wszędzie tam, gdzie powstaje heterochromatyna, i że ten znak praktycznie znika po usunięciu Raf1. Gdy komórki niosą mutację blokującą krok przyłączania ubikwityny (przy zachowanym H3K9me3 w punkcie startowym), domeny wyciszenia nie potrafią się rozprzestrzeniać na zewnątrz. Innymi słowy, H3K14ub nie jest tylko ozdobą; jest konieczny do napędzania frontu heterochromatyny. Eksperymenty biochemiczne i obrazujące wyjaśniają dlaczego: H3K14ub znacznie zwiększa aktywność enzymu Clr4 i pomaga utrzymać cały kompleks na chromatynie, podnosząc lokalne stężenie H3K9me3 ponad próg wymagany do stabilnego dziedziczenia. Co więcej, zwiększenie poziomu Raf1 potrafi zastąpić kilka innych czynników zwykle niezbędnych do utrzymania tych domen wyciszenia, podkreślając, że regulacja ubikwitynacją napędzana przez Raf1 jest centralnym dźwignią kontroli.
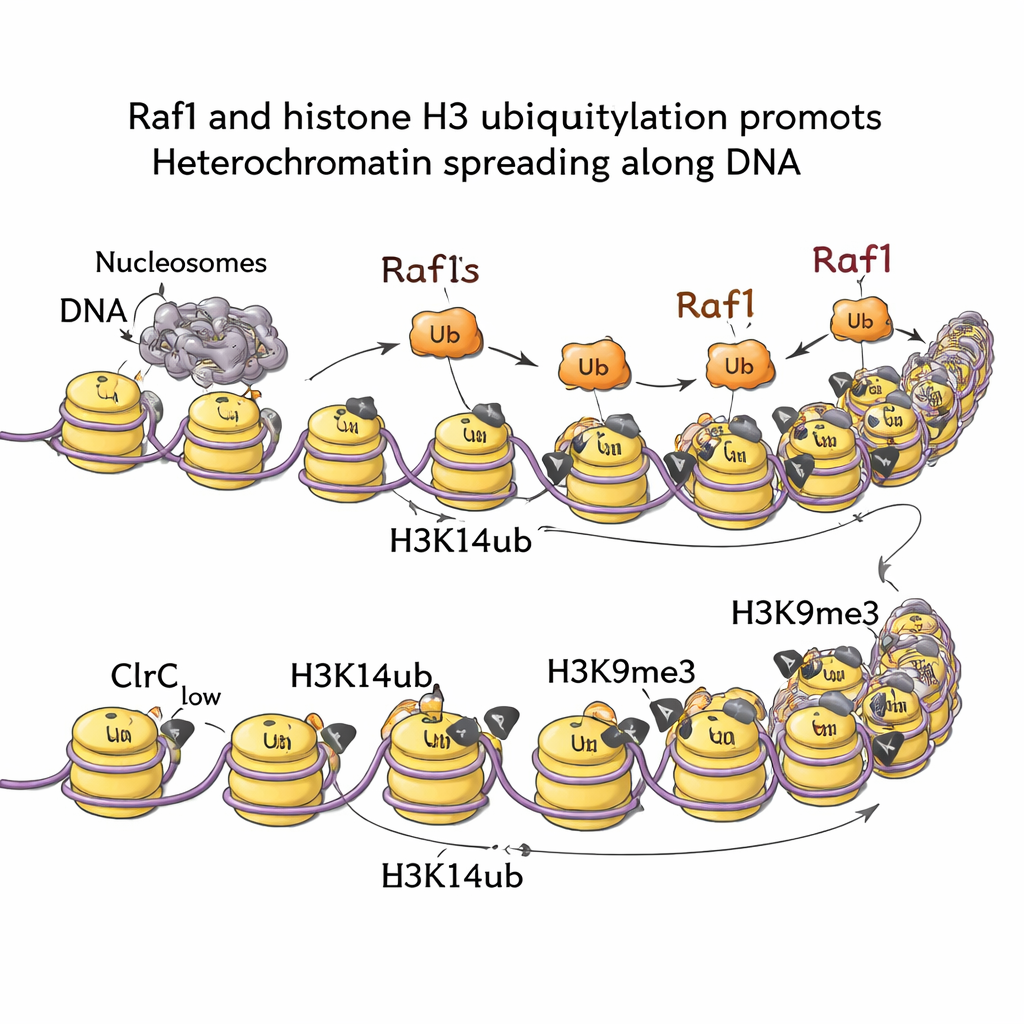
Sygnały z szlaków degradacji RNA i wzrostu
Komórki nie pozostawiają poziomów Raf1 przypadkowi. Badanie pokazuje, że dwa główne systemy reagujące na stres wpływają na to, co autorzy nazywają regulacyjnym centrum dziedziczności heterochromatyny (HRH), skupionym wokół Raf1. Po pierwsze, szlak nonsensownej degradacji (NMD) — znany z niszczenia wadliwych mRNA — celuje w mRNA kodujące Raf1, utrzymując poziomy Raf1 niskie w normalnych warunkach. Wyłączenie NMD stabilizuje RNA Raf1, zwiększa obfitość białka Raf1 i przywraca rozprzestrzenianie heterochromatyny w mutantach, które w innych warunkach nie potrafią utrzymać domen wyciszenia. Po drugie, sensor wzrostu i stresu zwany TORC2, działający przez kinazę Gad8, promuje ekspresję Raf1. Wysoka temperatura wyłącza ten szlak, obniżając poziomy Raf1, osłabiając heterochromatynę i utrudniając komórkom utrzymanie stanów wyciszenia, chyba że Raf1 zostanie eksperymentalnie podwyższony.
Stres, oporność na leki i szersze implikacje
Autorzy łączą następnie to molekularne centrum z adaptacją w praktyce. Ekspozycja drożdży na kofeinę, stres znany również z osłabiania NMD w innych systemach, podnosi poziomy Raf1 i wzmacnia rozprzestrzenianie heterochromatyny do nowych miejsc, w tym genów, których wyciszenie nadaje oporność na kofeinę i leki przeciwgrzybicze. Podobnie, komórki z sztucznie podwyższonym Raf1 stają się bardziej odporne na flukonazol i klotrymazol, powszechnie stosowane środki przeciwgrzybicze. Odwrotnie, gdy Raf1 jest zmniejszony — przez wysoką temperaturę lub utratę sygnalizacji TORC2–Gad8 — heterochromatyna staje się niestabilna, a pamięć epigenetyczna zanika, chyba że Raf1 zostanie przywrócony. Ponieważ białka podobne do Raf1, kompleks ClrC i znacznik H3K14ub mają odpowiedniki w patogennych grzybach i u ssaków, odkrycia te sugerują, że podobne centrum epigenetyczne wykrywające stres może kształtować oporność na leki, rozwój i choroby u wielu gatunków.
Dlaczego to ma znaczenie
W codziennym ujęciu praca ta pokazuje, że wyciszanie genów przez chromatynę nie jest sztywnym zamkiem, lecz inteligentnym, regulowanym systemem. Komórki używają centralnego centrum do odczytywania sygnałów środowiskowych — zmian temperatury, stanu odżywienia, stresów chemicznych — i zwiększają lub zmniejszają poziom Raf1. To z kolei reguluje, jaka część genomu otoczona jest długotrwałą ciszą i jak łatwo komórki mogą „przeprogramować” się bez mutacji DNA. Odkrycie kluczowej roli ubikwitynacji histonu H3 i dawki Raf1 w tym procesie dostarcza schematu, w jaki sposób stres szybko przekształca epigenetyczny krajobraz — oraz wskazuje potencjalne drogi wpływania na oporność grzybów na leki lub patologiczne wyciszanie genów u ludzi.
Cytowanie: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Słowa kluczowe: heterochromatyna, dziedziczenie epigenetyczne, ubikwitynacja histonów, adaptacja na stres, oporność grzybów na leki