Clear Sky Science · pl
Rozwiązywanie integralności strukturalnej origami DNA i farmakokinetyki in vivo
Obserwowanie maleńkich maszyn DNA w organizmie
DNA można składać jak papier w mikroskopijne, trójwymiarowe kształty — technikę tę nazywa się origami DNA. Te nanostruktury można zaprogramować tak, by precyzyjnie przenosiły leki, szczepionki lub cząsteczki sygnalizacyjne. Ale po wstrzyknięciu do organizmu czy pozostają wystarczająco długo nienaruszone, by zadziałać, czy też szybko się rozpadają? Ten artykuł przedstawia nowy sposób obserwacji tych maszyn DNA działających w żywych zwierzętach, ujawniając, jak długo przetrwają, jak poruszają się w krwiobiegu, a nawet które fragmenty każdej struktury ulegają zniszczeniu jako pierwsze.
Dlaczego składanie DNA może zmienić medycynę
Origami DNA wykorzystuje te same zasady parowania zasad, które przechowują naszą informację genetyczną, ale wykorzystuje je do budowy obiektów w nanoskali. Naukowcy mogą rozmieszczać na tych obiektach białka, leki czy sygnały pobudzające układ odpornościowy jak wypustki na płycie Lego, tworząc wysoce kontrolowane terapie przeciwnowotworowe, przeciwautoimmunologiczne i przeciw infekcjom. Aby takie precyzyjne terapie były bezpieczne i skuteczne, regulatorzy i naukowcy muszą wiedzieć, jak nienaruszone te struktury pozostają w organizmie i jak szybko są usuwane — razem znane jako ich farmakokinetyka. Istniejące metody śledzenia zwykle dołączają barwniki fluorescencyjne lub po prostu liczą fragmenty DNA, co może sprawiać, że rozłożone szczątki wyglądają jak w pełni nienaruszone nanostruktury. Do tej pory nie istniał praktyczny sposób, by w żywych zwierzętach stwierdzić, czy pierwotne kształty origami DNA nadal są całe.
Molekularny „test integralności” dla origami DNA
Zespół opracował metodę nazwaną PLASTIQ, skrót od proximity ligation assay for structural tracking and integrity quantification. Kluczowy pomysł polega na tym, by samo origami DNA raportowało o swoim stanie. W określonych pozycjach każdej struktury badacze umieszczają pary krótkich „zszywek” DNA, które stykają się bokami wzdłuż helisy, gdy origami jest prawidłowo złożone. Jedna z każdej pary niesie małą chemiczną etykietę umożliwiającą enzymatyczne połączenie, czyli ligację, ale tylko jeśli nadal są trzymane blisko siebie przez nienaruszony włókno-szkielet. Jeśli struktura się topi, pęka lub zostaje rozkładana przez enzymy, te dwa fragmenty oddalają się i nie mogą być już ligowane. Po ligacji połączone pary są wzmacniane za pomocą standardowej reakcji łańcuchowej polimerazy i ilościowane przez czułe qPCR lub sekwencjonowanie, zamieniając obecność nienaruszonych lokalnych segmentów w mierzalne sygnały z zaledwie kilku mikrolitrów krwi.
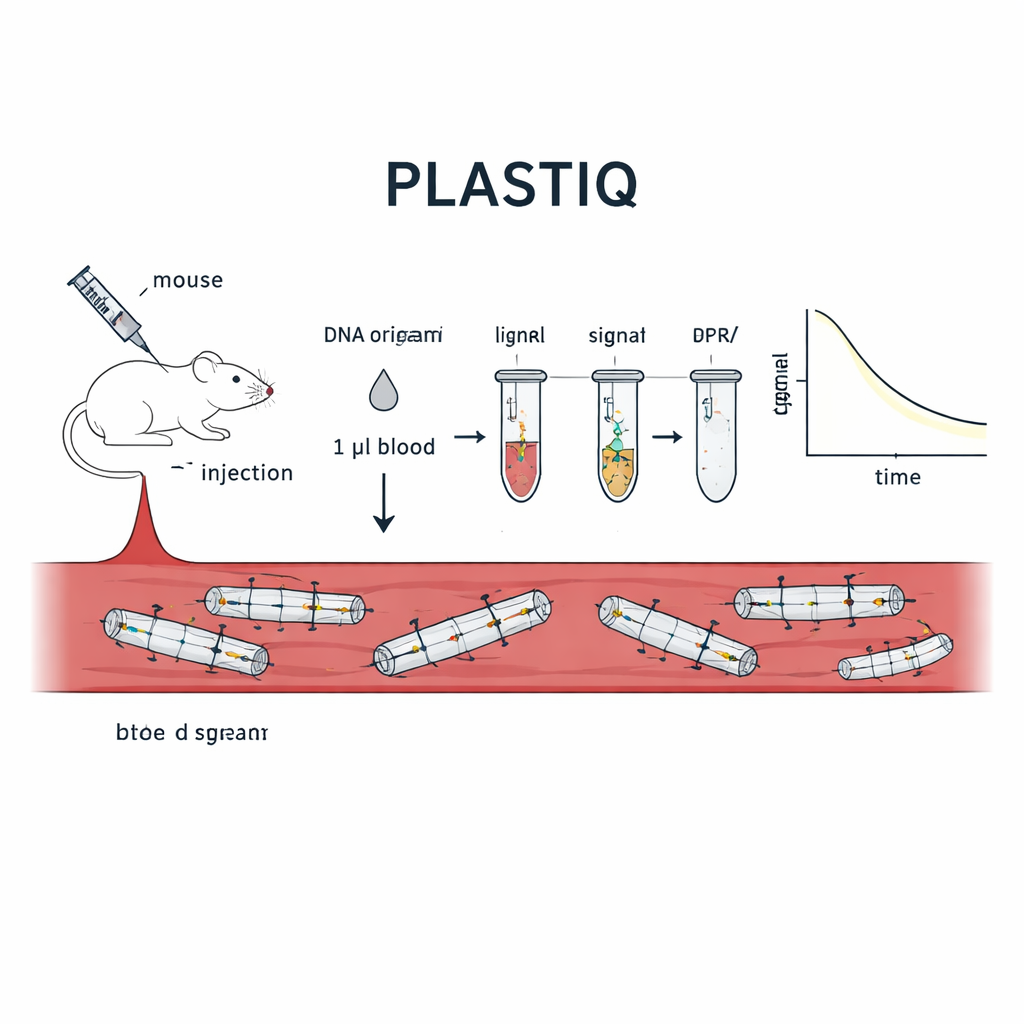
Wdrożenie testu u żywych myszy
Aby udowodnić, że PLASTIQ rzeczywiście mierzy integralność strukturalną, autorzy najpierw zastosowali go do prostych prętowych projektów origami DNA w probówkach. Sygnały pojawiały się tylko wtedy, gdy pręty były nienaruszone i zanikały po wywołanym cieple rozłożeniu, podczas gdy bardziej tradycyjne testy oparte na DNA nadal rejestrowały materiał DNA niezależnie od kształtu. Następnie wstrzyknięto te pręty myszy różnymi drogami — bezpośrednio do krwiobiegu, do jamy brzusznej, do mięśnia i pod skórę — i pobierano zaledwie jeden mikrolitr krwi w różnych momentach. PLASTIQ ujawnił, jak stężenie nienaruszonych struktur najpierw wzrastało, a potem spadało, w zależności od drogi podania, pasując do ogólnych oczekiwań z farmakologii leków, ale z dużo drobiazgowymi informacjami strukturalnymi. Metoda była czuła nawet do 0,01 femtomolara, a jednocześnie wymagała minimalnej ilości krwi, co pozwalało na wielokrotne pobieranie prób od tego samego zwierzęcia przez godziny.
Testowanie ochronnych powłok i ukrytych słabych punktów
Wiele grup próbuje chronić origami DNA, pokrywając je polimerami takimi jak PEG, sieciując nici światłem ultrafioletowym lub dodając związki chemiczne, ale trudno było ocenić, ile te zabiegi rzeczywiście pomagają in vivo. Korzystając z PLASTIQ, autorzy pokazali, że pręty pokryte PEG we krwi utrzymują integralność nieco dłużej niż nieosłonięte, ale też są szybciej usuwane po dostaniu się do krążenia, a powłoka nie przeszkadza enzymom PLASTIQ w wykonywaniu ich zadania. Łącząc PLASTIQ z prostymi modelami matematycznymi, wyekstrahowali szybkości wchłaniania i eliminacji dla różnych dróg podania i powłok, a nawet mogli symulować schematy wielokrotnego dawkowania. Następnie rozwinęli metodę dalej, stosując origami w kształcie beczki z podwójną warstwą, gęściej upakowaną wewnątrz niż na zewnątrz. Pomiary PLASTIQ pokazały, że zszywki na odsłoniętej zewnętrznej powierzchni traciły integralność szybciej niż te skierowane do wnętrza komory, co bezpośrednio potwierdza, że ukryte helisy są osłonięte przed enzymami degradującymi we krwi.
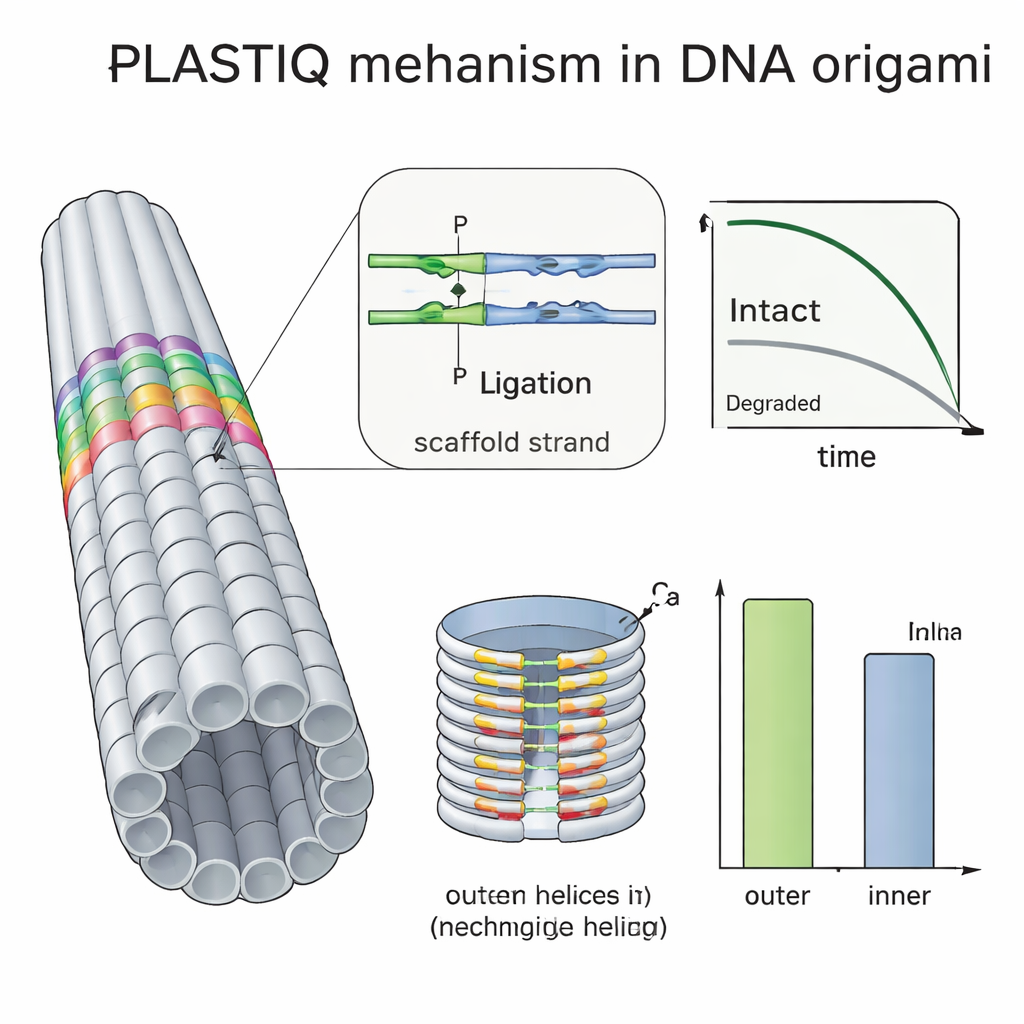
Co to oznacza dla przyszłych terapii opartych na DNA
Dla osoby nietechnicznej PLASTIQ można uznać za kontrolę stanu strukturalnego nanourządzeń DNA podróżujących po organizmie. Zamiast pytać jedynie „czy tu jest DNA?”, pyta „czy to DNA nadal jest złożone w precyzyjny obiekt, który zaprojektowaliśmy?”. Odpowiadając na to pytanie z wysoką czułością z niewielkich prób krwi, PLASTIQ daje deweloperom leków sposób na optymalizację projektu, powłoki i dawkowania leków i szczepionek opartych na origami DNA. Z czasem takie szczegółowe, ilościowe informacje o zachowaniu tych nanostruktur w rzeczywistych środowiskach biologicznych mogą pomóc przekształcić origami DNA z eleganckiej koncepcji laboratoryjnej w solidne, gotowe do oceny przez regulatorów terapie.
Cytowanie: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Słowa kluczowe: origami DNA, nanomedycyna, dostarczenie leku, farmakokinetyka, nanotechnologia