Clear Sky Science · pl
szczepienie mRNA przezwycięża upośledzenie wywołane przez hemozoin w przypadku szczepionek przeciwmalarycznych opartych na całych pasożytach u myszy
Dlaczego przebyta malaria osłabia działanie szczepionek
Malaria zabija setki tysięcy osób rocznie, a jedną z najbardziej obiecujących strategii jest użycie całych, osłabionych pasożytów do wytrenowania układu odpornościowego. Ciekawie jednak ta „złota norma” działa znacznie lepiej u osób, które nigdy wcześniej nie miały malarii, niż u tych wychowanych w regionach, gdzie choroba jest powszechna. Badanie przeprowadzone na myszach stawia proste, ale kluczowe pytanie: co w przebytej infekcji malarycznej sprawia, że wysoce skuteczna szczepionka nagle zawodzi — i czy nowy rodzaj szczepionki mRNA może rozwiązać ten problem?
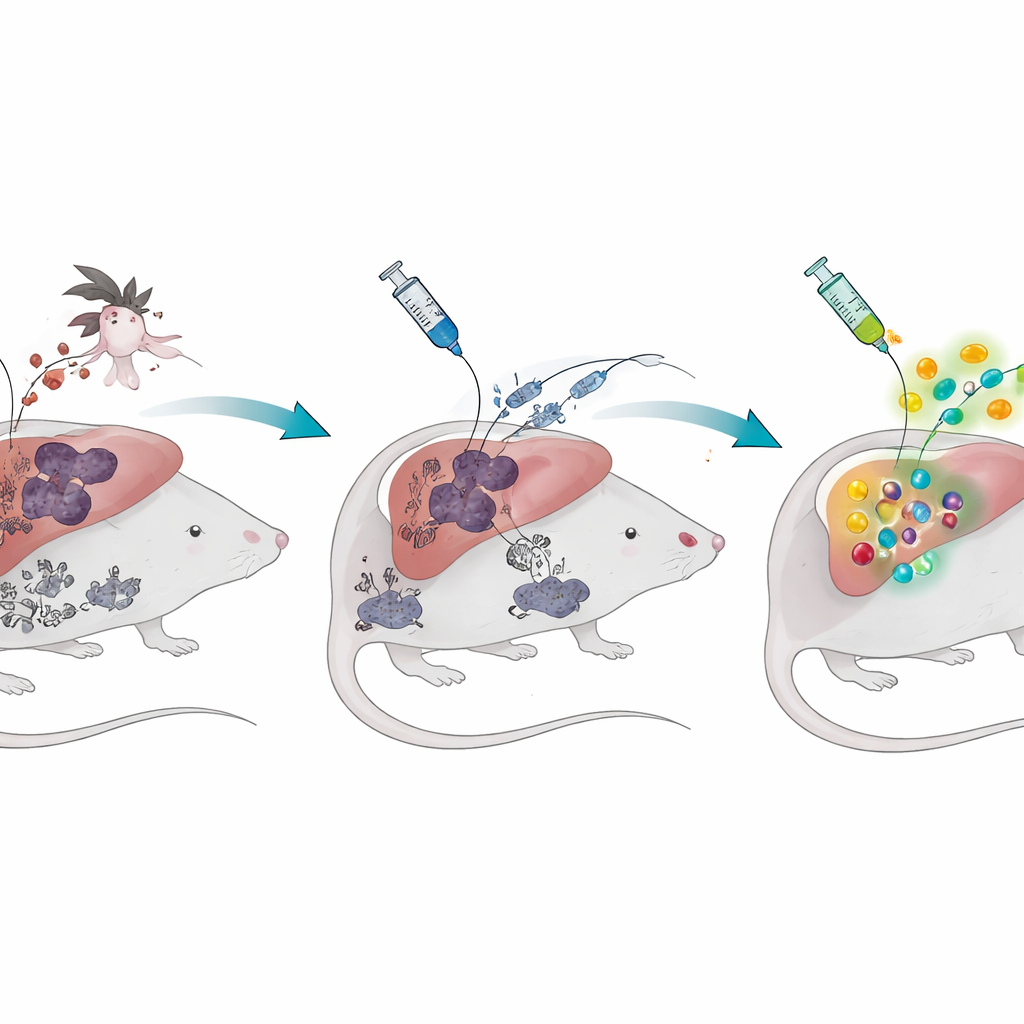
Opowieść o dwóch etapach malarii
Pasożyt malarii ma w organizmie człowieka dwa główne etapy. Najpierw, po ukąszeniu przez komara, cicho zakaża wątrobę. Później wnika do czerwonych krwinek, wywołując gorączkę i chorobę. Szczepionki oparte na całych pasożytach, zwane promieniowo osłabionymi sporozoitami, celują w cichy etap wątrobowy: pasożyty wnikają do komórek wątroby, ale nie kończą cyklu życiowego, dając układowi odpornościowemu bezpieczny podgląd. U myszy bez wcześniejszego kontaktu z malarią ta strategia tworzy dużą liczbę wyspecjalizowanych komórek T zabójców, które osiedlają się w wątrobie i potrafią zniszczyć pasożyty, zanim wywołają chorobę. Jednak gdy badacze najpierw zakażali myszy krwinkowym etapem malarii i pozwalali infekcji się oczyścić, ta sama szczepionka wytwarzała znacznie mniej ochronnych komórek T, a zwierzęta były dużo mniej chronione przy ekspozycji na żywe pasożyty.
Trwały pigment, który nie znika
Zespół zapytał następnie, co różni te „doświadczone malarią” myszy. Jeden wyraźny podejrzany to hemozoin, ciemny, krystaliczny pigment, który pasożyt wytwarza w czerwonych krwinkach, aby odtruć żelazne odpady powstające przy trawieniu hemoglobiny. Ten pigment nie znika po ustąpieniu infekcji; może zalegać w wątrobie, śledzionie i szpiku kostnym przez wiele miesięcy. Naukowcy stwierdzili, że nawet ponad rok po zakończeniu infekcji krwinkowej myszy wciąż miały zmagazynowany hemozoin i osłabioną odpowiedź komórek T na szczepionkę przeciwko etapowi wątrobowemu. Podanie zdrowym myszom oczyszczonego syntetycznego hemozoinu — bez żywych pasożytów — wystarczyło, by naśladować tę długotrwałą słabość szczepionki i zmniejszyć ochronę przed późniejszym wyzwaniem malarią.
Jak hemozoin sabotuje strażników odporności
Zagłębiając się bardziej, badacze skupili się na komórkach dendrytycznych, strażnikach układu odpornościowego, które pobierają fragmenty patogenów i prezentują je komórkom T. Aby szczepionka oparta na całych pasożytach przeciwko etapowi wątrobowemu zadziałała, komórki dendrytyczne muszą wychwycić materiał pasożyta pochodzący z zakażonych komórek wątroby i pokazać go komórkom T zabójcom. W eksperymentach hodowlanych zespół wykazał, że hemozoin bezpośrednio zakłóca ten etap pobierania: im większa ekspozycja komórek dendrytycznych na hemozoin, tym mniej efektywnie połykały one białkowe antygeny. Defekt występował zarówno w komórkach mysich, jak i w ludzkich komórkach odpornościowych uzyskanych od dawców krwi i nie zależał od jednego dobrze znanego sensora zapalnego, co sugeruje, że sam hemozoin działa jako fizyczna lub biochemiczna przeszkoda w normalnym przetwarzaniu antygenów.
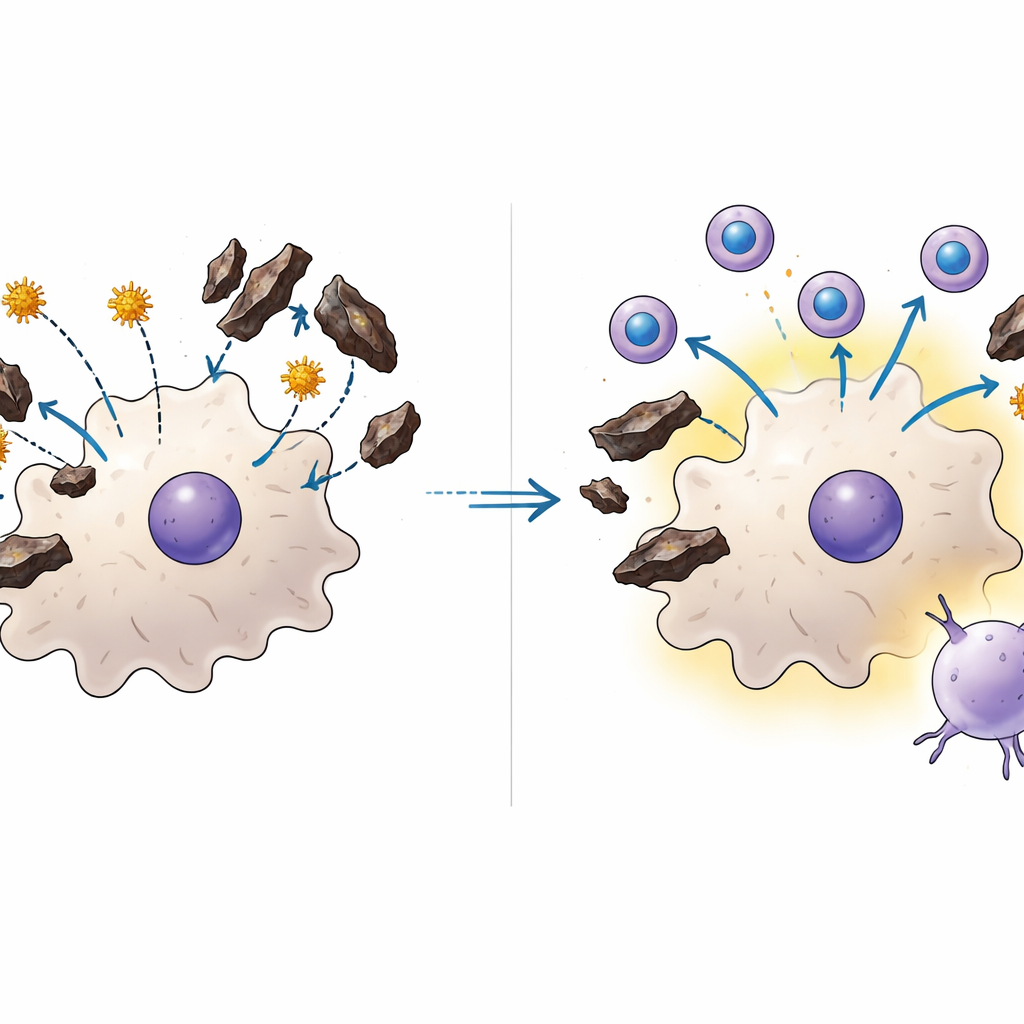
Szczepionki mRNA omijają tę przeszkodę
Aby sprawdzić, czy inny format szczepionki może uniknąć tego problemu, naukowcy zaprojektowali szczepionkę mRNA zapakowaną w lipidowe nanocząstki. Zamiast dostarczać białka pasożyta z zewnątrz, podejście to daje komórkom gospodarza instrukcje genetyczne do wytwarzania krótkich fragmentów kilku białek pasożyta wewnątrz komórki. U myszy z wcześniejszą malarią i bez niej szczepionka mRNA wygenerowała podobnie silne odpowiedzi komórek T zabójców i poprawiła kontrolę zakażenia wątrobowego. Co uderzające, gdy szczepionkę mRNA podano w połączeniu z jedną dawką szczepionki na bazie całych pasożytów, myszy zbudowały szczególnie duże pulę komórek T, które zająły długoterminowe miejsce w wątrobie — populację komórek znaną z szybkiego zapewniania ochrony. W warunkach hodowlanych hemozoin nie blokował ani pobierania, ani funkcji nanocząstek załadowanych mRNA, co tłumaczy, jak ta strategia może się udać tam, gdzie starsza szczepionka sama zawodzi.
Co to oznacza dla przyszłych szczepień przeciwmalarycznych
W praktycznym ujęciu badanie pokazuje, że przebyte infekcje malaryczne pozostawiają mikroskopijne, mineralne resztki, które zapychają sposób, w jaki niektóre komórki odpornościowe uczą się od szczepionek, osłabiając wiodącą szczepionkę opartą na całych pasożytach. Ale przez przejście na szczepionkę mRNA lub łączenie jej z nią — która podsuwa instrukcje dotyczące fragmentów pasożyta bezpośrednio do komórek — naukowcy mogą ominąć te resztki i przywrócić silną ochronę u gospodarzy doświadczonych malarią — przynajmniej u myszy. Praca wskazuje na hemozoin jako istotną przeszkodę dla szczepionek u osób żyjących w regionach endemicznych i sugeruje, że starannie zaprojektowane schematy szczepień mRNA lub mieszane mogą być obiecującą drogą do bardziej skutecznej, szeroko użytecznej immunizacji przeciwmalarycznej.
Cytowanie: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Słowa kluczowe: szczepionki przeciwmalaryczne, hemozoin, szczepionka mRNA, odporność komórek T, infekcja Plasmodium