Clear Sky Science · pl
Początkowe miejsca nawrotu SIV po przerwaniu terapii antyretrowirusowej u makaków rezus
Dlaczego wirus wraca
Współczesne leki przeciw HIV potrafią zepchnąć ilość wirusa we krwi do poziomów tak niskich, że standardowe testy nic nie wykrywają. Jednak po zaprzestaniu leczenia wirus niemal zawsze powraca. Badanie przeprowadzone na makakach rezus zakażonych bliskim krewnym HIV — wirusem SIV — stawia podstawowe, lecz kluczowe pytanie: gdzie dokładnie w ciele pojawia się pierwsza iskra tego nawrotu i jakie tkanki rozdmuchują ją w większy ogień?
Śledzenie barkodów wirusa
Aby śledzić wirusa z niezwykłą precyzją, badacze użyli specjalnego SIV, w którym każda cząstka wirusa nosi unikalny genetyczny „kod kreskowy” — krótką, niegroźną sekwencję działającą jak numer seryjny. Dwudziestu czterech makakom podano mieszaninę tysięcy takich wirusów z kodami kreskowymi, po czym szybko rozpoczęto intensywną, trójlekową terapię antyretrowirusową. Leki zmniejszyły poziom wirusa we krwi do praktycznie niewykrywalnego i utrzymywały go przez ponad rok, naśladując skuteczne długoterminowe leczenie HIV u ludzi. Ponieważ każdy kod kreskowy oznaczał odrębną linię wirusową, zespół mógł później ustalić, które konkretne linie wirusowe „obudziły się” po zaprzestaniu leczenia i w jakich miejscach ciała to przebudzenie miało początek.
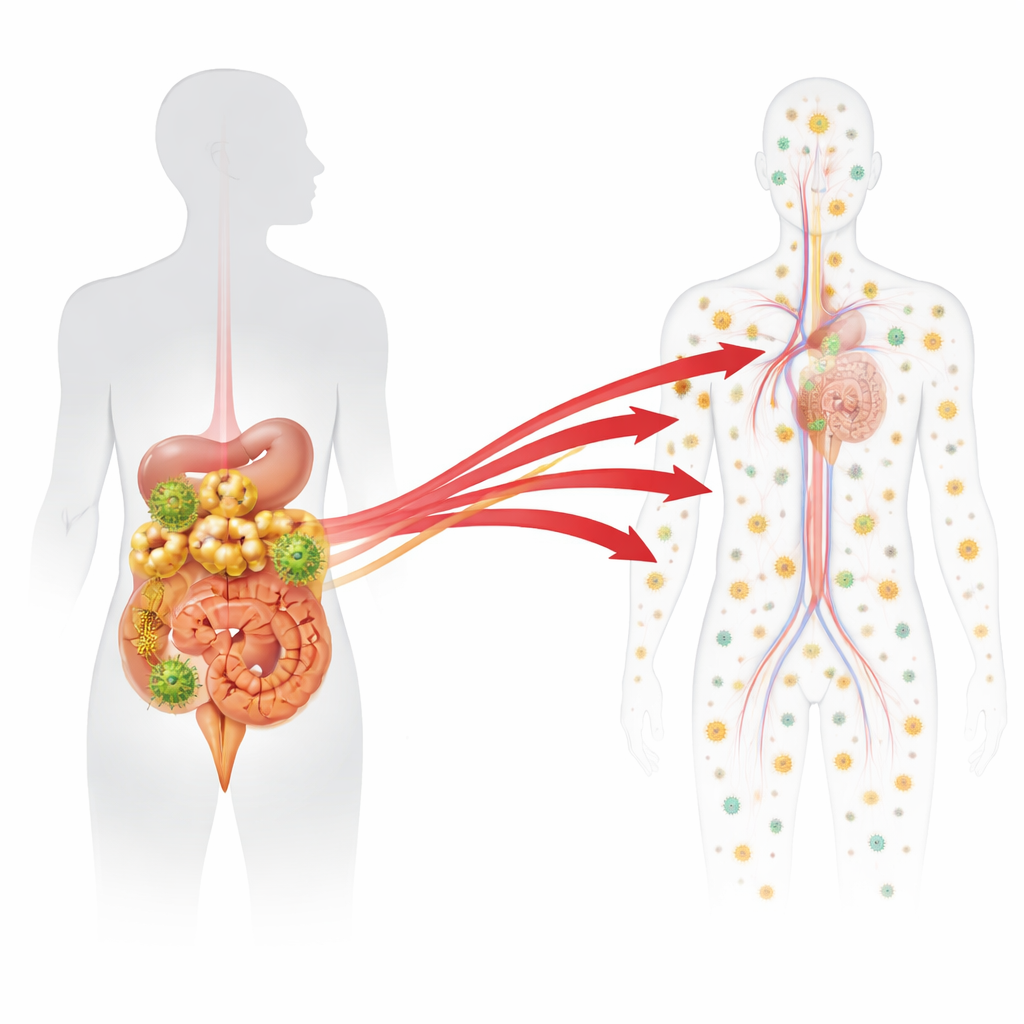
Wgląd w tkanki w trakcie i po terapii
Na koniec długiego okresu leczenia makaki podzielono na grupy. Część badano wciąż podczas terapii, aby określić normalny wzorzec niskiego tła materiału genetycznego wirusa, który utrzymuje się mimo leków. Innym przerwano leczenie i badano je po pięciu lub siedmiu dniach — przed lub w chwili, gdy wirus zaczynał pojawiać się ponownie we krwi. Od każdego zwierzęcia pobrano i przeanalizowano około 90 próbek tkanek z obejmujących jelito, różne rodzaje węzłów chłonnych, narządów krwiotwórczych jak szpik kostny oraz narządów nieimmunologicznych, takich jak wątroba i płuca. Dla każdej tkanki mierzyli, ile wirusowego DNA (oznaka zakażonych komórek) i wirusowego RNA (oznaka aktywnej produkcji wirusa) występowało dla każdego kodu kreskowego. Następnie zastosowali modele statystyczne, aby wskazać każdy kod kreskowy, którego poziom RNA w danej tkance wzrósł znacznie powyżej tego, co można by oczekiwać od prostego, niskiego tła aktywności podczas terapii.
Wskazywanie pierwszych iskierek nawrotu
Te niezwykle aktywne kody kreskowe, które badacze nazwali „odstającymi”, wyróżniały linie wirusowe prawdopodobnie przeżywające świeże wybuchy replikacji i lokalnego rozprzestrzeniania po odstawieniu leków. W sumie u wszystkich zwierząt zidentyfikowano 32 takie odstające kody. Co ważne, gdy wirus ponownie pojawiał się we krwi, około połowa kodów znalezionych w osoczu odpowiadała tym odstającym w tkankach, co bezpośrednio łączy konkretne miejsca tkankowe z najwcześniejszym etapem ogólnoustrojowego nawrotu. Większość odstających kodów występowała tylko w jednej próbce tkankowej, co zgadza się z bardzo lokalnym punktem startowym, podczas gdy mniejsza część zdążyła już rozprzestrzenić się do sąsiednich fragmentów jelita i spływających z nich węzłów chłonnych. Tylko u jednego zwierzęcia z wyraźnie wyższymi poziomami wirusa we krwi zaobserwowano dowody na to, że wiele tkanek — w tym odległych — zostało już ponownie zasiedlonych. Sugeruje to etapowy postęp: najpierw ciche zapłonienie w jednym miejscu, potem miejscowa ekspansja, a następnie rozprzestrzenienie po całym ciele.
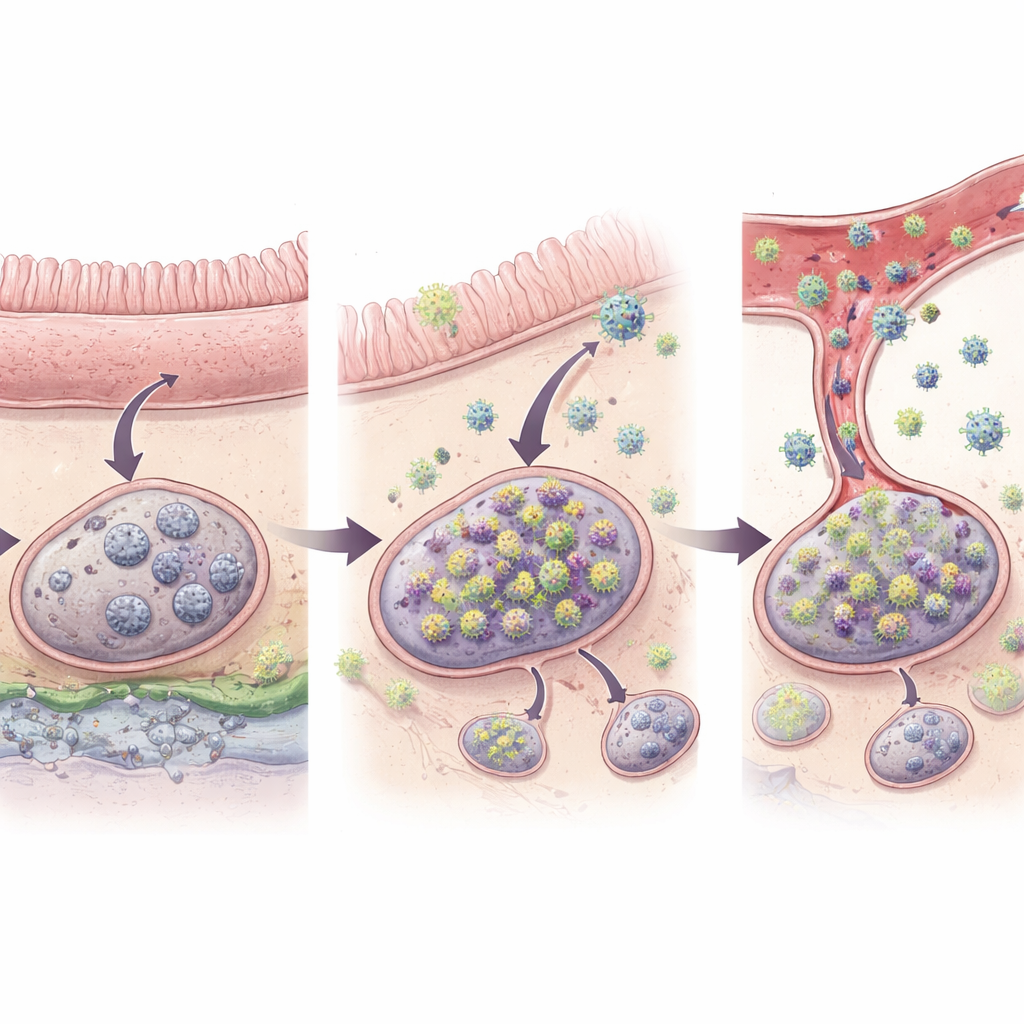
Dlaczego jelita mają największe znaczenie
Jedno spostrzeżenie było szczególnie wyraźne: niemal wszystkie wczesne zdarzenia nawrotu dało się prześledzić do przewodu pokarmowego i związanych z nim tkanek odpornościowych. Z 27 kodów uznanych za rzeczywiste początki nawrotu, 96% znajdowało się w samych jelitach lub w przy-jelitowych węzłach chłonnych, takich jak węzły krezkowe drenujące jelito cienkie i grube. Tylko jedno miejsce początkowe pojawiło się w węźle chłonnym niezwiązanym z jelitem, a żadne nie zidentyfikowano w narządach takich jak wątroba, płuca czy szpik kostny. Analizy statystyczne wykazały, że nawet po uwzględnieniu liczby zakażonych komórek, związane z jelitem tkanki limfoidalne były około dziesięciokrotnie bardziej prawdopodobne niż inne miejsca limfoidalne, by dać początek wirusowi nawrotowemu. Unikalne środowisko jelit — ciągła ekspozycja na pokarm i mikroby oraz częste stany zapalne przy zakażeniach podobnych do HIV — może utrzymywać zakażone komórki bardziej aktywne i łatwiejsze do ponownego pobudzenia do produkcji wirusa.
Co to oznacza dla przyszłych terapii
Krótko mówiąc, praca ta sugeruje, że po odstawieniu silnych leków podobnych do tych stosowanych przeciw HIV wirus niemal zawsze restartuje się z kilku ukrytych rezerwuarów w i wokół jelit, a nie równomiernie ze wszystkich zakątków ciała. Początkowo te wybuchy są bardzo małe i ograniczone do jednego fragmentu tkanki, ale gdy wirus dotrze do krwiobiegu i odległych narządów, poziomy szybko rosną. Dla wysiłków zmierzających do długotrwałej remisji lub wyleczenia oznacza to, że terapie muszą docierać i skutecznie działać w limfoidalnych tkankach jelit. Narzędzia pozwalające wizualizować lub pobierać próbki z tych trudno dostępnych miejsc u ludzi albo leki specjalnie ukierunkowane na działanie tam mogą okazać się kluczowe, by zapobiec zapłonowi pierwszych iskier nawrotu zanim zdążą się rozprzestrzenić.
Cytowanie: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Słowa kluczowe: Nawroty HIV, rezerwuar wirusa, tkanka limfoidalna jelit, model makaka rezus, przerwanie terapii antyretrowirusowej