Clear Sky Science · pl
Analiza porównawcza zbiorów danych z głębokiego skanowania mutacji w enterowirusach A i B ujawnia rozbieżności funkcjonalne i cele terapeutyczne
Dlaczego małe wirusy RNA mają dla nas znaczenie
Enterowirusy to duża grupa drobnych wirusów RNA, które krążą po całym świecie, zwykle wywołując łagodne przeziębienia lub dolegliwości żołądkowe, ale czasem prowadząc do porażeń, uszkodzeń serca czy innych ciężkich chorób. Mamy niewiele szczepionek i jeszcze mniej leków działających szeroko przeciwko nim, częściowo dlatego, że te wirusy ewoluują bardzo szybko. W tym badaniu zadano pozornie proste pytanie o dużych praktycznych konsekwencjach: gdy wirusy mutują, które części ich aparatu można zmieniać swobodnie, a które są tak istotne, że ewolucja niemal je „zamraża”? Odpowiedzi wskazują nowe strategie projektowania terapii, których wirus trudno będzie przechytrzyć.
Czytanie instrukcji wirusa, mutacja po mutacji
Naukowcy skupili się na dwóch ludzkich enterowirusach wywołujących bardzo różne choroby: enterowirusie A71, powiązanym z ciężkimi schorzeniami neurologicznymi u dzieci, oraz coxsackievirusie B3, związanym z zapaleniem serca, a nawet rakiem trzustki. Zastosowali technikę zwaną głębokim skanowaniem mutacji, tworząc biblioteki wirusowe, w których niemal każda pozycja w białkach wirusa została systematycznie zmieniona. Te zmutowane wirusy pozwolono infekować komórki w hodowli, a za pomocą sekwencjonowania wysokoprzepustowego mierzono, jak każda zmiana wpływa na wzrost wirusa. Porównując każdy mutant z pierwotnym wirusem, zespół zbudował szczegółową mapę miejsc w proteomie wirusa, które tolerują zmiany, oraz tych silnie ograniczonych. 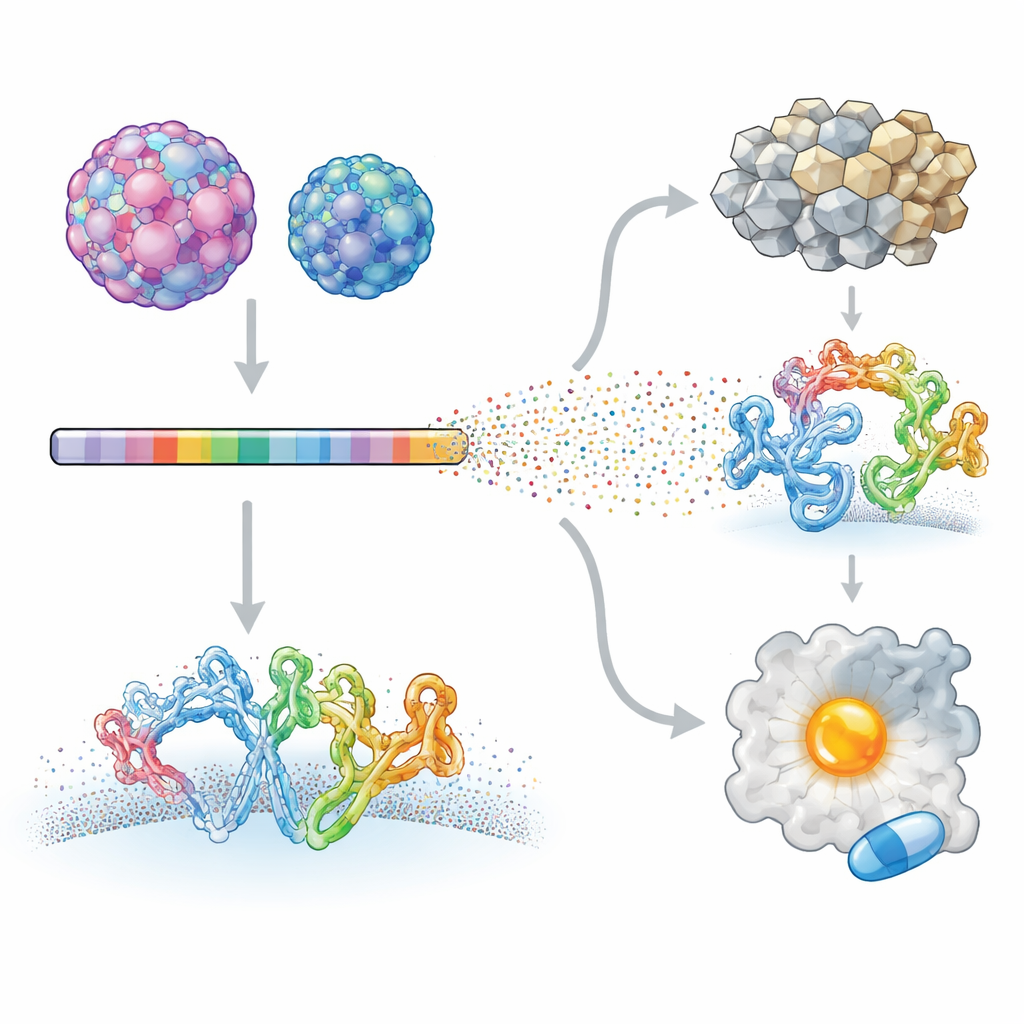
Wspólne twarde ograniczenia i specyficzna elastyczność wirusa
Mimo że oba wirusy dzielą ze sobą zaledwie około połowy sekwencji aminokwasowych, wykazały zadziwiająco podobne ogólne wzorce ograniczeń. Wewnętrzne enzymatyczne „konie pociągowe”, które kopiują genom, tną białka wirusowe i rozwijają RNA, były w obu wirusach wysoce wrażliwe na mutacje. Podobnie ukryte powierzchnie utrzymujące razem powłokę białkową, czyli kapsyd, okazywały się trudne do zmiany bez uszkodzenia wirusa. W przeciwieństwie do tego, wiele regionów zwróconych na zewnątrz i wchodzących w interakcje z gospodarzem było bardziej podatnych na zmiany i często różniło się wyraźnie między dwoma gatunkami. Analiza strukturalna wykazała, że zachowane, nietolerancyjne na mutacje obszary skupiają się wokół miejsc aktywnych i interfejsów montażowych, podczas gdy regiony stykające się z receptorami gospodarza, błonami czy cząsteczkami układu odpornościowego stanowią ogniska specyficznej dla gatunku elastyczności.
Jak wirusy wchodzą w komórki i unikają obrony
Zespół przyjrzał się następnie molekularnemu uściskowi dłoni między wirusem a gospodarzem. Enterowirus A71 i coxsackievirus B3 używają różnych receptorów komórkowych do wejścia, a badanie wykazało, że dokładne ślady kontaktu na powierzchni kapsydu są jednymi z najbardziej różniących się regionów pod względem tolerancji na mutacje. Reszty chwytające receptor dla jednego wirusa są silnie ograniczone w tym wirusie, ale stosunkowo dopuszczalne w drugim, co odzwierciedla, jak każdy z nich dopracował własną platformę dokującą. Podobne rozbieżności pojawiły się w małym białku związanym z błoną zwanym 3A, które pomaga przekształcać błony komórkowe i rekrutować czynniki gospodarza do replikacji genomu. Modelowanie sugerowało, że oba wirusy używają częściowo różnych łat kontaktowych na 3A do wiązania tego samego czynnika gospodarza, GBF1, i mogą też wprowadzać to białko w błony na różnych głębokościach. Te różnice pomagają wyjaśnić, dlaczego blisko spokrewnione wirusy mogą infekować różne tkanki i wywoływać odmienne wzorce chorób.
Czego ewolucja w laboratorium nie pokazuje — i co trafnie odzwierciedla
Aby umieścić eksperymenty w hodowlach komórkowych w kontekście rzeczywistym, autorzy porównali swoje mapy mutacji z tysiącami naturalnych sekwencji wirusa pochodzących z próbek pacjentów. Ogólnie miejsca elastyczne w laboratorium miały tendencję do bycia zmiennymi również w naturze, zwłaszcza w szerszych porównaniach na poziomie gatunkowym. Jednak gdy przyjrzeli się, które konkretne aminokwasy są preferowane w danym miejscu, ewolucja naturalna i selekcja laboratoryjna najściślej zgadzały się w obrębie pojedynczego typu wirusa. Największe rozbieżności skupiały się na zewnętrznej powierzchni kapsydu oraz na regionach wchodzących w interakcje z gospodarzem w białkach nieustrukturalnych 2A i 3A — dokładnie tam, gdzie odpowiedzi odpornościowe i złożone środowiska gospodarza mają największe znaczenie. To sugeruje, że głębokie skanowanie mutacji odzwierciedla podstawowe mechaniczne ograniczenia białek wirusowych, podczas gdy prawdziwe infekcje nakładają dodatkowe naciski ze strony odporności i tropizmu tkankowego, które trudniej wiernie odwzorować in vitro.
Odnalezienie wspólnego słabego punktu dla przyszłych leków
Na koniec badacze sprawdzili, czy te mapy mogą wskazać wspólną achillesową piętę dla rozwoju leków. Za pomocą narzędzi obliczeniowych przeszukali oba wirusy w poszukiwaniu kieszeni na powierzchniach białek, które potencjalnie mogłyby wiązać małe cząsteczki leków. Następnie nałożyli dane mutacyjne, by zobaczyć, które kieszenie składają się z reszt, których wirus nie może łatwo zmienić bez szkody dla siebie. Jedna kieszeń, zlokalizowana na helikazie 2C — pierścieniowym silniku pomagającym rozwijać RNA wirusa — wyróżniała się. Jej kształt i składowe reszty są wysoko zachowane w czterech głównych ludzkich gatunkach enterowirusów, leży z dala od już znanych miejsc aktywnych, a zmiany tam są rzadkie w naturze i silnie szkodliwe w testach laboratoryjnych. 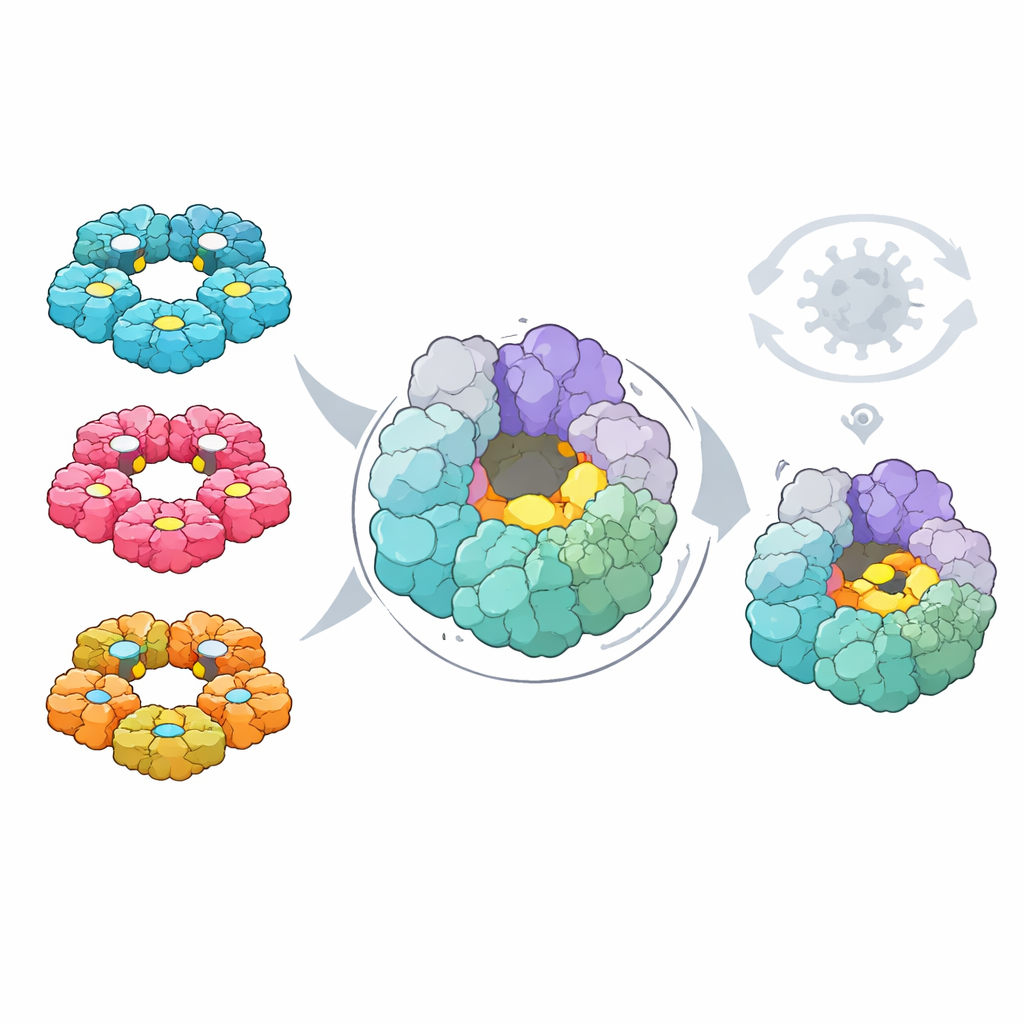
Co to oznacza dla przyszłych terapii
Systematycznie badając, jak każda możliwa pojedyncza zmiana literowa wpływa na dwa ważne enterowirusy, to badanie ujawnia wyraźny podział między wspólnym, sztywnym rdzeniem aparatu wirusowego a bardziej elastycznymi, specyficznymi dla wirusa interfejsami z gospodarzem. Zachowany rdzeń obejmuje nowo wyróżnioną kieszeń na helikazie 2C, która wydaje się trudna do zmodyfikowania przez wirusa bez utraty sprawności, co czyni ją atrakcyjnym celem dla szerokopasmowych leków przeciwwirusowych z wysoką barierą dla powstania oporności. Równocześnie bardziej podatne powierzchnie zewnętrzne i miejsca kontaktu z gospodarzem wyjaśniają, dlaczego spokrewnione wirusy zachowują się tak różnie w organizmie i wskazują, gdzie szczepionki oraz terapie oparte na układzie odpornościowym będą musiały mierzyć się z szybką ewolucją. Razem te wnioski dostarczają mapy drogowej do projektowania terapii, które wykorzystują ewolucyjne ograniczenia samego wirusa.
Cytowanie: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Słowa kluczowe: enterowirusy, ewolucja wirusów, głębokie skanowanie mutacji, cele przeciwwirusowe, helikaza 2C