Clear Sky Science · pl
Naturalne szlaki H2 umożliwiają biokompatybilną hydrogenację metabolitowych alkenów w bakteriach
Przekształcenie mikrobów w maleńkie ekologiczne fabryki
Wyobraź sobie, że zwykłe bakterie jelitowe mogłyby pomóc zastąpić paliwa kopalne przy produkcji codziennych chemikaliów — od konserwantów spożywczych po tworzywa — a przy tym oczyszczać odpady żywnościowe. Badanie pokazuje, że powszechne laboratoryjne szczepy Escherichia coli potrafią to zrobić: naturalnie wytwarzają wodór wewnątrz komórek, a ten wodór może być wykorzystywany na powierzchni komórki do napędzania przemysłowych reakcji chemicznych w łagodnych, wodnych warunkach. Łącząc żywe mikroby z metalowym katalizatorem stałym, autorzy wyznaczają drogę do czystszej, oszczędzającej węgiel produkcji.
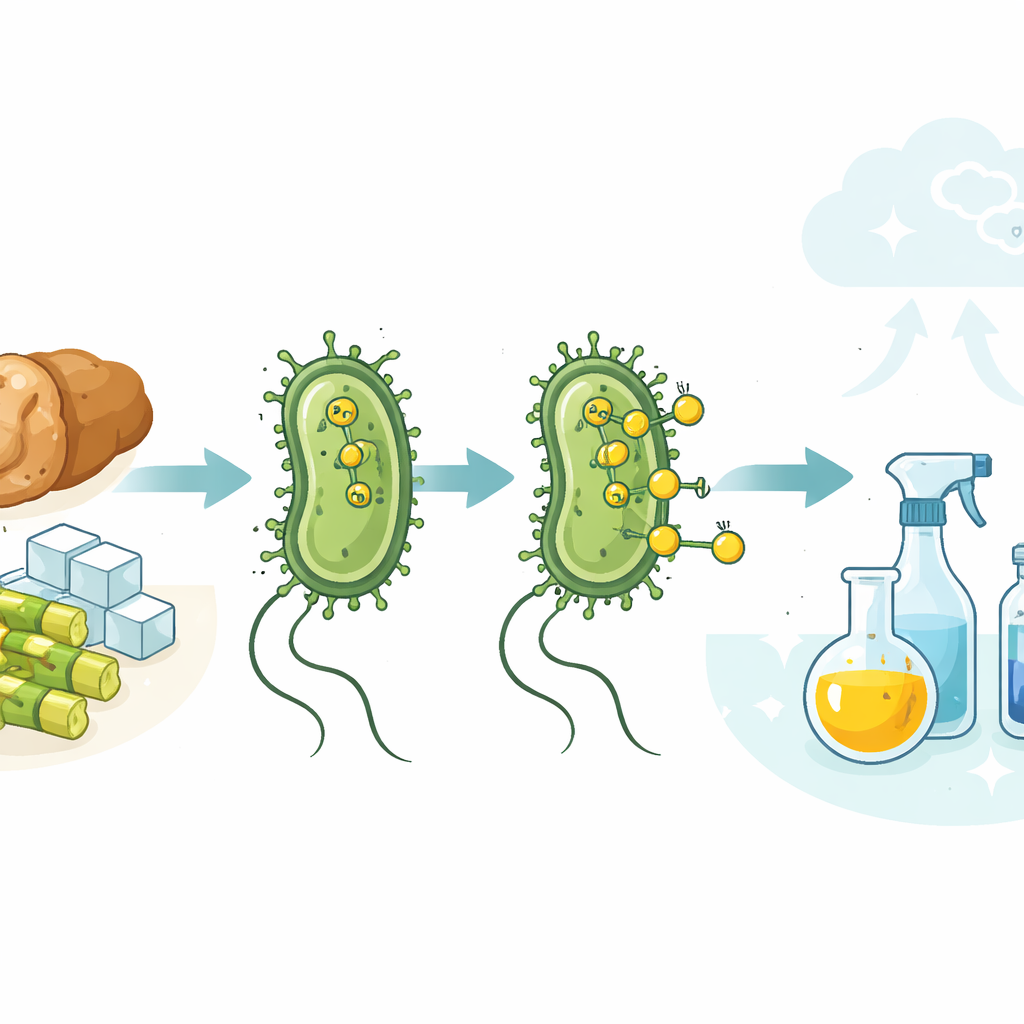
Dlaczego wodór ma znaczenie dla produktów codziennego użytku
Gazowy wodór jest centralnym surowcem współczesnej chemii. Służy do zamieniania ciekłych olejów w smarowidła, ulepszania paliw surowcowych oraz do wytwarzania wielu składników leków i tworzyw sztucznych. Obecnie prawie cały ten wodór pochodzi z paliw kopalnych, głównie gazu ziemnego i węgla, co wiąże się z dużymi emisjami dwutlenku węgla. Jednocześnie wiele mikroorganizmów naturalnie uwalnia wodór, rozkładając cukry w warunkach niedoboru tlenu. Zagadką, którą autorzy rozwiązują, jest to, jak wykorzystać ten łagodny, biologiczny strumień wodoru do napędzania tych samych reakcji, które przemysł obecnie przeprowadza pod wysokim ciśnieniem, w rozpuszczalnikach organicznych i przy użyciu gazu pochodzącego z paliw kopalnych.
Pozwalanie bakteriom zasilać metalowy katalizator
Zespół skupił się na prostych reakcjach addycji wodoru, gdzie podwójne wiązanie w cząsteczce jest „nasycane” wodorem. Hodowali kilka niemodyfikowanych szczepów E. coli w pożywkach na bazie cukru, a następnie dodali drobno rozproszony katalizator palladowy kompatybilny z żywymi komórkami. W warunkach beztlenowych rodzimy metabolizm bakterii przekształcał cukier w formian, a następnie w gazowy wodór przy wewnętrznej powierzchni błony komórkowej. Mikroskopia ujawniła, że naładowane dodatnio cząstki katalizatora osiadają na naładowanej ujemnie powierzchni komórki, gdzie spotykają uwalniany wodór. Tam metal wykorzystuje mikrobiologiczny wodór do redukcji testowej cząsteczki, kwasu kawowego, do jej nasyconego produktu przy bardzo wysokich wydajnościach — często lepszych niż uzyskane przy uprzednio silnie zmodyfikowanym szczepie.
Poszerzanie wachlarza produktów i surowców
Gdy podstawowa reakcja zadziałała, badacze przetestowali szeroką gamę związków zawierających podwójne wiązania węgiel–węgiel, w tym kwasy pochodzenia roślinnego i długołańcuchowe związki tłuszczowe. Wiele z nich zostało płynnie przekształconych do form nasyconych, niektóre w niemal ilościowych wydajnościach. Zbudowali też szczepy E. coli produkujące dodatkowy wodór przez skierowanie większego strumienia metabolizmu do rodzimych szlaków tworzących wodór. Takie wzmocnione szczepy umożliwiły podobne konwersje przy użyciu mniejszej ilości katalizatora metalicznego. W zaskakującym zabiegu zespół zastąpił czysty cukier zupą z upłynnionego czerstwego chleba jako źródło pożywienia. Enzymy rozbiły czerstwy chleb na glukozę, którą bakterie fermentowały równie skutecznie, przekształcając powszechny odpad żywnościowy zarówno w biologiczny wodór, jak i w chemikalia o podwyższonej wartości.
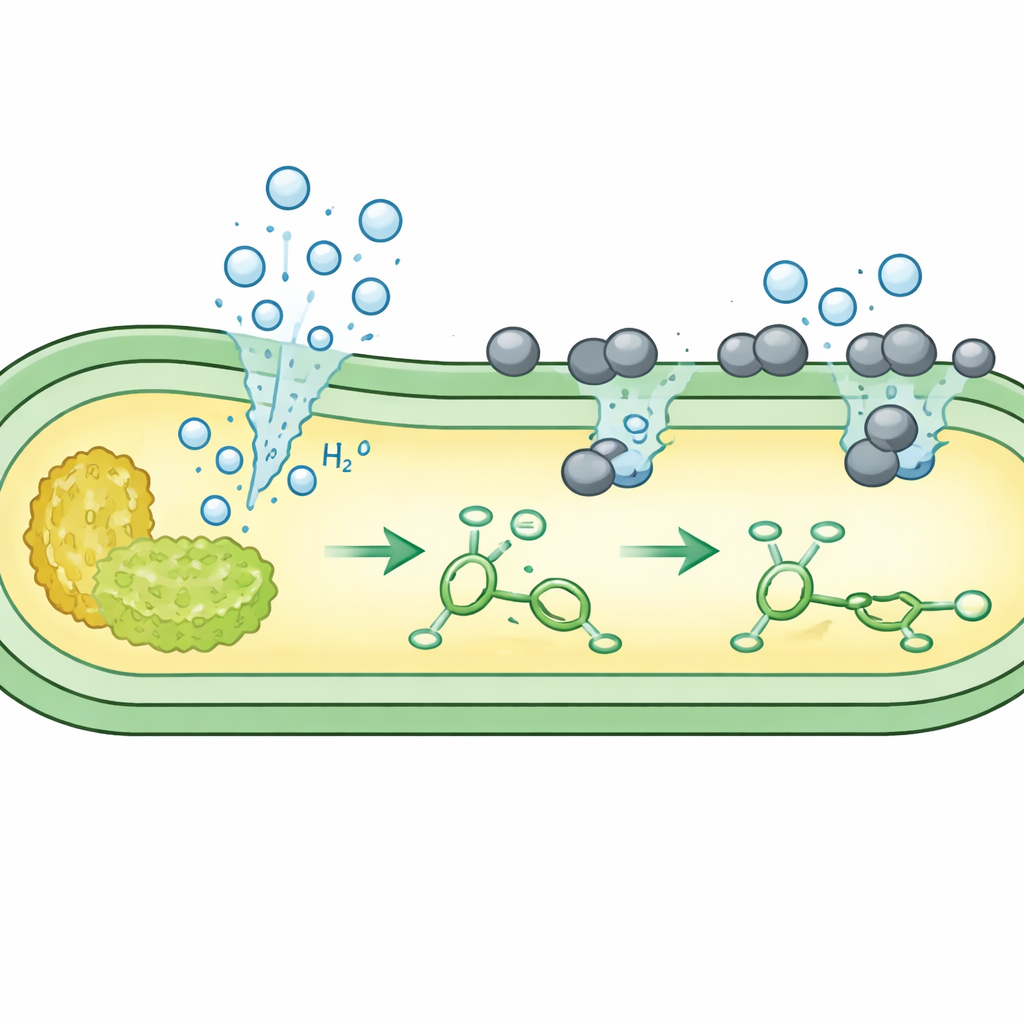
Wytwarzanie jednocześnie składnika i paliwa wewnątrz jednej komórki
Następnie autorzy zapytali, czy pojedyncza bakteria może wytwarzać nie tylko „odczynnik” w postaci wodoru, ale też nienasycony „substrat”, który ma zostać przekształcony. Zaprojektowali E. coli tak, żeby najpierw kierować przepływ cukru do szlaków produkujących aromatyczne cegiełki, takie jak kwas cynamonowy i coumarowy, oraz do oddzielnego szlaku generującego wodór. Gdy w kulturze zgromadziły się te wewnętrzne metabolity, dodano katalizator palladowy. Na powierzchni komórki katalizator wykorzystał wytworzony in situ wodór do konwersji nowo utworzonych metabolitów z podwójnymi wiązaniami w pełni do produktów nasyconych, takich jak kwas hydrocynamonowy, desaminotyrozyna i kwas adipinowy — kluczowy prekursor do nylonu. W niektórych wariantach taka kometabolizm osiągnął niemal całkowitą konwersję, wszystko w tej samej żywej kulturze.
Pomiary korzyści klimatycznych
Aby sprawdzić, czy ta pomysłowa biochemia rzeczywiście pomaga planecie, zespół przeprowadził ocenę cyklu życia porównując swoje hybrydowe podejście „chemo‑mikrobowe” ze standardowymi drogami hydrogenacji napędzanymi wodorem z paliw kopalnych lub wodorem elektrolitycznym. Gdy biologiczny wodór i produkcja substratów w komórce zostały połączone w jednym, energooszczędnym procesie, całkowite emisje gazów cieplarnianych znacznie zmalały. Wykorzystanie czerstwego chleba jako surowca dodatkowo poprawiło wynik: unikając składowania lub spalania i przekształcając wyrzuconą żywność w chemikalia, niektóre scenariusze stały się w sumie ujemne pod względem emisji węgla — oznacza to, że usuwają więcej gazów cieplarnianych, niż emitują.
Znaczenie dla przyszłej produkcji
Mówiąc prosto, badanie pokazuje, że codzienne bakterie można skłonić, by działały zarówno jako źródło energii, jak i fabryka składników dla ważnych reakcji chemicznych, podczas gdy stały metal na ich powierzchni dyskretnie dopracowuje końcowy etap. Ponieważ wszystko dzieje się w wodzie, w temperaturze zbliżonej do temperatury ciała i z użyciem odnawialnych lub odpadowych cukrów, podejście to może pewnego dnia zaoferować czystsze alternatywy dla tradycyjnych zakładów petrochemicznych. Przy dalszym inżynierskim dopracowaniu szlaków mikrobiologicznych i katalizatorów ta platforma żywych komórek może umożliwić nową generację zrównoważonych procesów, które zamieniają odnawialny węgiel i wyrzuconą żywność w użyteczne produkty o znacznie mniejszym śladzie klimatycznym.
Cytowanie: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Słowa kluczowe: mikrobowy wodór, zielona chemia, biokataliza, odpady-na-chemikalia, zrównoważona produkcja