Clear Sky Science · pl
Monowalentne pseudo-naturalne produkty potęgują degradację IDO1 przez jego rodzimy E3 KLHDC3
Wyłączanie enzymu sprzyjającego nowotworom
Nasz układ odpornościowy nieustannie patroluje w poszukiwaniu komórek nowotworowych, lecz guzy często odpowiadają przejmowaniem chemii organizmu. Kluczowym graczem w tej rozgrywce jest enzym zwany IDO1, który pomaga nowotworom unieszkodliwiać komórki odpornościowe. W pracy opisano nową klasę małocząsteczkowych związków, które robią więcej niż tylko blokować aktywność IDO1 — przekonują komórki, by pozbyły się tego enzymu całkowicie. Wykorzystując naturalne mechanizmy usuwania odpadów komórkowych, związki te mogą na nowo przywrócić ataki odporności na guzy w sposób niedostępny dla starszych leków.
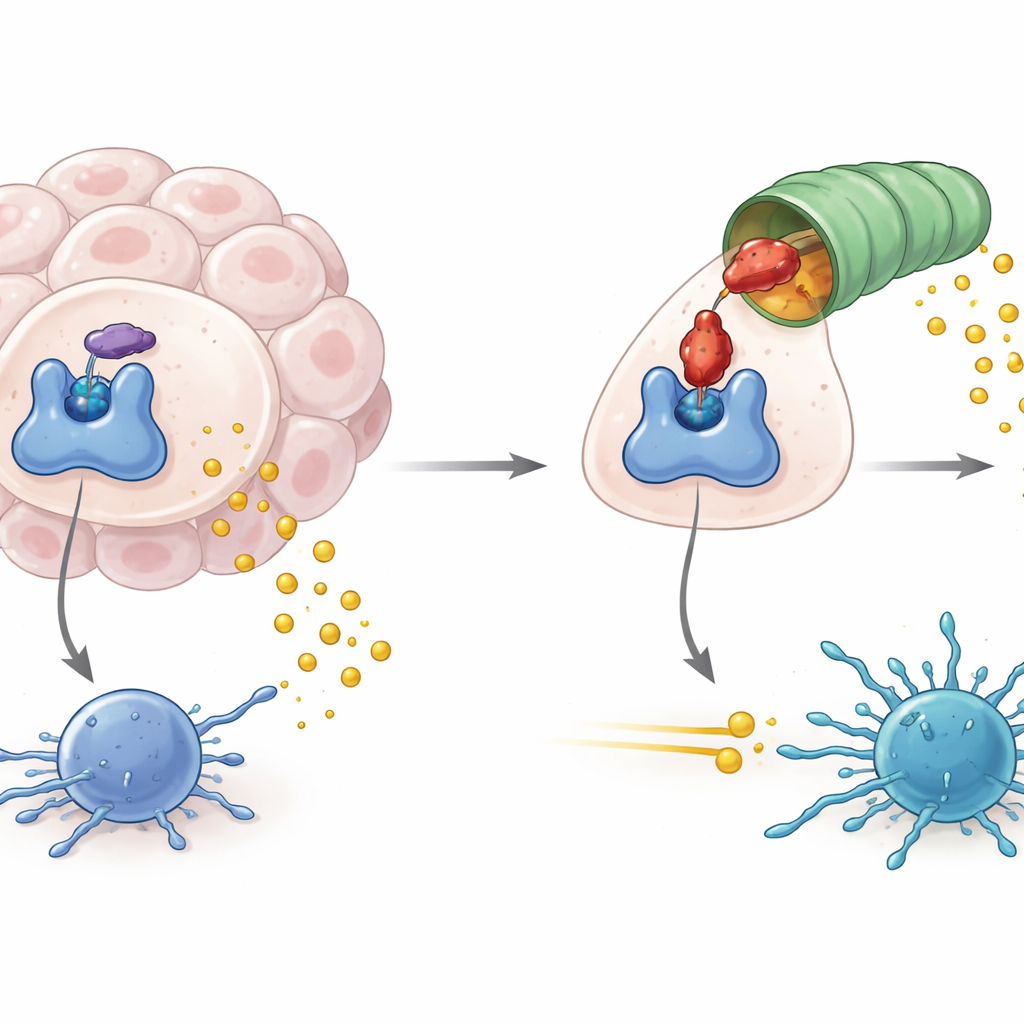
Jak guzy wykorzystują metabolicznego strażnika
IDO1 znajduje się na wejściu ścieżki metabolicznej rozkładającej aminokwas tryptofan do produktu nazwanego kinureniną. Gdy IDO1 jest liczny i aktywny, poziom tryptofanu spada, a kinurenina rośnie, co tworzy środowisko chemiczne tłumiące aktywność komórek odpornościowych, w tym walczących z rakiem limfocytów T. Wysoka aktywność IDO1 wiąże się nie tylko ze słabszą odpowiedzią anty‑nowotworową, lecz także z nowotworami wywoływanymi przez wirusy i niektórymi formami neurodegeneracji. Dlatego twórcy leków koncentrowali się na blokowaniu aktywności enzymatycznej IDO1, mając nadzieję przerwać ten immunosupresyjny sygnał i poprawić skuteczność istniejących immunoterapii przeciwnowotworowych.
Dlaczego proste blokery enzymów zawiodły
Mimo obiecujących wyników w badaniach na zwierzętach, badania kliniczne tradycyjnych inhibitorów IDO1 okazały się rozczarowujące. Pojawia się wyjaśnienie, że IDO1 jest czymś więcej niż prostym katalizatorem. Nawet jeśli jego aktywność chemiczna zostanie zablokowana, sam białkowy nośnik może działać jako centrum sygnalizacyjne, które nadal sprzyja wzrostowi i rozprzestrzenianiu się guza. Niektóre inhibitory wręcz stabilizują IDO1, zwiększając ilość białka w komórkach. Innymi słowy, wyłączenie tylko funkcji katalitycznej może pozostawić nietkane jej pro‑nowotworowe, nieenzymatyczne role — albo, co gorsza, je wzmocnić.
Projektowanie związków wywołujących samozniszczenie
Autorzy przeszukali dużą bibliotekę „pseudo‑naturalnych” cząsteczek — zsyntetyzowanych związków zbudowanych z fragmentów inspirowanych produktami naturalnymi, lecz połączonych na nowe sposoby. Odkryli rodzinę związków nazwanych iDeg, wywodzących się z roślinopodobnego składnika (−)-myrtanol. Związki te wiążą się w zwykłej kieszeni IDO1 przeznaczonej dla jego zawierającego żelazo kofaktora, hemu. Wypierając hem, iDegy osłabiają zdolność IDO1 do wytwarzania kinureniny i, co kluczowe, przekształcają część ogonowej domeny białka. Struktury krystaliczne o wysokiej rozdzielczości pokazują, że gdy iDegy zajmują miejsce hemu, rozluźniają i częściowo dewulgarizują helisę C‑terminalną, która normalnie jest utrzymywana w zwartej, chronionej konformacji.
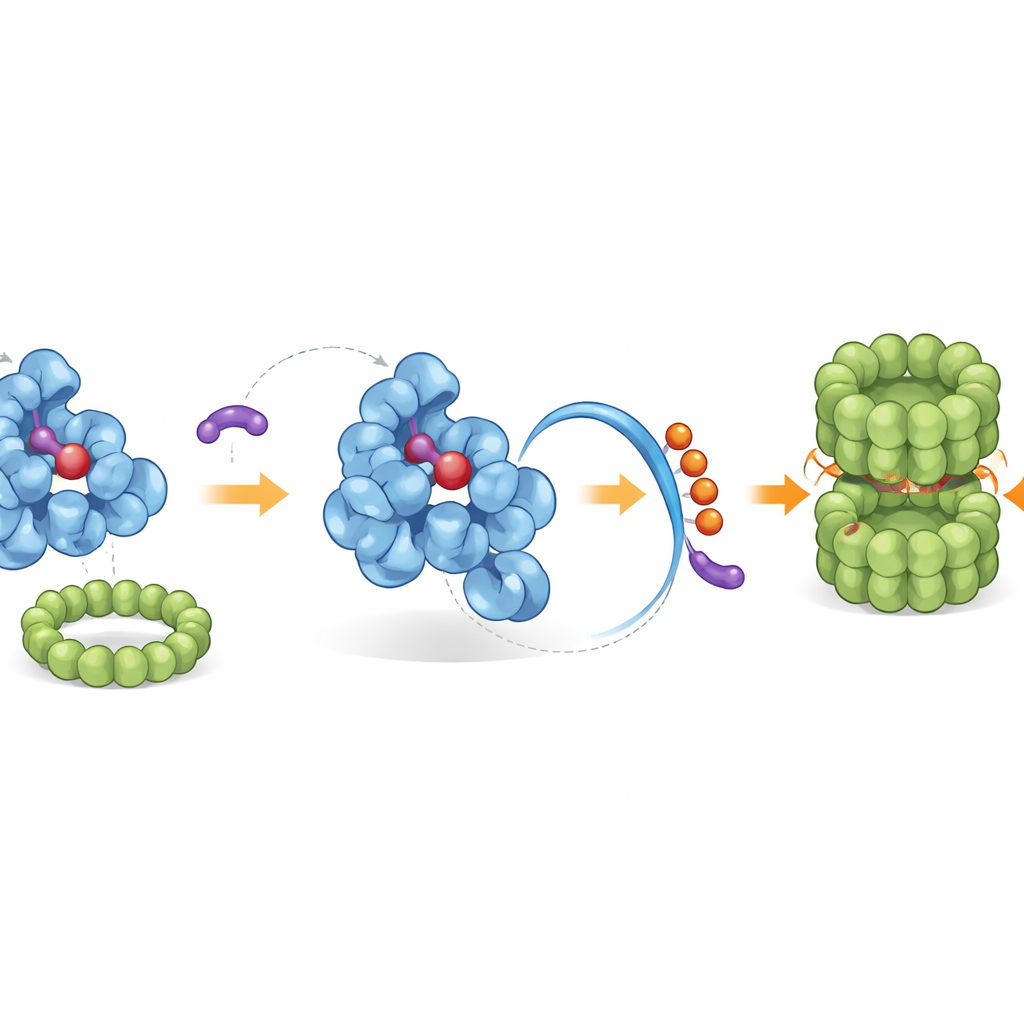
Rekrutowanie rodzimych sprzątaczy komórkowych
Przekształcony ogon odsłania wbudowany „koniec znacznik”, który maszyneria usuwania odpadów komórkowych rozpoznaje. Dzięki przesiewom genetycznym i rekonstrukcjom biochemicznym badacze zidentyfikowali konkretny kompleks ligazowy, zwany CRL2–KLHDC3, który naturalnie przyłącza małe „flagi” ubikwityny do odsłoniętego ogona IDO1, znakując go do degradacji przez proteasom — molekularną niszczarkę komórki. W warunkach fizjologicznych tylko forma IDO1 pozbawiona hemu jest efektywnie tak oznaczana, podczas gdy związany z hemem IDO1 jest chroniony. iDegy przechylają tę równowagę, wiążąc się tylko z formą bezhemową i wzmacniając naturalną drogę degradacji. Najsilniejsze związki z serii nie tylko blokują produkcję kinureniny, lecz także zwiększają ubikwitynację IDO1 i zdecydowanie obniżają poziom tego białka w różnych typach komórek nowotworowych.
Zmiana losu IDO1 — i odpowiedzi immunologicznych
To dwuaspektowe działanie ma istotne konsekwencje funkcjonalne. W testach migracji komórek raka jajnika klinicznie badany inhibitor IDO1, który stabilizuje enzym, w rzeczywistości przyspieszył ruch komórek, co zgadza się z nieenzymatyczną, pro‑nowotworową rolą IDO1. Przeciwnie, związek z serii iDeg spowolnił migrację, zgodnie zarówno z zahamowaniem aktywności enzymatycznej, jak i utratą samego białka. Badanie ujawnia więc nowy sposób manipulowania IDO1: nie przez siłowe przenoszenie go do obcej ligazy za pomocą masywnej, zaprojektowanej cząsteczki, lecz przez „doładowanie” istniejącej, rodzimniej drogi degradacji, która już funkcjonuje w komórkach.
Co to może znaczyć dla przyszłych terapii przeciwnowotworowych
Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że ważna jest jakość — nie tylko ilość — hamowania enzymu. Nowe małe cząsteczki działają jak precyzyjne wyłączniki: blokują IDO1 w podatnej konformacji, którą komórka jest przygotowana zniszczyć, odcinając zarówno jego wkład metaboliczny, jak i sygnalizacyjny w przetrwaniu guza. Ponieważ iDegy są kompaktowe, mają właściwości zbliżone do leków i polegają na własnej ligazie komórki do usunięcia IDO1, mogą oferować subtelniejsze i szerzej stosowalne podejście niż wcześniejsze „degradery białek”. Jeśli podobne strategie da się zastosować do innych problematycznych białek, praca ta zapowiada nową generację terapii, które skłaniają chore komórki do demontażu własnych molekularnych „broni”.
Cytowanie: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Słowa kluczowe: IDO1, immunoterapia przeciwnowotworowa, ukierunkowana degradacja białek, ligaza ubikwitynowa, małocząsteczkowe degradery