Clear Sky Science · pl
Biokompatybilne zrównoważenie ligandów w koordynacji metali przejściowych umożliwia łagodną arylację białek w komórce
Przekształcanie metali w delikatne narzędzia komórkowe
Wiele potężnych reakcji chemicznych opiera się na metalach, lecz zbliżenie tych samych metali do żywych komórek zwykle kończy się problemami: uszkodzeniem, stresem i śmiercią komórek. W badaniu pokazano, że przy odpowiednim „uchwycie” molekularnym wokół atomu niklu można przeprowadzić złożoną reakcję wewnątrz żywych komórek bez ich uszkadzania. Ten przełom pozwala naukowcom oznaczać tysiące konkretnych miejsc w białkach, a nawet śledzić pojawianie się trudnych do wykrycia patogenów, otwierając nowe możliwości mapowania tego, co naprawdę dzieje się w komórkach w zdrowiu i chorobie.
Dlaczego metale są zarazem sprzymierzeńcami i zagrożeniem
Nikiel i inne metale działają już cicho w naszych organizmach jako składniki naturalnych enzymów, ale mogą też być toksyczne, jeśli wiążą się w niewłaściwym miejscu. Natura rozwiązuje ten problem, otaczając metale starannie dobranymi małymi cząsteczkami i białkami, które kierują je do właściwych celów i blokują niepożądane reakcje. Chemicy natomiast często stosują odczynniki metaloorganiczne o bardzo dużej reaktywności i bez dopasowania do warunków biologicznych. Były one doskonałymi narzędziami do budowy złożonych cząsteczek w kolbie, ale zbyt ostrymi, by używać ich swobodnie w komórkach, zwłaszcza gdy celem jest przyłączenie małego „znacznika” do konkretnego aminokwasu w białku bez zakłócania reszty komórki.
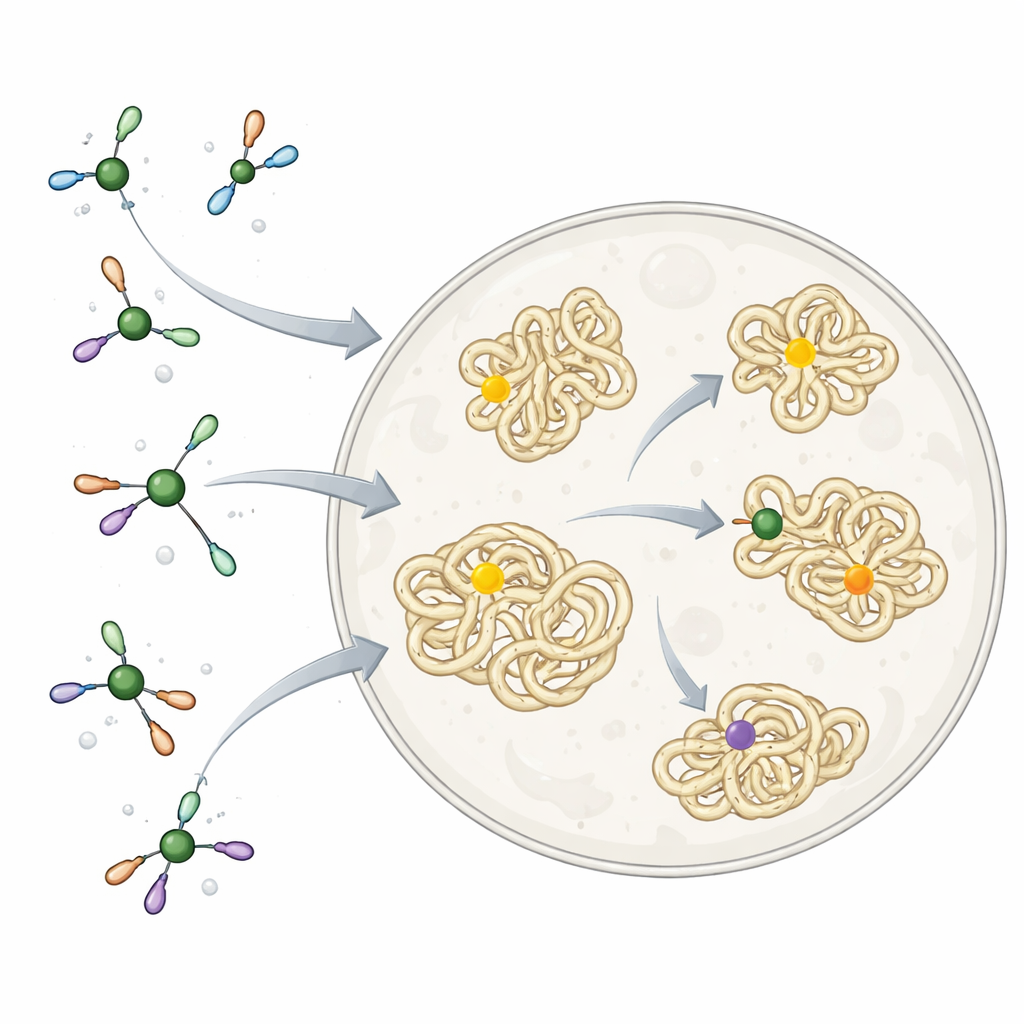
Projektowanie łagodniejszego odczynnika niklowego
Badacze czerpali inspirację z tego, jak komórki same radzą sobie z niklem. Zbudowali zestaw kompleksów niklu otoczonych prostym, biokompatybilnym ligandem zwanym TMEDA. Ta mała cząsteczka działa jak miękki zacisk: na tyle silny, by zapobiec przyklejaniu się niklu do niewłaściwych składników komórkowych, ale na tyle luźny, by pozwolić mu wykonać kluczową reakcję. Reakcja łączy fragment arylowy — płaski, pierścieniowy grupę często spotykaną w lekach — z atomem siarki aminokwasu cysteiny w białkach. Na oczyszczonych białkach w roztworze te kompleksy niklu bardzo szybko i selektywnie przyłączały grupy arylowe do pojedynczych miejsc cysteinowych i działały przy wielu różnych kształtach i pozycjach białek, co wskazuje, że chemia ta jest szeroko zgodna z prawdziwymi cząsteczkami biologicznymi.
Edycja białek wewnątrz żywych komórek
Następnie zespół zapytał, czy te same odczynniki będą działać wewnątrz żywych komórek bez toksycznego działania. Porównali proste sole niklu, znane z szkodliwości, z kompleksami niklu związanymi z TMEDA. W komórkach ssaczych proste źródła niklu powodowały znaczną śmiertelność komórek przy stosunkowo niskich dawkach, natomiast zrównoważone ligandowo kompleksy były dobrze tolerowane nawet przy stężeniach milimolowych. To okno bezpieczeństwa pozwoliło badaczom na zanurzenie bakterii i komórek ssaczych w odczynnikach niklowych wystarczająco długo, by przeniknęły one do wnętrza i modyfikowały białka. Poprzez wbudowanie azotowego „uchwytu” w jedną wersję grupy arylowej mogli później dołączać fluorescencyjne barwniki lub znaczniki biotynowe po reakcji, ujawniając wyraźne, zależne od dawki barwienie białek w cytoplazmie i jądrze żywych komórek.
Mapowanie reaktywnych miejsc białek w całym proteomie
Mając bezpieczną i szybką reakcję wewnątrz komórek, autorzy przekształcili ją w narzędzie odkrywcze. Traktowali żywe komórki ludzkie odczynnikiem niklowym zawierającym azot, a następnie użyli fotoczułej biotyny i zaawansowanej spektrometrii mas, aby zobaczyć dokładnie, które cysteiny zostały zmodyfikowane. W pojedynczym eksperymencie wykryli niemal 11 000 miejsc cysteinowych w prawie 5 000 białkach — około dwa razy więcej białek niż we wszystkich poprzednich badaniach profilowania cysteiny w żywych komórkach łącznie. Oznaczanie było wysoce selektywne względem cysteiny i wykazywało niewielkie uprzedzenia co do określonych typów białek, lokalizacji czy znanych miejsc aktywnych. Co ciekawe, wiele z celowanych białek było uważanych za „nieligandowalne” według obecnych standardów odkrywania leków, w tym białka sygnalizacyjne o niskiej obfitości i przełączniki czułe na redoks, które trudno badać jedynie metodami genetycznymi.
Śledzenie ukrytych patogenów w czasie rzeczywistym
Ta sama chemia okazała się także na tyle czuła, by wykrywać obce białka powstające podczas infekcji. W komórkach ludzkich zawierających latentne sekwencje wirusowe metoda wykryła czynniki transkrypcyjne wirusa obecne na niezwykle niskich poziomach, w tym alternatywne formy splicingowe. Zespół następnie zakażał komórki dwoma bardzo różnymi patogenami: wewnątrzkomórkową bakterią Chlamydia trachomatis oraz wirusem Sindbis, wirusem RNA spokrewnionym z chikungunya. Poprzez pulsacyjne traktowanie zakażonych komórek odczynnikiem niklowym w różnych momentach byli w stanie pułapkować miejsca cysteinowe na kluczowych bakteryjnych białkach rybosomalnych i regulatorowych, gdy bakteria przechodziła między etapami cyklu życiowego, oraz na krytycznych wirusowych białkach nien strukturalnych, które napędzają replikację RNA. Oznaczone miejsca wyróżniają się teraz jako potencjalne słabe punkty przyszłych strategii przeciwwirusowych lub przeciwbakteryjnych.
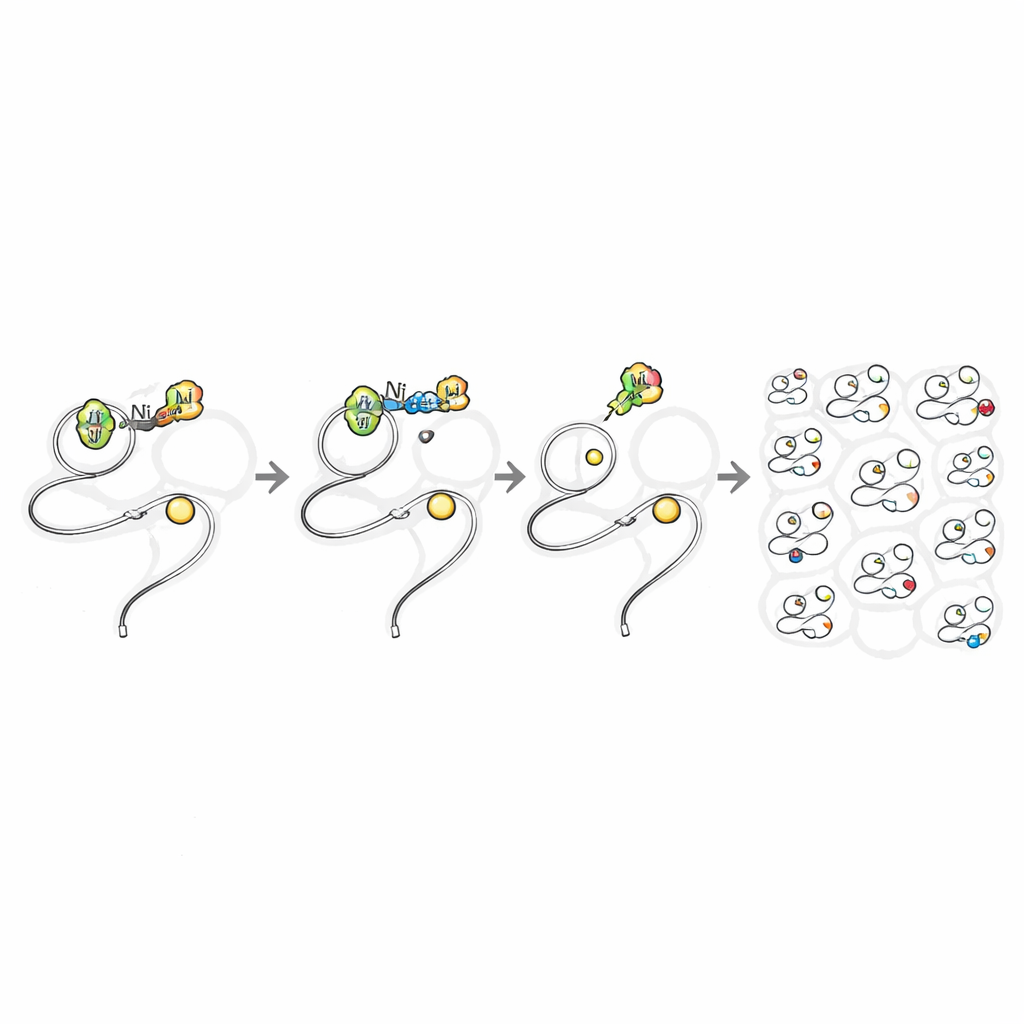
Co to oznacza dla przyszłej chemii komórkowej
Poprzez staranne zrównoważenie powłoki ligandowej wokół niklu praca ta pokazuje, że tradycyjnie ryzykowny metal może przeprowadzić precyzyjną, kowalencyjną reakcję edycji białek głęboko wewnątrz żywych komórek przy minimalnej szkodliwości. Umożliwia to stworzenie szczegółowej, funkcjonalnej mapy reaktywnych miejsc cysteinowych w całym proteomie, w tym białek rzadkich, przejściowych lub trudnych do zaadresowania farmakologicznie. Oferuje też sposób śledzenia i badania patogenów w komórkach gospodarza na poziomie pojedynczych aminokwasów. Szerzej rzecz ujmując, badanie sugeruje, że wiele innych „zakazanych” chemii metali może zostać oswojonych w podobny sposób, otwierając nową erę, w której potężne narzędzia chemii syntetycznej działają bezpiecznie w systemach żywych.
Cytowanie: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Słowa kluczowe: profilowanie cysteiny, biokonjugacja niklem, znakowanie białek w żywych komórkach, chemoproteomika, mapowanie proteomu patogenów