Clear Sky Science · pl
Tłumaczenie lokalne specyficzne dla RNA jest wzorcowane przez kondensaty podczas wzrostu komórek wielojądrzastych
Jak duże komórki synchronizują odległe zadania
Komórki w naszych organizmach zwykle są małymi, samodzielnymi jednostkami z jednym jądrem. Jednak niektóre organizmy, w tym pewne grzyby i komórki mięśniowe, to ogromne przegrody wypełnione wieloma jądrami dzielącymi wspólną cytoplazmę. W takich olbrzymach sygnały i cząsteczki mogą długo dyfundować z miejsca na miejsce, co rodzi pytanie: jak koordynują wzrost i podział na takich odległościach, nie tracąc kontroli? To badanie zajmuje się tym problemem w wielojądrzastym grzybie, ujawniając, jak drobne kropelki wewnątrz komórki lokalnie dostrajają produkcję białek dokładnie tam, gdzie są potrzebne.
Drobne krople, które organizują olbrzymią komórkę
W nitkowatym grzybie Ashbya gossypii długie rurkowate komórki zwane strzępkami zawierają wiele jąder, które dzielą się niesynchronicznie, podczas gdy wzrost odbywa się głównie na końcach. Wcześniejsze prace wykazały, że białko o nazwie Whi3 tworzy mikroskopijne krople, czyli kondensaty, z określonymi informacyjnymi RNA (mRNA) kodującymi kluczowe regulatory cyklu komórkowego i wzrostu wierzchołka. Autorzy postanowili zbadać, co te kondensaty właściwie robią. Przy użyciu szybkiego obrazowania trójwymiarowego odkryli, że kondensaty Whi3 zmieniają rozmiar i liczbę w zależności od ich położenia w komórce oraz lokalnego stanu wzrostu i podziału jąder. Duże kondensaty grupują się w pobliżu wolno rosnących wierzchołków strzępek, podczas gdy mniejsze, bardziej zmienne kondensaty otaczają jądra znajdujące się w określonych fazach cyklu komórkowego. Mutanty grzyba, które nie potrafią tworzyć normalnych kondensatów, rosną szybciej na końcach i wykazują bardziej zsynchronizowane podziały jąder, co sugeruje, że właściwości kondensatów pomagają koordynować te procesy.
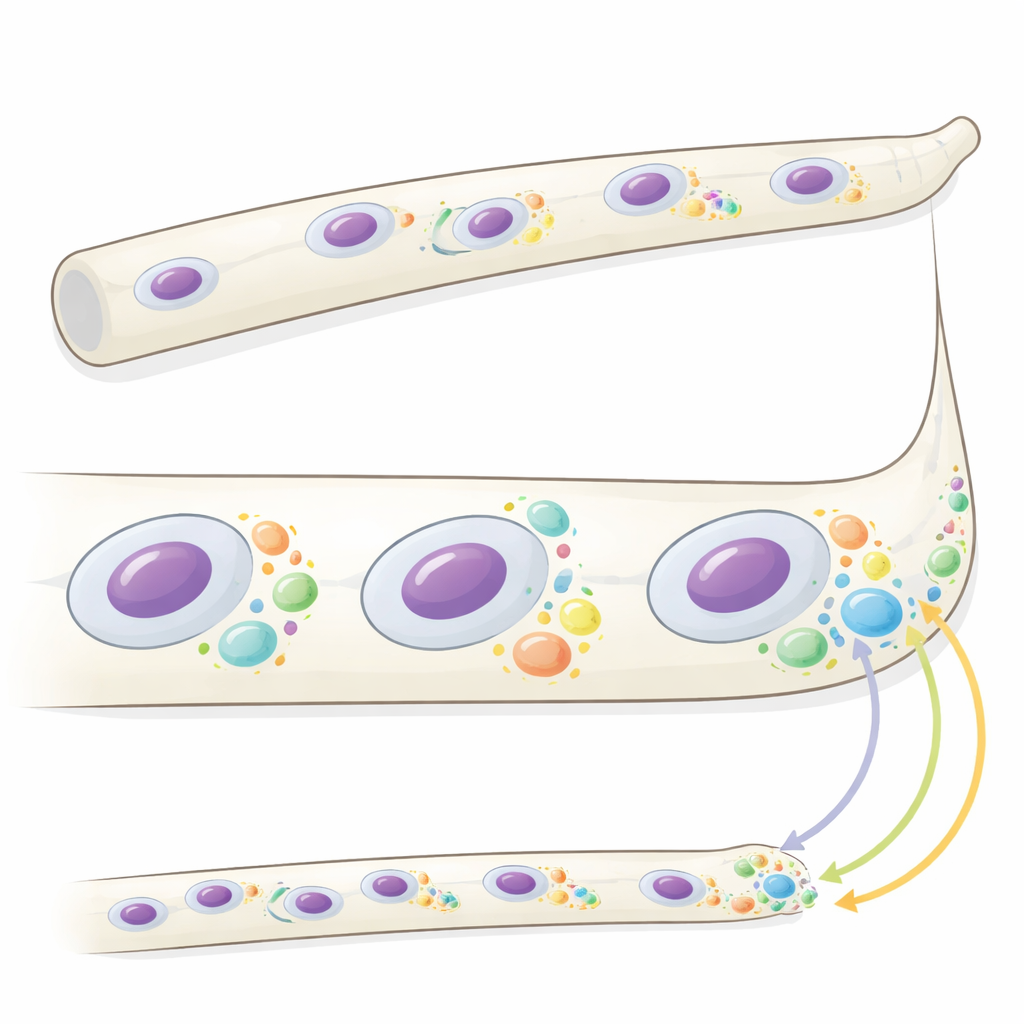
Lokalna produkcja białka zapisana w przestrzeni i czasie
Aby sprawdzić, czy kondensaty Whi3 kontrolują miejsce powstawania białek, zespół zmierzył translację — proces przekształcania mRNA w białko — dla dwóch ważnych wiadomości związanych z Whi3. Jeden, CLN3, koduje cyklinę pomagającą napędzać komórki przez cykl podziału; drugi, BNI1, koduje czynnik kształtujący wzrost na końcu strzępki. Używając czułej metody fluorescencyjnej wykrywającej aktywne rybosomy na pojedynczych endogennych cząsteczkach mRNA, badacze pokazali, że CLN3 jest tłumaczony głównie w pobliżu niektórych jąder i tylko w określonych fazach ich cyklu, szczególnie wokół jąder w mitozie. mRNA BNI1 skupia się przy wierzchołkach strzępek, lecz jego translacja tam jest zwykle rzadka i zmienna. Gdy zachowanie Whi3 zostaje zmienione przez mutację fosfo-mimetyczną, translacja BNI1 staje się mocno wzbogacona na końcach, a wzrost końców przyspiesza, co ujawnia, że Whi3 może tłumić lub umożliwiać translację w zależności od swojego stanu i lokalizacji.
Minimalne składniki, wiele wyników
Aby sprawdzić, czy takie dostrajanie jest właściwością wrodzoną składników kondensatu, autorzy odtworzyli system w ekstraktach bezkomórkowych. Do obszarów regulatorowych mRNA CLN3 lub BNI1 dołączyli raporter lucyferazy i zmieszali te RNA z oczyszczonym Whi3 w różnych stężeniach. Przy niskich poziomach, gdy nie tworzą się krople, translacja zmieniała się niewiele. Przy wyższych poziomach sprzyjających tworzeniu kondensatów translacja związana z CLN3 była silnie zahamowana w miarę wzrostu stężenia Whi3 i rozmiaru kondensatów. BNI1 zachowywał się inaczej: umiarkowany poziom kondensatów zwiększał jego translację, podczas gdy bardziej obfite lub większe kondensaty przełączały układ w stan represji. Mutanty Whi3 tworzące mniejsze lub mniej liczebne krople albo RNA z mniejszą liczbą miejsc wiązania Whi3 przesuwały te odpowiedzi, często łagodząc represję i zwiększając translację. Te eksperymenty pokazują, że te same podstawowe składniki — Whi3, jego docelowe RNA i ich kondensaty — mogą generować kontinuum stanów translacyjnych poprzez zmianę stężenia, siły oddziaływań lub rozmiaru kropli.
Gdzie zachodzi translacja: na krawędzi kropli
Badania masowe uśredniają sygnał po wielu cząsteczkach i nie ujawniają, gdzie dokładnie zachodzi translacja w obrębie kondensatów lub wokół nich. Aby to zobrazować bezpośrednio, zespół użył raportera „MoonTag”, który świeci, gdy nowe łańcuchy białkowe wyłaniają się z rybosomów. In vitro zaobserwowali sygnały MoonTag akumulujące się na i w obrębie kropli Whi3–RNA, dowodząc, że te kondensaty mogą być rzeczywiście aktywnymi miejscami translacji, a nie jedynie magazynami. Co uderzające, zarówno rybosomy, jak i sygnały nowo powstających białek były najsilniejsze na interfejsie kropli, tworząc jasne pierścienie wokół każdego kondensatu. Mniejsze kondensaty, mając większy stosunek powierzchni do objętości, wspierały więcej translacji na RNA niż większe krople, które ogólnie były bardziej represyjne. Zmiana walencji RNA lub stanu ładunku Whi3 przesuwała to, czy ta strefa sprzyjająca translacji leżała na powierzchni, czy głębiej wewnątrz, co wskazuje, że subtelne cechy molekularne kondensatu dostrajają, jak łatwo aparat translacyjny może uzyskać dostęp do obecnych tam RNA.
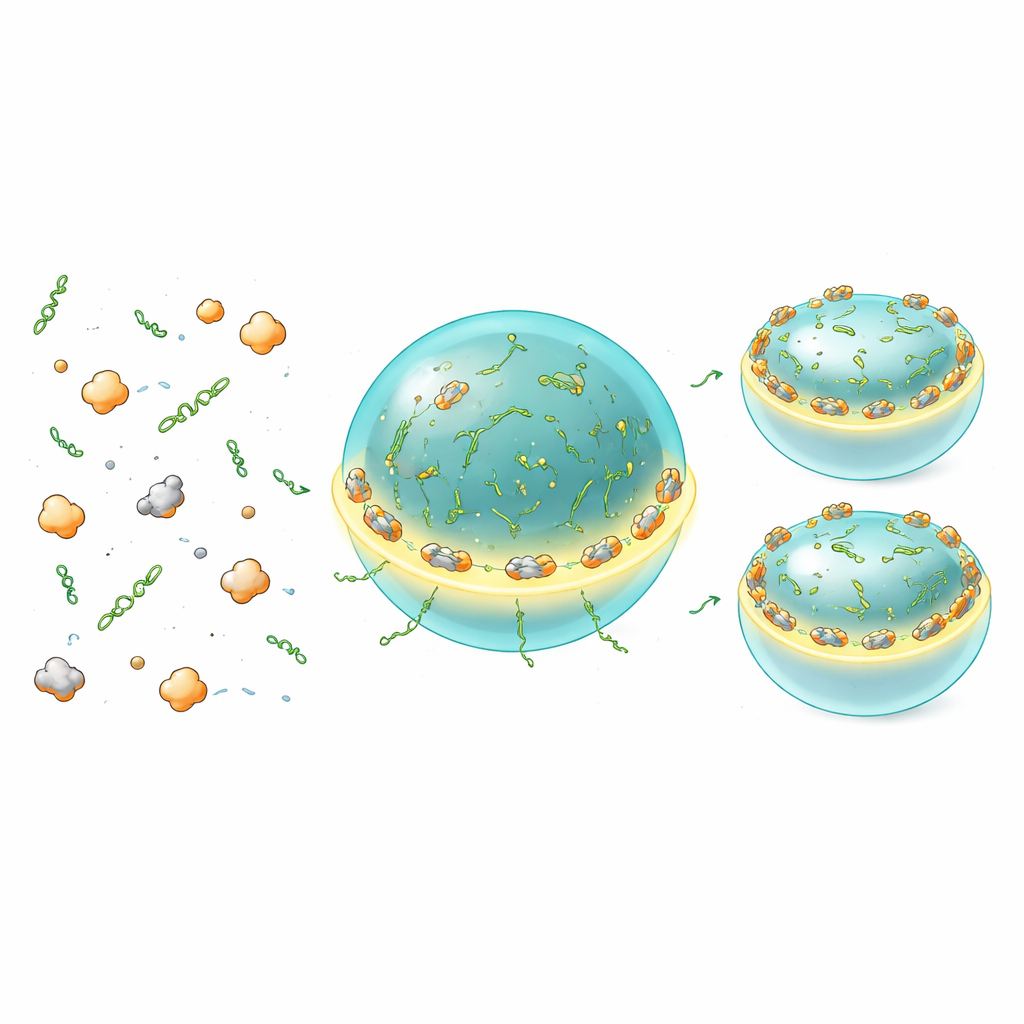
Precyzyjne dawkowanie dla zrównoważonego wzrostu
W sumie praca przedstawia kondensaty Whi3–RNA jako regulowane zawory, które odmierzają lokalnie wytwarzane białko, zamiast prostych włączników on–off. W grzybie oznacza to, że cyklina CLN3 może być produkowana w impulsach wokół wybranych jąder, by utrzymać ich cykle podziałowe w przeciwfazie, podczas gdy BNI1 może powstawać w przerywanych zrywach na końcach strzępek, podtrzymując wzrost, ale zapobiegając niekontrolowanej ekspansji w jednym miejscu. Gdy formowanie kondensatów lub ich własności zostają zaburzone, ta subtelna kontrola zanika: produkcja białka staje się bardziej jednorodna w przestrzeni i czasie, jądra dzielą się synchronicznie, zmieniają się wzory rozgałęzień, a ogólna morfologia ulega zaburzeniu. Dla szerokiego odbiorcy główne przesłanie jest takie, że komórki potrafią wykorzystywać maleńkie krople rozdzielone fazowo jako przestrzennie i czasowo strojoną aparaturę reakcyjną, pozwalając wielkim, wielojądrzastym komórkom koordynować wzrost i podział na dużych odległościach poprzez lokalne kształtowanie czasu i miejsca syntezy białek.
Cytowanie: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Słowa kluczowe: kondensaty biomolekularne, tłumaczenie lokalne, kontrola cyklu komórkowego, strzępki grzybowe, separacja faz