Clear Sky Science · pl
Ubikitynacja w pozycji lizyny 11 uruchamia indukcję interferonów typu I/III przez szlak cGAS–STING oraz receptory Toll-podobne 3 i 4
Jak nasze komórki biją na alarm
Gdy wirusy lub niebezpieczne cząsteczki wnikają do organizmu, nasze komórki muszą w ciągu minut zdecydować, czy uruchomić potężne antywirusowe sygnały alarmowe zwane interferonami. Te sygnały mogą ochronić nas przed ciężkimi zakażeniami — ale gdy są uruchomione niewłaściwie, mogą też napędzać szkodliwe choroby autoimmunologiczne. W badaniu tym odkryto wcześniej ukryty molekularny „centrala”, który pomaga zdecydować, kiedy włączać odpowiedzi interferonowe, a kiedy je powstrzymać. Zrozumienie tej centrali daje wskazówki dla lepszych szczepionek, terapii przeciwwirusowych i leczenia schorzeń napędzanych przez interferony.
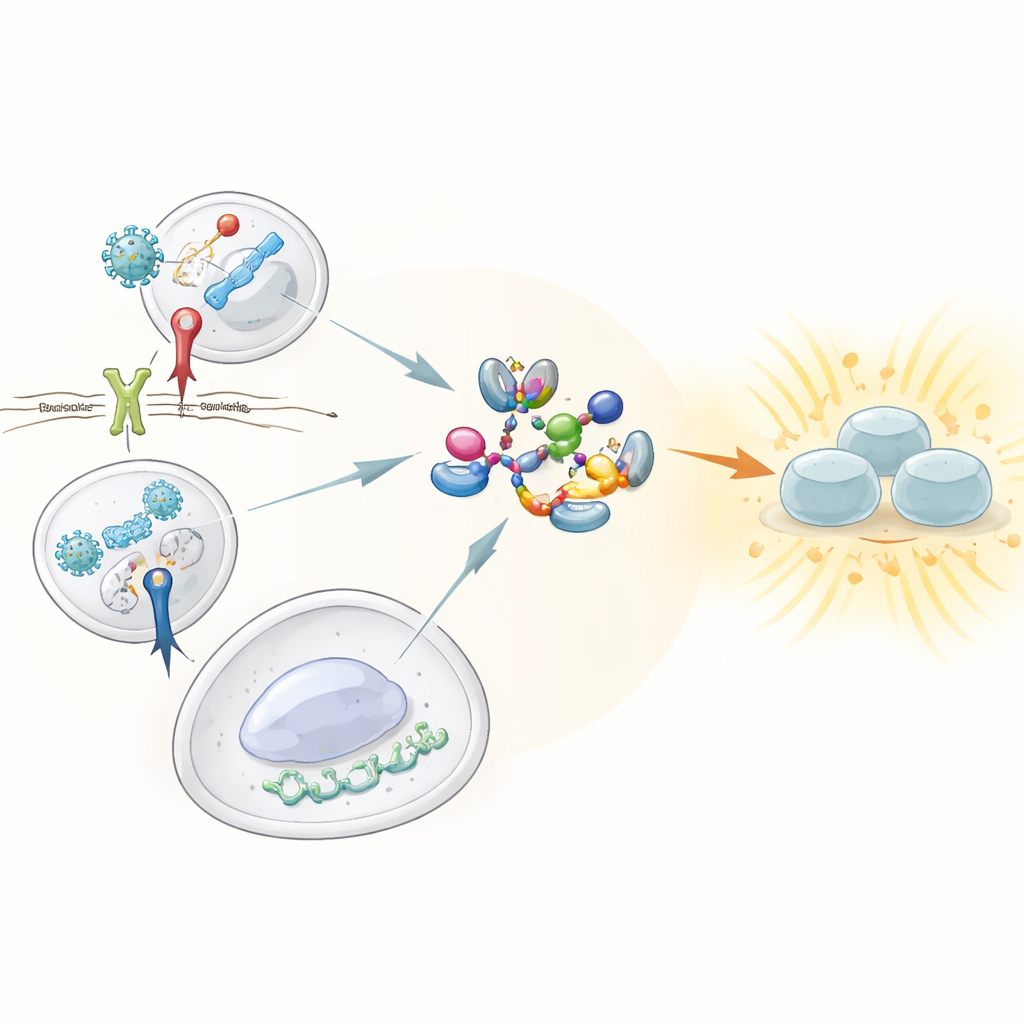
Strażnicy wyczuwający zagrożenie
Nasza odporność wrodzona opiera się na strażnikach zwanych receptorami rozpoznającymi wzorce, które patrolują w poszukiwaniu charakterystycznych cech wirusów i bakterii. Wśród nich trzy wyróżniają się zdolnością do wywoływania silnych odpowiedzi interferonowych: receptor Toll-podobny 3 (TLR3), który wykrywa dwuniciowe RNA wirusów; receptor Toll-podobny 4 (TLR4), który wyczuwa składnik ścian komórkowych bakterii; oraz szlak cGAS–STING, który rozpoznaje DNA znajdujące się w nieodpowiednim miejscu wewnątrz komórek. Wszystkie trzy muszą aktywować centralny enzym TBK1, który z kolei uruchamia czynnik transkrypcyjny IRF3, napędzając produkcję interferonów typu I i III. Dotychczas nie było dobrze zrozumiane, w jaki sposób te sensory zbiegają się na TBK1, by przełączyć go w stan aktywny.
Ukryty łącznik molekularny
Naukowcy odkryli, że białko o nazwie ANKIB1 działa jako istotny łącznik między tymi sensorami a TBK1. ANKIB1 jest enzymem, który przyłącza małe znaczniki molekularne, znane jako łańcuchy ubikwityny, do innych białek. Co ważne, buduje ono specyficzny typ łańcucha oparty na wiązaniu nazywanym „K11”, który wcześniej był lepiej znany z ról w podziale komórkowym niż w odporności. W ludzkich komórkach pozbawionych ANKIB1 stymulacja TLR3 lub aktywacja STING przestała prawidłowo prowadzić do aktywacji TBK1 i IRF3, a geny interferonowe ledwo się włączały. Przywrócenie ANKIB1 odtwarzało odpowiedź, co pokazuje, że ten pojedynczy enzym jest zarówno niezbędny, jak i wystarczający do uruchomienia tej gałęzi alarmu przeciwwirusowego.
Budowanie platformy dokującej dla białek przekaźnikowych
Bliższa inspekcja ujawniła, jak ANKIB1 wywiera swój wpływ. Gdy TLR3 lub STING wykrywają zagrożenie, tworzą wielobiałkowe platformy zwane signalosomami. ANKIB1 jest rekrutowany do tych platform przez region rozpoznający ubikwitynę. Będąc tam, ozdabia kilka kluczowych komponentów — w tym białka adaptorowe TRIF i samego STING oraz inne cząsteczki sygnalizacyjne — łańcuchami ubikwityny powiązanymi przez K11. Te łańcuchy nie oznaczają po prostu białek do degradacji; zamiast tego działają jak molekularne rzepy. Inne białko, Optineuryna (OPTN), jest przyciągane specyficznie do takich zmodyfikowanych miejsc. Działając jako adaptor przekaźnikowy, OPTN następnie sprowadza TBK1 do kompleksu, aby mógł zostać aktywowany i przekazać sygnał dalej do IRF3 i genów interferonowych. Gdy OPTN został usunięty, aktywacja TBK1 upadła, co podkreśla, że znakowanie K11 przez ANKIB1 i wiązanie OPTN tworzą jedną, niezbędną oś.
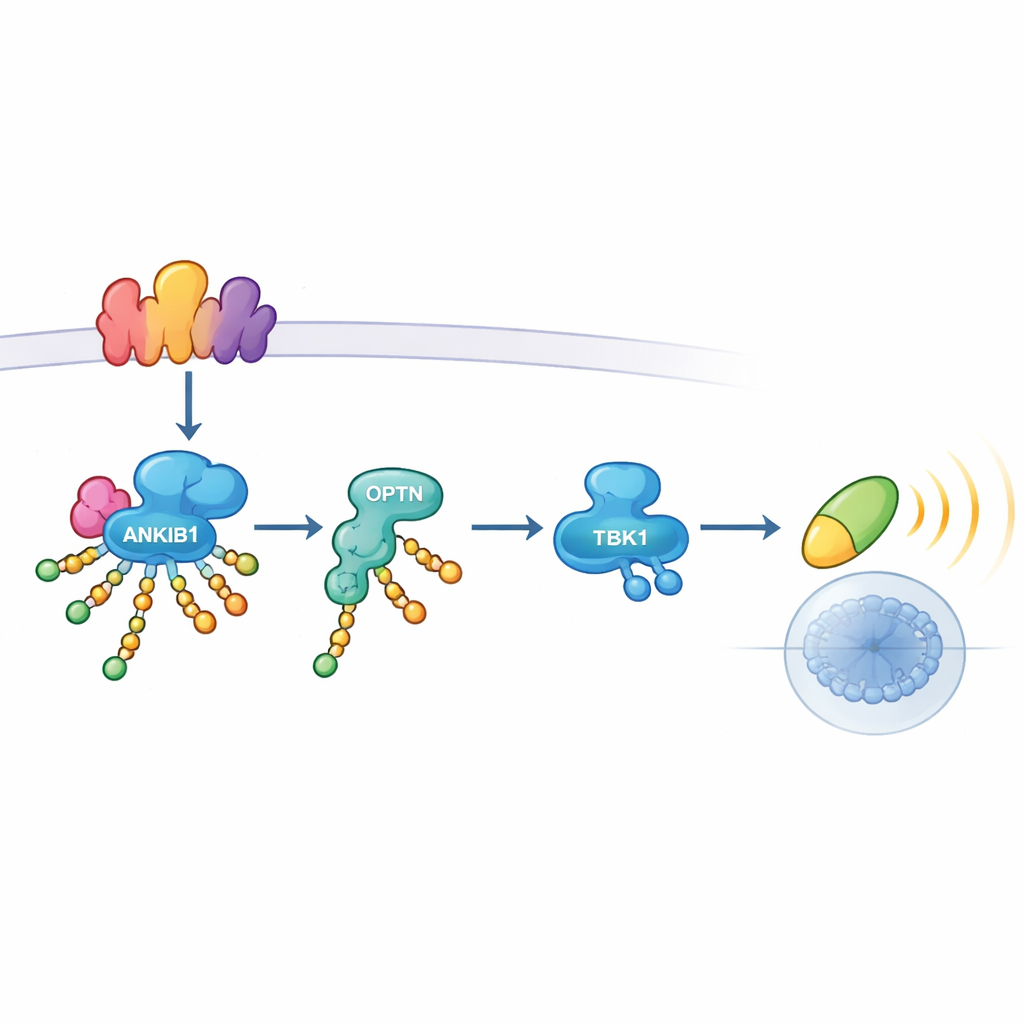
Kiedy ten szlak ma znaczenie — a kiedy nie
Zespół następnie zapytał, czy ten mechanizm jest uniwersalny dla wszystkich sensorów przeciwwirusowych. Odkryli, że ANKIB1 jest kluczowy dla indukcji interferonu za pośrednictwem TLR3, zależnego od TRIF ramienia TLR4 oraz szlaku cGAS–STING, z których wszystkie używają OPTN jako głównego adaptoru do TBK1. W przeciwieństwie do tego inny sensor, RIG-I, który wykrywa RNA wirusowe, polega na innym zestawie białek adaptorowych i nie potrzebuje ANKIB1 ani OPTN do aktywacji TBK1. Eksperymenty na myszach potwierdziły te obserwacje z komórek. Zwierzęta pozbawione Ankib1 wytwarzały znacznie mniej interferonu po aktywacji TLR3 lub STING, były chronione przed śmiertelnym zespołem zapalnym wywołanym nadmiernym interferonem, lecz stały się znacznie bardziej podatne na zakażenie wirusem opryszczki pospolitej typu 1, wirusem DNA, który w dużym stopniu zależy od interferonu napędzanego przez cGAS–STING. Odpowiedzi na wirusa grypy, który jest wykrywany głównie przez RIG-I, pozostały w dużej mierze nienaruszone.
Równoważenie ochrony i szkody
W sumie wyniki te ukazują łańcuchy ubikwityny powiązane przez K11, generowane przez ANKIB1, jako centralną walutę w głównym odgałęzieniu wrodzonego sygnalizowania przeciwwirusowego. Tworząc miejsca dokowania dla OPTN, ANKIB1 pomaga składać precyzyjny molekularny przekaźnik, który przekształca wykrywane zagrożenie przez TLR3, TLR4 (przez TRIF) i cGAS–STING w silną produkcję interferonów. Ta oś ma podwójną naturę: jest niezbędna do obrony przed pewnymi wirusami, ale także napędza zapalne choroby związane z interferonem, gdy jest nadmiernie aktywna. Ponieważ aktywność katalityczna ANKIB1 i jego specyficzne domeny są wymagane do tej funkcji, stanowią one atrakcyjne cele dla przyszłych leków zaprojektowanych albo w celu stłumienia szkodliwych odpowiedzi interferonowych w schorzeniach autoimmunologicznych, albo wzmocnienia odporności przeciwwirusowej tam, gdzie jest ona zbyt słaba.
Cytowanie: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Słowa kluczowe: odporność wrodzona, sygnalizacja interferonowa, ubikwitynacja, szlak cGAS–STING, infekcja wirusowa