Clear Sky Science · pl
Tkanka tłuszczowa otaczająca guz sprzyja unikaniu immunologicznemu w raku jelita grubego poprzez przemianę adipocytów w mezenchymalne komórki zrębowe
Dlaczego tłuszcz brzuszny wokół guza ma znaczenie
Rak jelita grubego rozwija się w ścianie jelita, ale styka się bezpośrednio z grubą warstwą tłuszczu brzusznego. Większość osób postrzega ten tłuszcz jako bierną wyściółkę. To badanie ujawnia coś zaskakującego: tłuszcz otaczający guz może potajemnie odciągać komórki odpornościowe walczące z rakiem, pomagając nowotworowi ukryć się przed układem odpornościowym. Zrozumienie tej ukrytej rywalizacji wskazuje nowe sposoby przewidywania, kto zareaguje na immunoterapię, oraz jak poprawić skuteczność tych terapii.
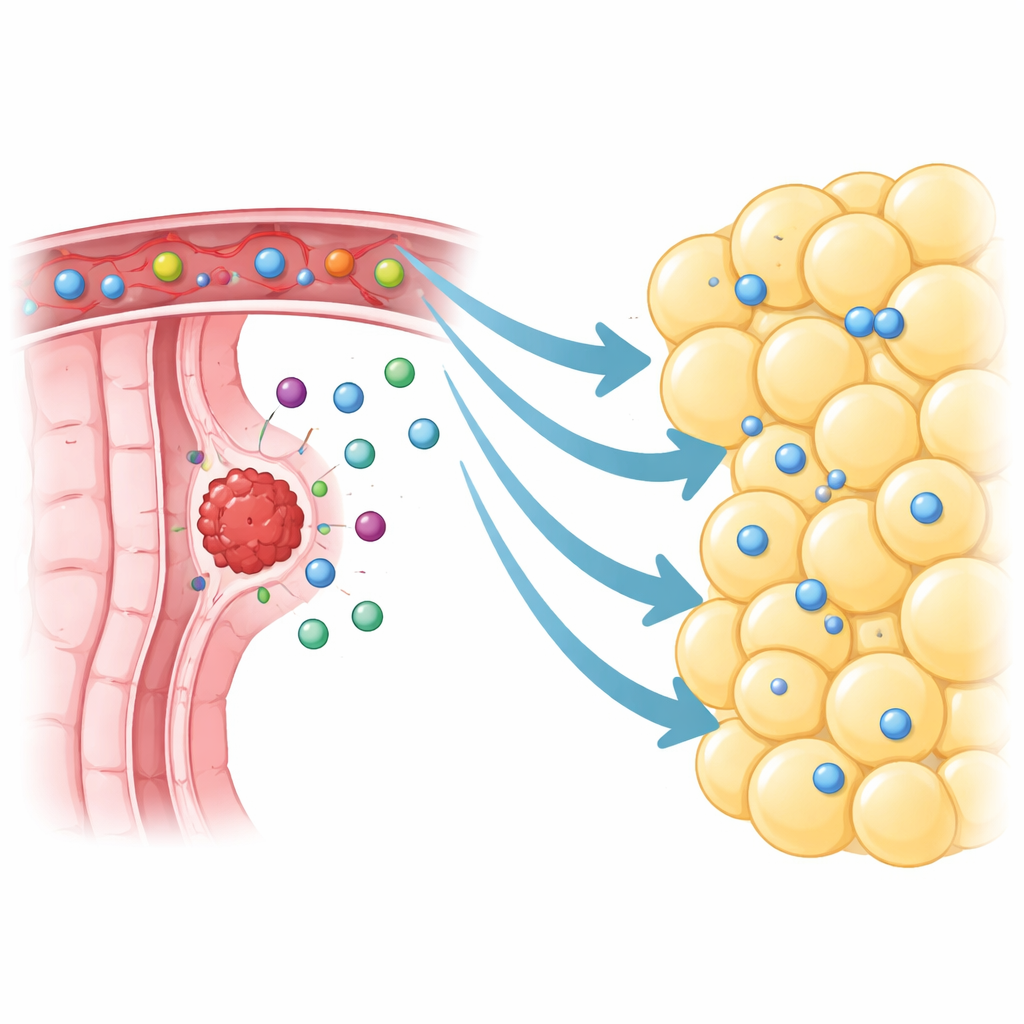
Ruchliwa, odpornościowa okolica obok guza
Naukowcy skoncentrowali się na trzewnym tłuszczu bezpośrednio otaczającym guzy jelita grubego, zwanym peritumoralną tkanką tłuszczową trzewną. Przy użyciu sekwencjonowania RNA pojedynczych komórek odwzorowali ponad 370 000 indywidualnych komórek z guzów, pobliskiego tłuszczu, oddalonego tłuszczu i tkanki normalnej. Zamiast być cicha i obojętna, tkanka tłuszczowa przy guzie wrzała od komórek odpornościowych, zwłaszcza limfocytów T i B. Naukowcy znaleźli nawet zorganizowane skupiska przypominające małe węzły chłonne, co świadczy, że ta tkanka może gościć aktywne reakcje odpornościowe. W porównaniu z tłuszczem pobranym z dalszych miejsc, peritumoralny tłuszcz zawierał znacznie więcej limfocytów, w tym komórek pamięci i swoistych dla guza cytotoksycznych limfocytów T, które zasadniczo powinny patrolować w poszukiwaniu nowotworu.
Kiedy pomocne komórki odpornościowe trafiają w niewłaściwe miejsce
Aby sprawdzić, czy ten bogaty w komórki odpornościowe tłuszcz pomaga czy szkodzi, zespół użył modeli mysich, w których guzy były wszczepiane przy poduszce tłuszczowej przypominającej sytuację u ludzi. Następnie chirurgicznie usuwali ten pobliski tłuszcz lub chemicznie go rozpuszczali. Paradoksalnie, usunięcie peritumoralnego tłuszczu spowolniło wzrost guza. Guzy z myszy, którym usunięto ten tłuszcz, zawierały więcej limfocytów CD4 i CD8, w tym komórek rozpoznających antygeny guza. Dodatkowe eksperymenty śledzące komórki odpornościowe dawców wykazały, że gdy tłuszcz był obecny, wiele z tych komórek gromadziło się w poduszce tłuszczowej zamiast w guzie. Usunięcie tłuszczu przekierowywało komórki do guza, wzmacniając odpowiedź przeciwnowotworową. Innymi słowy, tłuszcz działał jako konkurencyjny rezerwuar, który pochłaniał komórki odpornościowe i utrudniał im dotarcie do prawdziwego celu.
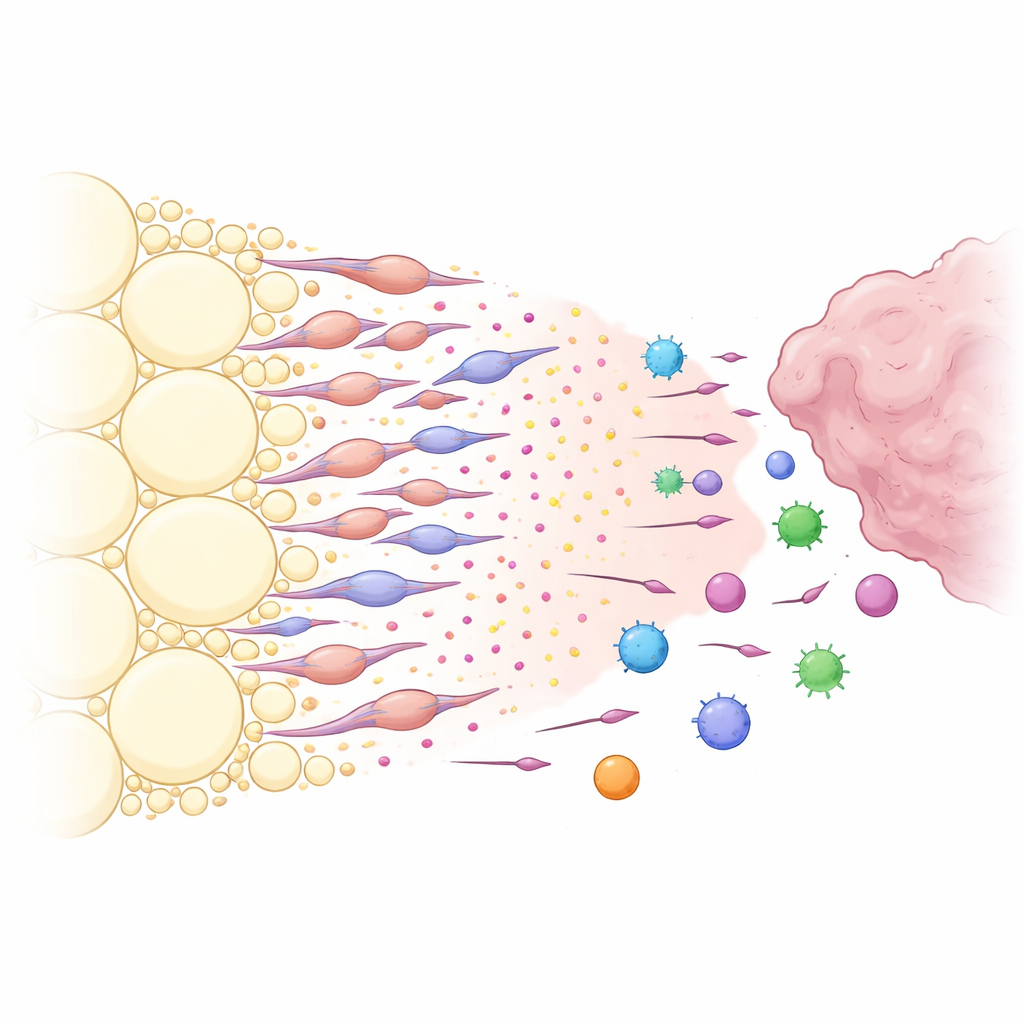
Chemiczna przynęta tworzona przez przekształcone komórki tłuszczowe
Co sprawiało, że peritumoralny tłuszcz tak skutecznie przyciągał komórki odpornościowe? Analizując sygnały komunikacyjne między typami komórek, badacze zidentyfikowali silną ścieżkę chemiczną skoncentrowaną na molekule CXCL12 i jej receptorze CXCR4. Komórki zrębu w tłuszczu przy guzie produkowały wysokie poziomy CXCL12, podczas gdy wiele komórek odpornościowych wyrażało CXCR4, co czyniło je wrażliwymi na ten sygnał. Lokal blokujący CXCL12 w tłuszczu lub genetyczne usunięcie go w zrębie tłuszczowym powodowało kurczenie się guzów i pozwalało większej liczbie CXCR4-dodatnich komórek odpornościowych przeniknąć do guza zamiast być odprowadzanymi. Zespół odkrył następnie, że głównymi producentami CXCL12 nie były zwykłe adipocyty, lecz specjalna grupa komórek fibroblastopodobnych pochodzących z tkanki tłuszczowej, nazwanych przez autorów adipocytarnymi fibroblastami związanymi z rakiem. Czynniki uwalniane przez guz, zwłaszcza czynnik wzrostu TGF-β1, skłaniały lokalne komórki zrębu tłuszczowego do przekształcenia się w te fibroblastopodobne komórki, które z kolei wydzielały duże ilości CXCL12 i innych sygnałów sprzyjających wzrostowi.
Przekształcenie tarczy w słaby punkt
Ponieważ te przekształcone komórki pomagają odprowadzać komórki odpornościowe z dala od guza, badacze sprawdzili, czy rozmontowanie tego „odpornościowego zbiornika” może poprawić immunoterapię. U myszy zaprojektowanych tak, by adipocytarne fibroblasty związane z rakiem mogły być selektywnie eliminowane, leczenie przeciwciałem blokującym PD-1 stało się znacznie skuteczniejsze: guzy rosły wolniej, a do guza napływało więcej swoistych dla guza i CXCR4-dodatnich limfocytów T. Podobnie leki lub przeciwciała blokujące CXCL12 lub jego receptor CXCR4 działały synergistycznie z blokadą PD-1 w modelach raka jelita grubego podskórnych i ortotopowych. Takie kombinacje nie tylko zmniejszały rozmiar guza, lecz także przebudowywały pejzaż odpornościowy wewnątrz guza.
Wskazówki z badań obrazowych pacjentów i co dalej
Zespół sprawdził następnie, czy ich odkrycia mają znaczenie u pacjentów. W grupie osób z miejscowo zaawansowanym rakiem jelita grubego otrzymujących skojarzoną chemioterapię, radioterapię i immunoterapię przeciw PD-1, ci, którzy osiągnęli całkowitą odpowiedź, mieli zwykle mniejszą objętość peritumoralnego tłuszczu trzewnego w rezonansie magnetycznym przed leczeniem. Ilościowo obszar tego tłuszczu przewidywał odpowiedź na terapię lepiej niż niektóre standardowe markery tkankowe, a pacjenci z dużą objętością peritumoralnego tłuszczu mieli znacznie niższe wskaźniki odpowiedzi. Dla czytelnika niebędącego specjalistą wniosek jest uderzający: nie tylko sam guz, lecz także tłuszcz bezpośrednio go otaczający może decydować o skuteczności immunoterapii. Skupiając się na tym tłuszczu — mierząc go, by ukierunkować decyzje terapeutyczne, albo celując w jego przekształcone komórki zrębu i sygnał CXCL12–CXCR4 — może być możliwe przekształcenie ochronnej tarczy guza w terapeutyczny słaby punkt.
Cytowanie: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, tłuszcz trzewny, immunoterapia, CXCL12 CXCR4