Clear Sky Science · pl
Przebudowa ER to cecha starzenia zależna od ER-fagii
Dlaczego wewnętrzne fałdy komórki mają znaczenie wraz z wiekiem
Komórki w naszych ciałach wypełnia labiryntowa sieć błonowa zwana siateczką śródplazmatyczną, albo ER. Ta struktura pomaga w tworzeniu tłuszczów i białek, zarządza cukrami i wapniem oraz nieustannie komunikuję się z innymi częściami komórki. Ponieważ przez tę sieć przechodzi tak wiele kluczowych zadań, długotrwałe przekształcenia ER mogą wpływać na to, jak starzeją się tkanki, jak odporne są na stres i ostatecznie — jak długo pozostajemy zdrowi. W tym badaniu zadano przewrotnie proste pytanie: czy sama ER starzeje się w określony, uporządkowany sposób, a jeśli tak, czy ta zmiana to jedynie szkodliwe zużycie, czy wbudowana strategia ochronna?
Ukryta zmiana na warsztacie komórkowym
Wykorzystując zaawansowane mikroskopy i znaczniki fluorescencyjne u małego robaka Caenorhabditis elegans, autorzy śledzili ER w żywych osobnikach, gdy przechodziły od młodej dorosłości do starości. W młodych komórkach ER tworzy szerokie, ułożone w stosy płaty obsadzone aparatami do syntezy białek, przypominające schludnie zorganizowane hale produkcyjne. W miarę starzenia się robaków te płaty kurczyły się objętościowo i ustępowały miejsca cieńszej, bardziej rurkowatej sieci zajmującej mniej miejsca. Pomiary wykazały, że całkowita zawartość ER spada znacząco, równocześnie zmieniając kształt, co wskazuje nie na przypadkowe uszkodzenia, lecz na skoordynowane zmniejszanie i rekonfigurację organelli.
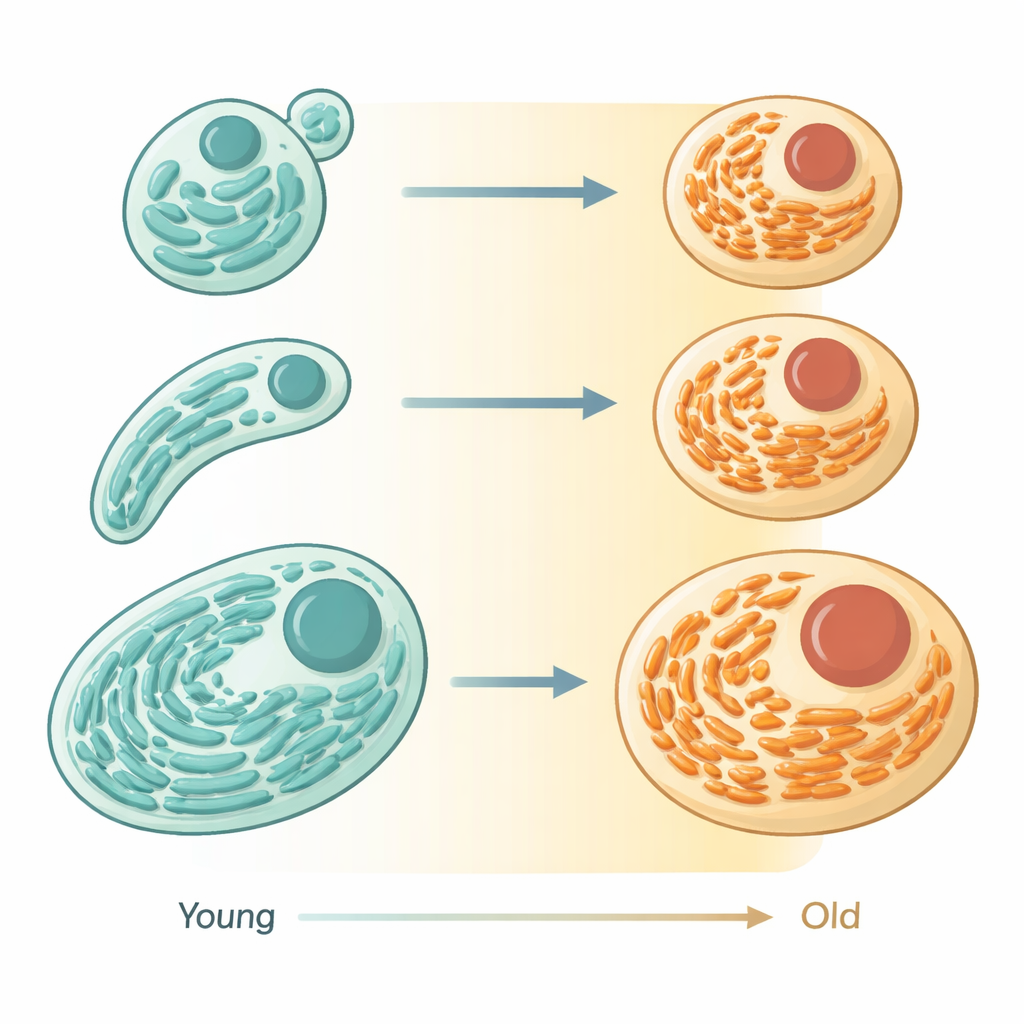
Od produkcji białek do gospodarowania tłuszczami
Kształt w biologii często sygnalizuje funkcję i tu również to się potwierdziło. Badacze porównali zmiany białek związanych z ER w czasie w różnych tkankach robaka. Białka zaangażowane w budowę, fałdowanie i kontrolę jakości innych białek malały z wiekiem, równolegle z utratą płatowego ER. W przeciwieństwie do tego wiele białek ER związanych z metabolizmem tłuszczów i błon pozostawało stabilnych lub nawet wzrastało. Te wzorce sugerują, że starzejące się komórki redukują masową produkcję białek i przekierowują zasoby ER na zarządzanie lipidami i błonami. Co istotne, analiza dużych zbiorów danych ze starzejących się myszy wykazała podobny obraz: białka ER związane z sekrecją i obróbką białek miały tendencję do spadku, podczas gdy te uczestniczące w metabolizmie lipidów i autofagii były względnie zachowane lub zwiększone.
Szlak recyklingu komórkowego napędzający przebudowę
Co napędza tę szeroko zakrojoną przebudowę? Zespół przypisał zmiany ER-fagii, formie selektywnego „zjadania” samego siebie, w której komórka pakuje fragmenty ER w pęcherzyki recyklingowe przeznaczone do rozkładu w lizosomach. Zablokowanie podstawowych genów autofagii u robaków powstrzymało normalną, związana z wiekiem utratę masy ER oraz przejście z płatów do rurek, pokazując że ten szlak recyklingu nie ogranicza się do sprzątania resztek, lecz aktywnie rzeźbi organellum. Niezależne eksperymenty u drożdży potwierdziły, że komponenty ER są przekierowywane do centrum recyklingu komórkowego wraz ze starzeniem się komórek, również w sposób zależny od autofagii. Mikroskopia elektronowa ujawniła fragmenty ER wewnątrz degradujących przegrodzeń, dostarczając fizycznego dowodu, że kawałki sieci są celowo usuwane.

Kontrola specyficzna dla tkanek wspólnego programu starzenia
Chociaż przebudowa ER była widoczna w wielu tkankach robaka — jelicie, hipodermie przypominającej skórę, mięśniach i neuronach — wyzwalacze okazały się specyficzne dla danej tkanki. W hipodermie wcześniej mało poznane białko błonowe o nazwie TMEM-131 powiązało obrót ER z obróbką kolagenu. Gdy TMEM-131 było zmniejszone, związana z wiekiem utrata ER w tej tkance została w dużej mierze zahamowana, co sugeruje, że ER jest pomniejszana, gdy maleje liczba jej „klientów” kolagenowych. W jelicie z kolei kluczowym regulatorem był odcinek IRE-1–XBP-1 odpowiedzi na niepofałdowane białka, centralny szlak wykrywający stres. Wyciszenie tej gałęzi sygnalizacyjnej zachowywało jelitowy ER podczas starzenia, co sugeruje, że w tym narządzie sygnalizacja stresu ER pomaga decydować, kiedy części ER powinny zostać poświęcone.
Przeprogramowanie ER dla dłuższego życia
Badanie łączy też przebudowę ER z długowiecznością. U robaków kilka dobrze poznanych interwencji wydłużających życie — osłabienie sygnałów podobnych do insuliny, obniżenie czujności odżywczej mTOR, usunięcie linii płciowej czy nieznaczne spowolnienie syntezy białek — wszystkie wywoływały zmniejszenie ER i zwiększenie sieci rurek wcześnie w dorosłości, zamiast czekać na starość. Co ważne, gdy ER-fagia była wyłączona, długie życie zwykle uzyskiwane przez hamowanie mTOR zarówno u drożdży, jak i robaków było wyraźnie skrócone lub znikało. Wskazuje to, że starannie kontrolowane przycinanie ER nie jest jedynie skutkiem ubocznym starzenia czy leczenia, lecz jednym z mechanizmów, dzięki którym komórki osiągają trwalszy stan.
Co to znaczy dla zdrowego starzenia
Dla laika utrata znacznej części kluczowej struktury komórkowej podczas starzenia może brzmieć wyłącznie szkodliwie. Praca ta kreśli jednak bardziej zniuansowany obraz. ER wydaje się być aktywnie przebudowywana — poprzez selektywne samozjadanie i regulację dostosowaną do tkanek — tak aby starzejące się komórki produkowały mniej nowych białek, inwestowały więcej w zarządzanie lipidami i błonami oraz możliwie zmniejszały ryzyko przewlekłego stresu. Ta przebudowa wydaje się być zachowana od drożdży po ssaki i jest wymagana dla co najmniej niektórych form wydłużenia życia. W dłuższej perspektywie jednak kurczenie się ER może pociągać za sobą kompromisy, wpływając na to, jak dobrze komórki naprawiają inne organelle i radzą sobie z późnym spadkiem sprawności. Ukazując ER-fagię i dynamikę ER jako podstawowe cechy normalnego i opóźnionego starzenia, badania te wskazują nowe dźwignie, które być może kiedyś będzie można wyregulować, by promować zdrowsze, bardziej odporne tkanki.
Cytowanie: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Słowa kluczowe: siateczka śródplazmatyczna, autofagia, starzenie komórkowe, homeostaza białek, metabolizm lipidów