Clear Sky Science · pl
Genomika funkcjonalna z rozdzielczością czasową przy użyciu głębokiego uczenia ujawnia globalną hierarchiczną kontrolę autofagii
Jak komórki się recyklingują — i jak wiedzą, kiedy przestać
Nasze komórki przetrwają trudne czasy, poddając własne elementy recyklingowi w procesie zwanym autofagią — dosłownie „samo‑zjadaniem”. Zbyt mało recyklingu powoduje gromadzenie uszkodzonych składników; zbyt dużo sprawia, że komórka kanibalizuje sama siebie. To badanie stawia pozornie proste pytanie o dużych konsekwencjach dla starzenia i chorób: jak żywa komórka włącza i wyłącza autofagię w odpowiednich momentach, gdy poziomy składników odżywczych rosną i maleją?
Śledzenie tysięcy komórek przez cykl od uczty do głodu
Aby to zbadać, naukowcy użyli drożdży piekarskich jako modelu i obserwowali niemal sześć tysięcy różnych mutantów podczas głodówki i powrotu do odżywienia. Każda linia drożdży miała fluorescencyjne znaczniki struktur zaangażowanych w autofagię, co pozwoliło mikroskopowi o dużej mocy rejestrować obrazy co godzinę, gdy składniki odżywcze były usuwane, a następnie przywracane. Zamiast ręcznie sortować te obrazy, zespół wytrenował algorytmy głębokiego uczenia, by rozpoznawały, kiedy komórka znajduje się w stanie autofagii — wyłącznie na podstawie cech obrazu, a nie ludzkiej oceny. To pozwoliło uzyskać precyzyjne przebiegi czasowe aktywności autofagii dla niemal całego genomu drożdży, ujawniając, jak szybko i jak mocno każdy mutant reagował na zmiany składników odżywczych. 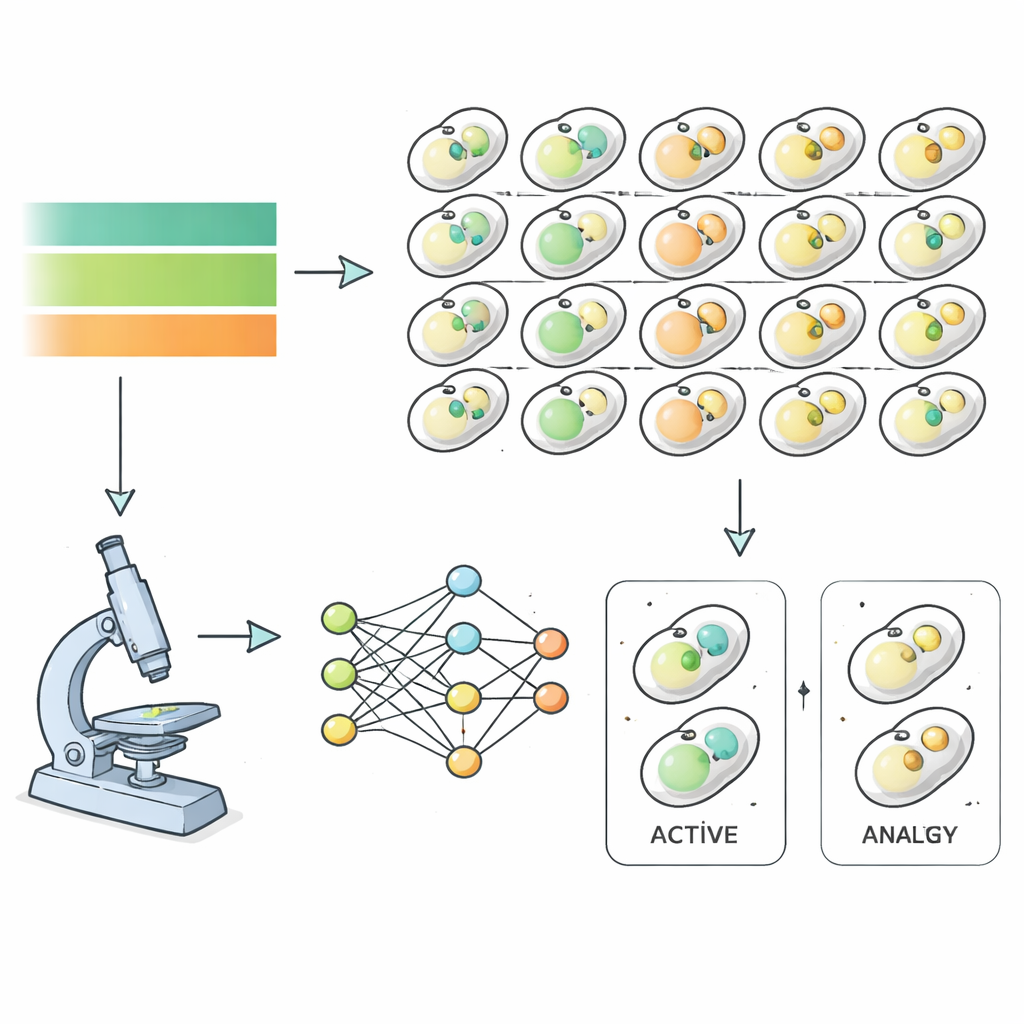
Sześć odrębnych sposobów, w jakie komórki źle radzą sobie z recyklingiem
Poprzez matematyczne dopasowanie tych przebiegów czasowych autorzy wyekstrahowali szczegółowe „kinetyczne odciski palców” dla każdego mutanta — jak szybko autofagia się włączała, jak długo utrzymywała się na wysokim poziomie i jak gwałtownie się wyłączała. Grupowanie tych sygnatur ujawniło sześć szerokich typów zachowań. Niektóre mutanty były „ultrawrażliwe”, reagując bardzo szybko na głodówkę i powrót składników odżywczych. Inne były „hipowrażliwe”, reagując ospale. Grupa „hiperaktywna” wykazywała nieprawidłowo wysokie podstawowe poziomy recyklingu, podczas gdy kilka grup miało różne stopnie niezdolności do uruchomienia właściwej odpowiedzi w ogóle. Co ważne, znane podstawowe geny autofagii znalazły się w najcięższych klasach, potwierdzając, że metoda wychwytuje prawdziwą biologię, a nie jedynie szum pomiarowy.
Mapowanie hierarchii kontroli nad autofagią
Autofagia nie zachodzi w izolacji; jest zintegrowana z szerszymi sieciami regulatorowymi komórki. Zespół nałożył swoje profile dynamiczne na duże mapy interakcji genetycznych i białkowych w drożdżach. Geny, których utrata powodowała silne defekty autofagii, miały tendencję do leżenia blisko znanego „rdzenia” maszynerii autofagicznej w tych sieciach, podczas gdy subtelniejsze mutanty znajdowały się dalej, co zgadza się z bardziej pośrednią kontrolą. Analizując, które procesy komórkowe były wzbogacone w każdej klasie zachowań, odkryli, że uruchamianie autofagii wywołane głodówką jest silnie kształtowane przez szlaki zajmujące się RNA, produkcją białek i metabolizmem energetycznym, natomiast wyłączanie autofagii po powrocie składników odżywczych zależy bardziej od ruchu błon i kroków fuzji, które oczyszczają pęcherzyki recyklingowe.
Przybliżenie: jak powstają i są usuwane pęcherzyki
Autofagia przebiega przez dwa główne etapy: budowę pęcherzyków wypełnionych ładunkiem, a następnie ich fuzję z komórkową komorą recyklingową celem rozkładu. Aby rozdzielić te etapy, badacze eksplorowali „przestrzeń utajoną” wewnątrz swojej sieci neuronowej — skompresowaną reprezentację, której używa do rozróżniania obrazów. Rzutując tę wewnętrzną reprezentację na mapę dwuwymiarową, mogli obserwować, jak populacje komórek przesuwają się z obszaru bez pęcherzyków, przez obszar z wieloma wolnymi pęcherzykami, aż do regionu, gdzie pęcherzyki zostały oczyszczone. Korzystając z porównań statystycznych względem referencyjnych mutantów zablokowanych na różnych etapach, policzyli dla każdego genu, czy głównie wpływał na formowanie pęcherzyków, ich usuwanie, czy na oba procesy. Ta analiza wykazała, że kontrola formowania pęcherzyków jest wysoce wrażliwa na poziomy azotu w czasie, podczas gdy mechanizmy usuwania zachowują się bardziej stabilnie i często stanowią główne ograniczenie ogólnego przepływu recyklingu. 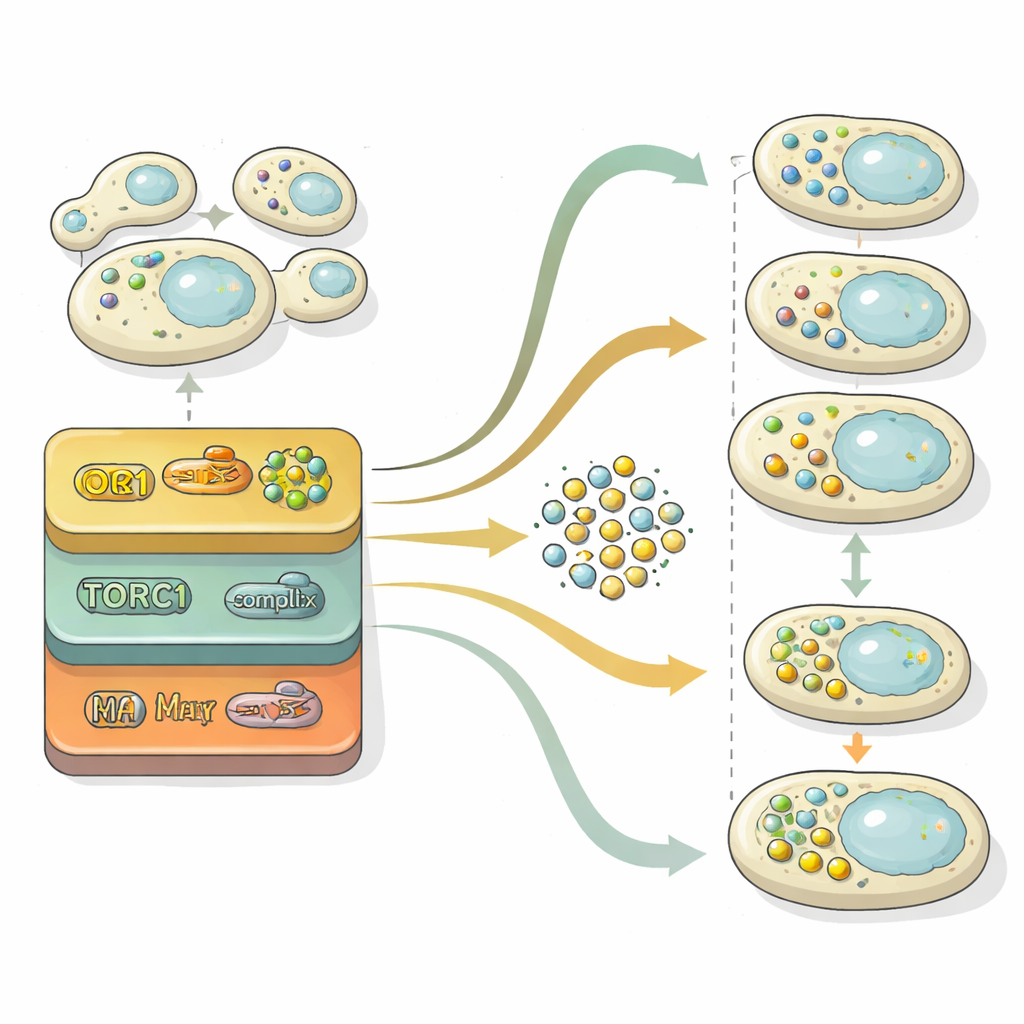
Ukryty hamulec recyklingu: droga retrogradacyjna
Jednym z najbardziej uderzających odkryć była tzw. droga retrogradacyjna (RTG), przenosząca sygnały z mitochondriów do jądra. Komórki drożdżowe pozbawione składników RTG wytwarzały zbyt wiele autofagosomów nawet gdy składników odżywczych było pod dostatkiem i miały trudności z ich oczyszczeniem po przywróceniu odżywienia. Szczegółowe eksperymenty pokazały, że ta ścieżka kontroluje ekspresję kluczowych genów autofagii, szczególnie nadrzędnego inicjatora ATG1, w dużej mierze niezależnie od znanego czujnika składników odżywczych TORC1, będącego celem leków takich jak rapamycyna. W praktyce sygnalizacja RTG działa jak hamulec zmieniający się w czasie, który zapobiega wymykającej się spod kontroli autofagii w bogatych warunkach i pomaga zakończyć odpowiedź, gdy warunki się poprawiają.
Dlaczego to ma znaczenie dla zdrowia i terapii
W sumie ta praca dostarcza mapy na poziomie genomu i z rozdzielczością czasową, jak komórki regulują autofagię w zmieniających się warunkach odżywczych. Ukazuje, że uruchamianie i zatrzymywanie autofagii nie są lustrzanymi odbiciami: znacznie więcej genów wpływa na to, jak zaczyna się recykling, niż na to, jak się kończy, a długoterminowa równowaga zależy w dużym stopniu od usuwania pęcherzyków i hamulców transkrypcyjnych, takich jak szlak RTG. Dla czytelnika ogólnego kluczowy wniosek jest taki, że samokanibalizm komórkowy podlega wielowarstowej, hierarchicznej kontroli i że teraz możemy szczegółowo odwzorować te warstwy. Taka perspektywa systemowa może w przyszłości umożliwić bardziej wyrafinowane terapie, które modulują autofagię w określonych fazach — wzmacniając korzystny recykling bez wywoływania szkodliwych skutków przewlekłego, niekontrolowanego trawienia wewnętrznego.
Cytowanie: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Słowa kluczowe: autofagia, głębokie uczenie, genetyka drożdży, detekcja składników odżywczych, recykling komórkowy