Clear Sky Science · pl
Wyrafinowane fenotypowanie odpowiedzi na szczepionki ujawnia transkryptomiczne determinanty heterogeniczności przeciwciał neutralizujących
Dlaczego niektóre szczepionki działają lepiej u niektórych osób
Kiedy zaciągamy rękaw, aby przyjąć zastrzyk przeciw COVID-19, możemy założyć, że układ odpornościowy wszystkich reaguje tak samo. W rzeczywistości ludzie bardzo różnią się szybkością i siłą wytwarzania ochronnych przeciwciał. To badanie śledziło dorosłych, którzy otrzymali inaktywowane szczepionki przeciw SARS-CoV-2 i pokazuje, że odpowiedzi na szczepionkę układają się w wyraźne wzorce, z których każdy napędzany jest przez różne wczesne sygnały odpornościowe zapisane w naszych genach i komórkach krwi. Zrozumienie tych wzorców może pewnego dnia pomóc dopasować harmonogramy szczepień tak, aby każdy otrzymał potrzebną ochronę.
Trzy drogi do ochrony po tym samym zastrzyku
Naukowcy śledzili 73 zdrowych dorosłych, którzy otrzymali dwie dawki inaktywowanej szczepionki przeciw COVID-19. Mierzyli przeciwciała neutralizujące — te, które mogą blokować wirusa — przed szczepieniem, tydzień po drugiej dawce i ponownie około miesiąca później. Zamiast prostego podziału na „wysokich” i „niskich” responderów, zastosowali metody oparte na danych, aby pogrupować osoby według tego, jak zmieniały się ich poziomy przeciwciał w czasie. Pojawiły się trzy wyraźne wzorce: grupa „nisko-opóźniona” z powolnym, umiarkowanym wzrostem przeciwciał; grupa „szybko-stabilizująca się”, której poziomy przeciwciał gwałtownie wzrosły, a następnie się ustabilizowały; oraz grupa „ciągłego wzrostu”, w której poziomy przeciwciał rosły dalej aż do najwyższych wartości. Te wzorce nie były wyjaśnione wiekiem, płcią ani masą ciała, a tylko częściowo tym, którą markę inaktywowanej szczepionki otrzymano.
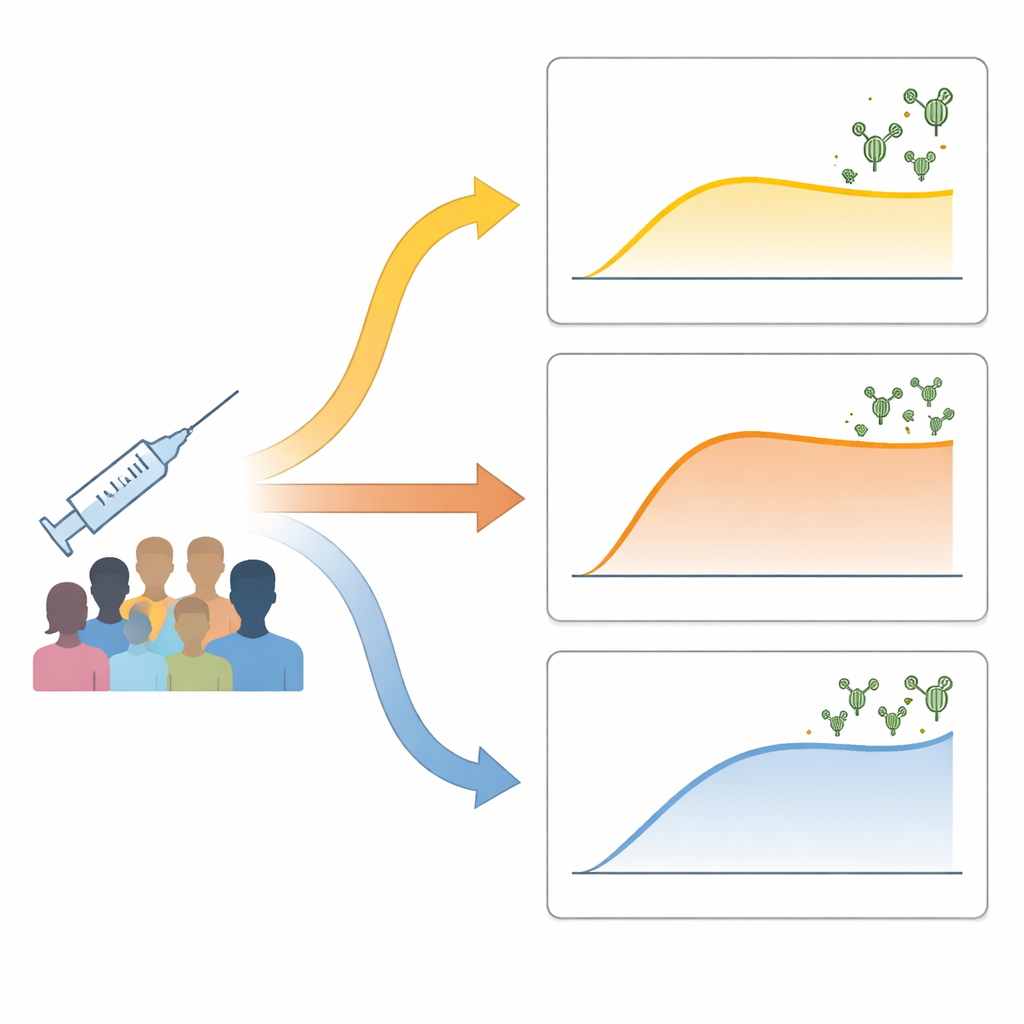
Jak wczesna aktywność odpornościowa kształtuje wynik
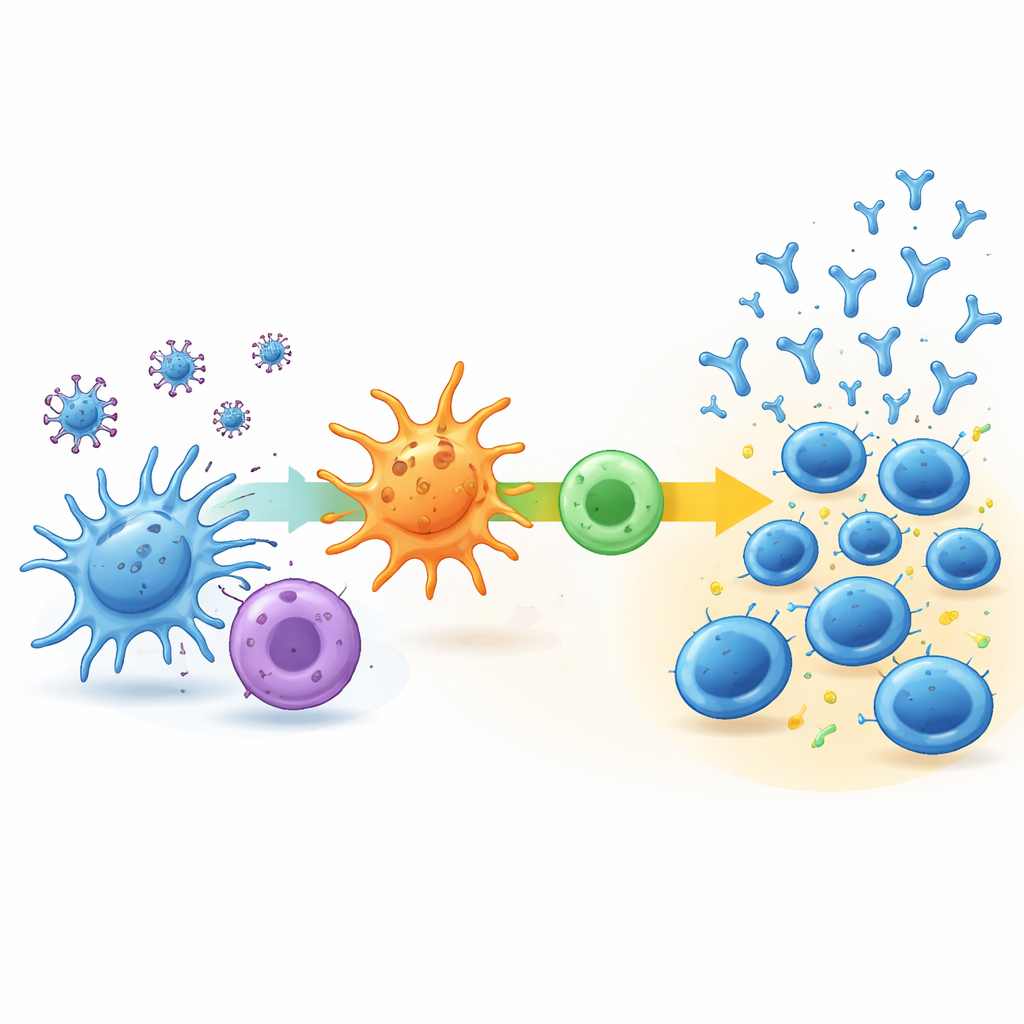
Aby dowiedzieć się, co napędza te różne ścieżki, zespół przeanalizował aktywność genów w komórkach odpornościowych we krwi na początku i tydzień po drugiej dawce. W grupie nisko-opóźnionej bardzo niewiele się zmieniło: kluczowe szlaki odpornościowe ledwo się włączały, a skład typów komórek odpornościowych we krwi pozostał w dużej mierze niezmieniony. W przeciwieństwie do tego, grupy szybko-stabilizująca się i ciągłego wzrostu wykazywały wyraźne oznaki wczesnej aktywacji odporności. W najsilniejszych responderach zaobserwowano skoordynowaną aktywność w szlakach przetwarzających fragmenty wirusa, prezentujących je innym komórkom odpornościowym oraz wspierających typ komórek T pomocniczych, który jest znany z wzmacniania produkcji przeciwciał. Osoby te miały też skłonność do większej liczby naiwnych komórek B i komórek T pomocniczych gotowych do reakcji, a później wykazywały nieco silniejszą specyficzną dla wirusa aktywność komórek T.
Ukryte warstwy kontroli w RNA i komórkach B
Ponad prostymi zmianami włączania i wyłączania genów, naukowcy przyjrzeli się subtelniejszym warstwom regulacji osadzonym w RNA, pośrednich cząsteczkach między DNA a białkiem. W grupie o najwyższej odpowiedzi geny odpornościowe zaangażowane w prezentowanie fragmentów wirusa ukazywały różne wzorce „splicingu” i krótsze regiony ogonowe na końcu swoich cząsteczek RNA. Uważa się, że te cechy ułatwiają komórkom produkcję określonych białek i utrzymanie silnego sygnalizowania. Zespół zrekonstruował także repertuar receptorów komórek B — unikalnych anten na komórkach produkujących przeciwciała — z tych samych próbek krwi. Choć ogólna różnorodność wydawała się podobna we wszystkich grupach, każdy wzorzec odpowiedzi używał nieco innych kombinacji i kształtów tych receptorów, a najsilniejsi responderzy preferowali typy receptorów wcześniej powiązane z potężnymi przeciwciałami przeciw białku kolca koronawirusa.
Wykrywanie prawdopodobnych niskich responderów przed szczepieniem
Ponieważ osoby z grupy nisko-opóźnionej mogą być mniej chronione po standardowym schemacie szczepień, badacze zapytali, czy możliwe byłoby ich wcześniejsze wykrycie. Skoncentrowali się na małym zestawie genów, które różniły się nieznacznie na początku między najsłabszymi a najsilniejszymi responderami. Przy użyciu metod uczenia maszynowego zbudowali model oparty na aktywności zaledwie ośmiu genów mierzonych przed szczepieniem. Model ten potrafił rozróżnić nisko-opóźnionych responderów z wysoką dokładnością w ich zbiorze danych, przy czym dwa geny zaangażowane w podstawowe sygnalizowanie komórkowe i zapalenie wnosiły największy wkład w moc predykcyjną. Chociaż wyniki te trzeba przetestować w większych i bardziej zróżnicowanych grupach, sugerują, że proste badanie krwi mogłoby pewnego dnia kierować bardziej spersonalizowanymi planami szczepień.
Co to oznacza dla przyszłych szczepionek
Ogólnie rzecz biorąc, to badanie pokazuje, że ludzie nie wykazują po prostu „silnych” lub „słabych” odpowiedzi przeciwciałowych; podążają różnymi przebiegami czasowymi ukształtowanymi przez wczesne, trudne do zauważenia wydarzenia odpornościowe. Najbardziej chronione osoby włączają skoordynowane sieci genów i komórek, które pomagają im szybko rozpoznać szczepionkę i zbudować trwałe przeciwciała, podczas gdy słabo reagujący wykazują stłumioną wczesną reakcję. Mapując te wewnętrzne różnice i budując narzędzia do przewidywania, kto zareaguje słabo, praca tworzy podstawy dla spersonalizowanych szczepień — na przykład wcześniejszych dawek przypominających lub alternatywnych formuł dla osób zagrożonych — tak aby korzyści ze szczepionek były bardziej równomiernie rozdzielone.
Cytowanie: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Słowa kluczowe: odpowiedzi na szczepionki, przeciwciała neutralizujące, szczepienia przeciw COVID-19, heterogeniczność układu odpornościowego, spersonalizowane szczepionki