Clear Sky Science · pl
Immunogenność i ochrona kandydatów na szczepionkę przeciw grypie ośmioskładnikową z użyciem adiuwantowanych białek lub mRNA‑LNP u myszy nieimmunizowanych
Dlaczego lepszy zastrzyk przeciw grypie ma znaczenie
Sezonowe szczepionki przeciw grypie ratują wiele żyć, ale ich skuteczność może znacznie się różnić w zależności od roku. Jednym z powodów jest to, że obecne szczepionki głównie uczą układ odpornościowy rozpoznawać jeden białkowy cel wirusa, przez co inne użyteczne cele są mniej wykorzystywane. To badanie na myszach bada szczepionki nowej generacji, które uczą układ odpornościowy rozpoznawać jednocześnie dwa kluczowe białka wirusa, i porównuje tradycyjne podejście oparte na białkach z nowszą technologią mRNA podobną do tej użytej w ostatnich szczepionkach przeciw COVID‑19.
Dwa cele zamiast jednego
Obecne szczepionki przeciw grypie skupiają się głównie na hemaglutyninie, czyli HA, białku ułatwiającym wirusowi przyłączanie się do naszych komórek. Badacze dodali drugie białko wirusowe, neuraminidazę, czyli NA, która pomaga wirusowi uwalniać się z zakażonych komórek i rozprzestrzeniać. Łącząc cztery warianty HA i cztery warianty NA pochodzące ze szczepów sezonowych z lat 2018–2019, zbudowali „ośmioskładnikową” szczepionkę mającą objąć dwa typy wirusa A i dwie linie wirusa B. Następnie zapakowali te osiem składników na dwa różne sposoby: jako oczyszczone białka zmieszane ze składnikiem wzmacniającym odporność oraz jako mRNA otoczone drobnymi lipidowymi pęcherzykami (mRNA‑LNP), które pobudzają komórki organizmu do wytwarzania białek wirusowych.
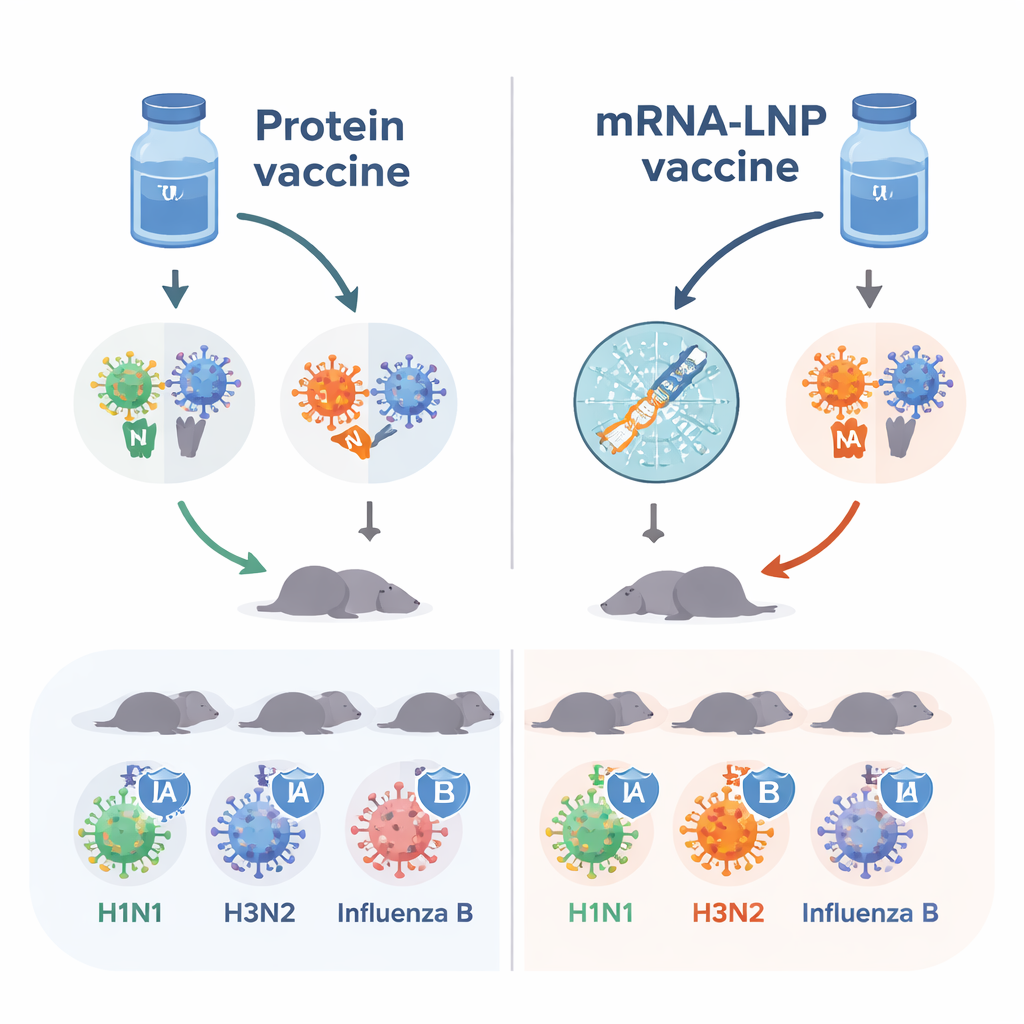
Silniejsze odpowiedzi przeciwciał z mRNA
Myszy nieimmunizowane — zwierzęta, które nigdy nie miały kontaktu z wirusami grypy ani szczepionkami — otrzymały dwie dawki albo szczepionki proteinowej, albo wersji mRNA‑LNP. Zespół mierzył przeciwciała rozpoznające HA i NA we krwi. Obie szczepionki wywołały przydatne odpowiedzi, ale szczepionki mRNA‑LNP konsekwentnie wytwarzały wyższe poziomy przeciwciał przeciw większości składników HA i NA. W szczególności przeciwciała hamujące aktywność NA, które niezależnie przyczyniają się do ochrony, były zazwyczaj silniejsze po szczepieniu mRNA‑LNP. Wyniki te sugerują, że przynajmniej w tym modelu zwierzęcym platforma mRNA sprawia, że te same cele wirusowe są bardziej widoczne dla układu odpornościowego.
Ochrona przed zgodnymi i aktualnymi szczepami
Prawdziwym testem było to, czy te szczepionki potrafią uchronić myszy przed ciężką chorobą. Przy dawkach przeskalowanych tak, by być zbliżonymi do ludzkiej szczepionki przeciw grypie, oba formaty szczepionek w pełni chroniły zwierzęta przed śmiertelną infekcją wirusami H1N1 i grypy B, które były blisko dopasowane do składników szczepionki, a także przed inżynierowanymi wirusami podobnymi do H3N2 stosowanymi, gdy standardowe szczepy ludzkie nie wywołują choroby u myszy. Zaszczepione myszy utrzymywały masę ciała i przeżywały, podczas gdy niezabezpieczone zwierzęta traciły na wadze i często umierały. Dla tych blisko spokrewnionych szczepów tradycyjne szczepionki proteinowe i szczepionki mRNA‑LNP wykazały podobną skuteczność pod względem przeżywalności, mimo że szczegóły odpowiedzi przeciwciał różniły się.
Przewaga wobec starszych, niedopasowanych wirusów grypy
Tam, gdzie podejście mRNA‑LNP wyróżniało się, były trudniejsze testy „niedopasowania”. Badacze wystawili zaszczepione myszy na historyczne szczepy H3N2 z lat 1968, 1975 i 1982 — wirusy różniące się od współczesnych szczepów, które miała naśladować szczepionka. Wszystkie niezabezpieczone myszy i większość zwierząt zaszczepionych szczepionkami proteinowymi zmarły, ale każda mysz, która otrzymała ośmioskładnikową szczepionkę mRNA‑LNP, przeżyła, mimo że nadal wykazywała objawy choroby. Ta przewaga w przeżyciu utrzymywała się prawie rok po szczepieniu, co wskazuje na długotrwałą ochronę. Gdy zespół przekazał surowicę krwi od zaszczepionych zwierząt do myszy niezabezpieczonych, tylko surowica zawierająca przeciwciała wzbudzone przez szczepionki mRNA‑LNP przeciw HA chroniła przed śmiercią po zakażeniu niedopasowanym wirusem, co wskazuje, że przeciwciała HA o reaktywności krzyżowej są kluczowym czynnikiem.
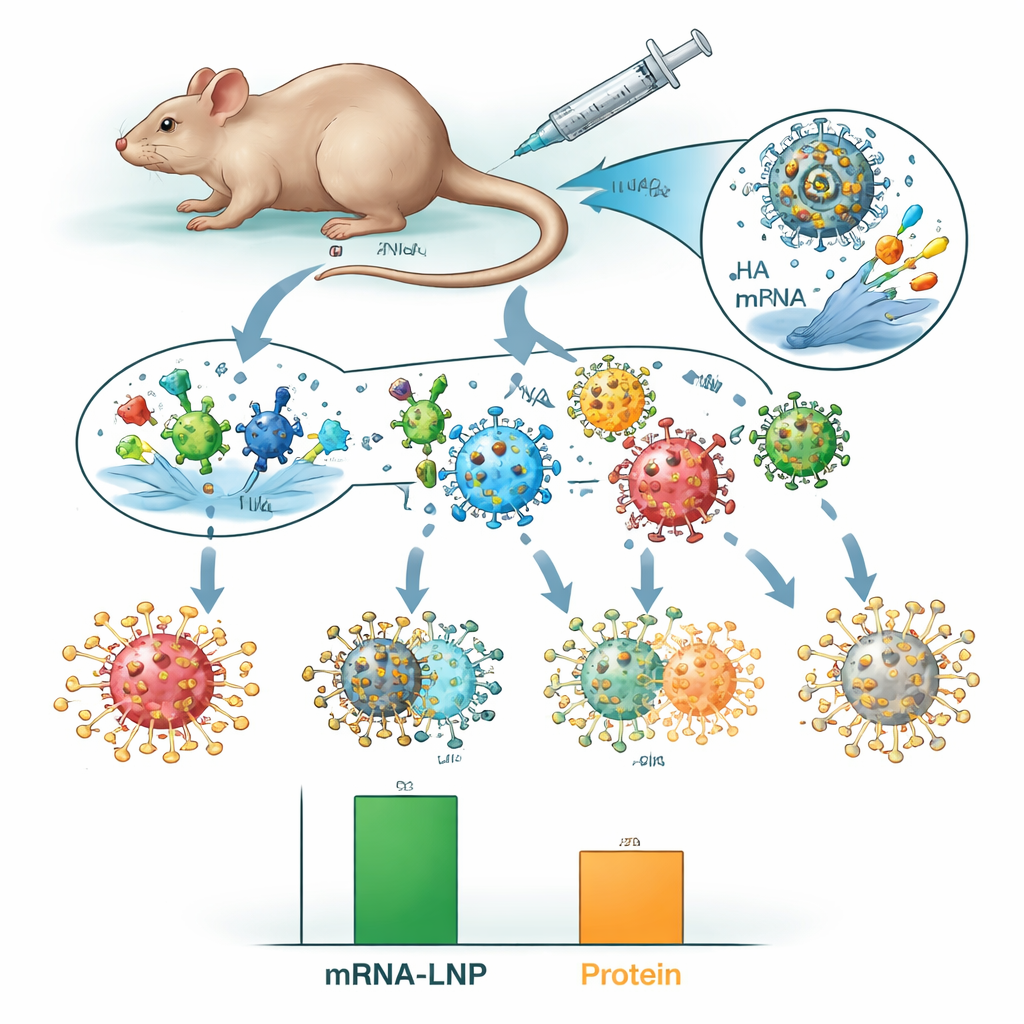
Co to oznacza dla przyszłych szczepionek przeciw grypie
Dla osoby niebędącej specjalistą przesłanie jest takie, że oba style szczepionek chroniły myszy przed rodzajami szczepów grypy, do których były zaprojektowane, ale wersja mRNA‑LNP oferowała też szerszą i dłużej utrzymującą się ochronę przed starszymi, nieaktualnymi wirusami. Poprzez uwzględnienie obu głównych białek powierzchniowych grypy i zastosowanie mRNA do ich prezentacji układowi odpornościowemu, ta strategia może pomóc zmniejszyć różnice między dobrymi i słabymi sezonami grypowymi. Chociaż wyniki na myszach nie gwarantują sukcesu u ludzi, a mocniejsze adiuwanty mogłyby nadal poprawić szczepionki proteinowe, praca wspiera pomysł, że wieloskładnikowe szczepionki mRNA przeciw grypie mogą pewnego dnia zapewnić bardziej niezawodną ochronę wobec szerszego zakresu krążących i pojawiających się szczepów grypy.
Cytowanie: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Słowa kluczowe: szczepionka przeciw grypie, mRNA‑LNP, hemaglutynina, neuraminidaza, ochrona krzyżowa