Clear Sky Science · pl
Adiuwant potęgujący przekrojową prezentację antygenu w szczepionkach przeciwnowotworowych dla ekspansji komórek T i synergii z anty‑PD‑1
Przekształcanie układu odpornościowego w precyzyjnego zabójcę nowotworów
Szczepionki przeciwnowotworowe często opisuje się jako uczące układ odpornościowy rozpoznawania i niszczenia guzów, ale w praktyce rzadko spełniały tę obietnicę. W tym badaniu zbadano nowy sposób „wzmocnienia” takich szczepionek, aby generowały silniejsze, dłużej utrzymujące się cytotoksyczne komórki T i lepiej współdziałały z popularnymi lekami immunoterapeutycznymi, takimi jak anty–PD‑1. Dla czytelników zainteresowanych tym, jak przyszłe terapie przeciwnowotworowe mogą łączyć leki biologiczne, szczepionki i inżynierię układu odpornościowego, praca ta daje wgląd w to, jak może wyglądać następna generacja wysoko ukierunkowanej immunoterapii.
Dlaczego szczepionki przeciwnowotworowe potrzebują lepszego wsparcia
Terapeutyczne szczepionki przeciwnowotworowe nie mają na celu zapobiegania chorobie, lecz leczenie osób z już istniejącymi guzami poprzez wywołanie silnych, swoistych odpowiedzi odpornościowych przeciw nowotworom. Kluczowymi wykonawcami są komórki CD8, „zabójcze” limfocyty T, które potrafią rozpoznać i zniszczyć komórki nowotworowe prezentujące charakterystyczne antygeny. Niestety antygeny nowotworowe słabo stymulują, ponieważ zwykle przypominają zmienione wersje własnych białek organizmu. Ciągła ekspozycja podczas rozwoju nowotworu może też prowadzić do wyczerpania lub tolerancji komórek T, osłabiając działanie szczepionek. Aby temu przeciwdziałać, szczepionki muszą być łączone z adiuwantami — pomocniczymi składnikami, które pobudzają odporność wrodzoną, poprawiają prezentację antygenu i budują dużą, odporną pulę swoistych dla guza komórek T.
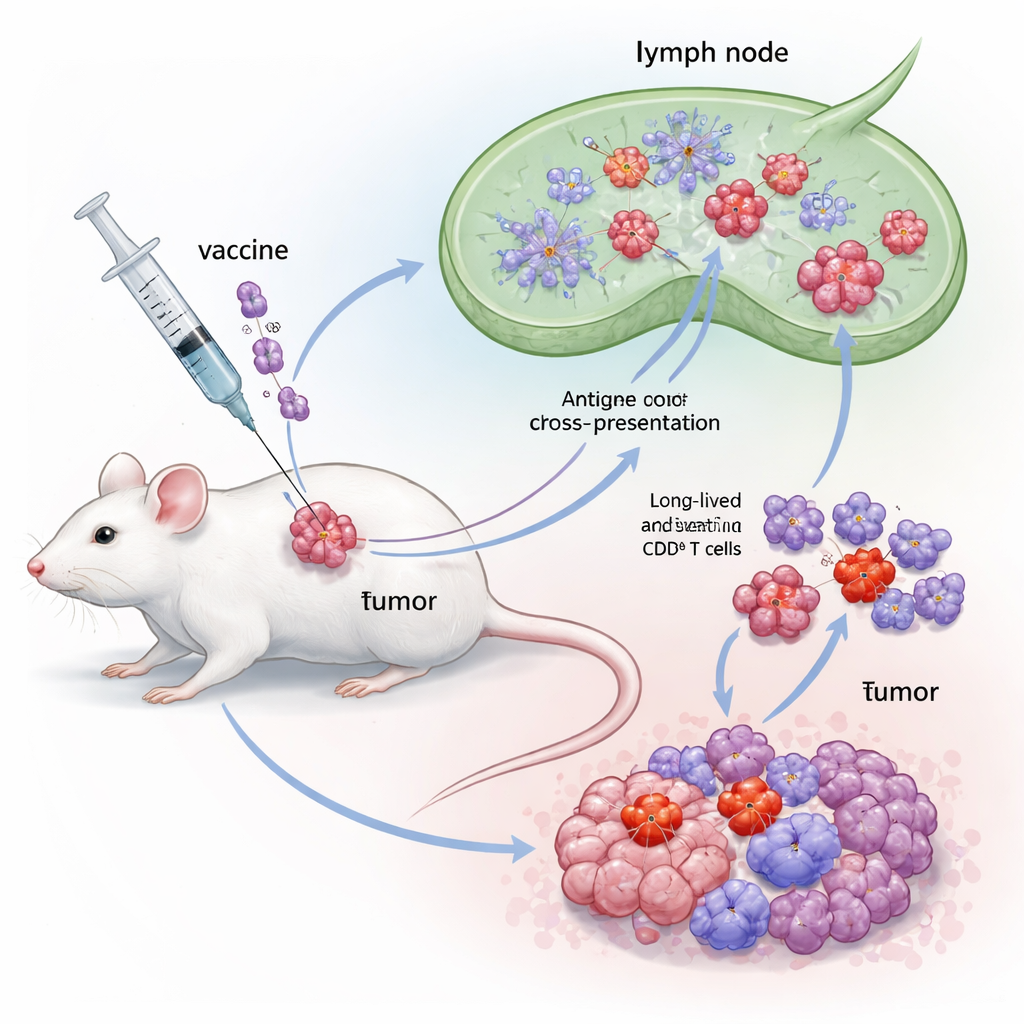
Hybrydowy wzmacniacz odporności zbudowany z dwóch silnych sygnałów
Naukowcy zaprojektowali hybrydowy adiuwant o nazwie Flt3L‑FlaB, w skrócie FB, przez połączenie dwóch cząsteczek stymulujących odporność w jeden białkowy fuzjat. Jedna część, Flt3L, to naturalny czynnik wzrostu, który rozszerza wyspecjalizowaną grupę komórek dendrytycznych znanych jako cDC1. Komórki te doskonale radzą sobie z „przekrojową prezentacją” — pobieraniem fragmentów materiału nowotworowego i pokazywaniem ich komórkom CD8 w sposób wywołujący silne odpowiedzi. Druga część, FlaB, to fragment bakteryjnej flageliny aktywujący receptor wrodzony TLR5 i działający jako silny sygnał niebezpieczeństwa. Poprzez połączenie ich autorzy chcieli zarówno zwiększyć liczbę cDC1, jak i przełączyć je w wysoce aktywny stan, poprawiając sposób prezentacji antygenów nowotworowych komórkom T oraz wydłużając czas trwania tej stymulacji.
Testowanie nowego adiuwanta w modelach guzów
Aby przetestować FB, zespół użył dobrze ugruntowanego mysiego modelu nowotworowego opartego na komórkach zaprojektowanych tak, by nosić onkoproteiny wirusa brodawczaka ludzkiego (HPV). Myszy najpierw otrzymały mały wszczep guza, a następnie terapeutyczną szczepionkę zawierającą antygen E7 z HPV, podawaną w połączeniu albo z samym Flt3L, albo z samą FlaB, albo z nową fuzją FB. Wszystkie szczepionki podawano w okolicy guza. Podczas gdy każdy z pojedynczych adiuwantów nieco spowalniał wzrost guza, szczepionka oparta na FB wyróżniała się: znacząco opóźniała progresję guza, wydłużała przeżycie i pozostawiła znaczącą część myszy całkowicie wolnych od guza. Analizy immunologiczne wykazały, że szczepienie FB wygenerowało niezwykle silne odpowiedzi komórek CD8 specyficznych dla E7 we krwi, w węzłach chłonnych i w śledzionie, z wysokimi poziomami interferonu‑gamma i intensywną proliferacją komórek T — dowód na to, że fuzja robiła więcej niż proste sumowanie efektów obu składników.
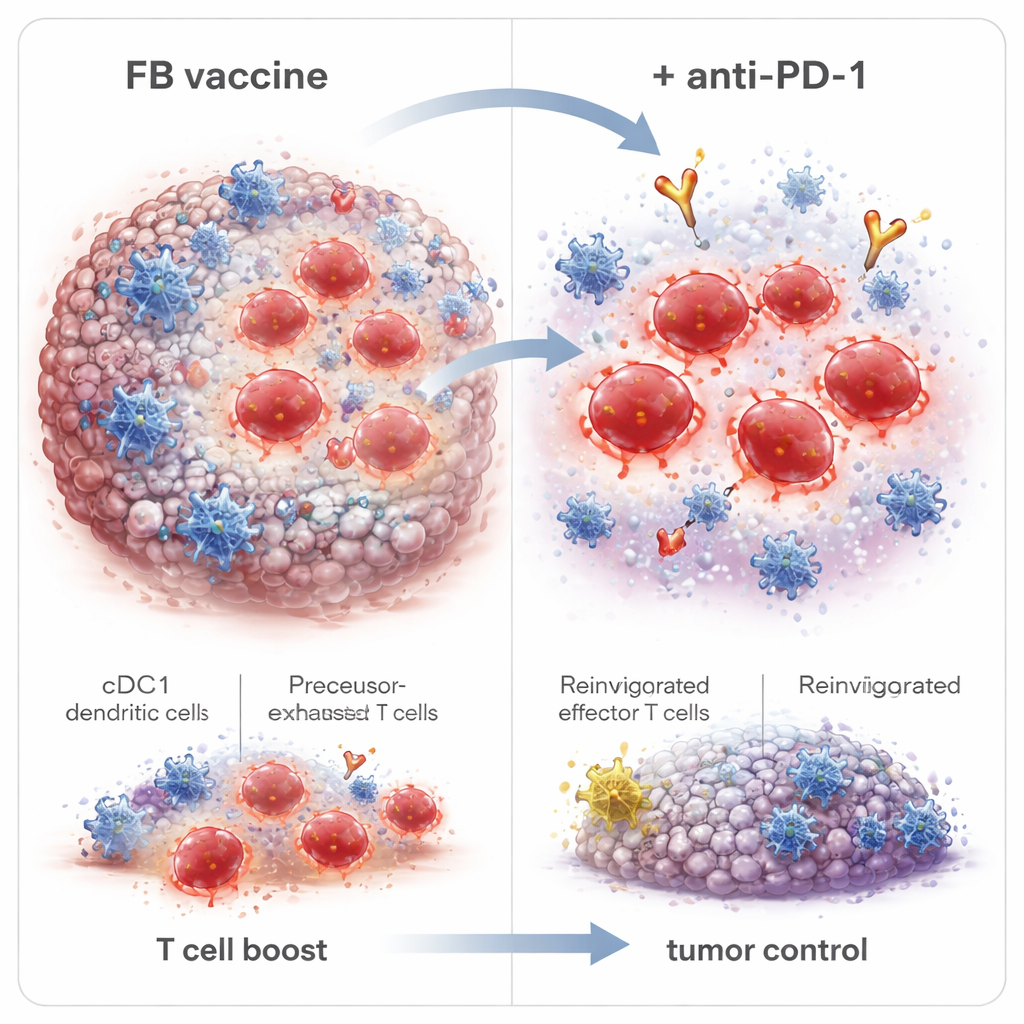
Budowanie trwałej pamięci odpornościowej i lepszy partner dla anty–PD‑1
Wnikliwsze analizy wykazały, że FB zmieniał nie tylko liczbę pojawiających się komórek CD8, ale też ich typy. Zwiększał odsetek krótkotrwałych efektorów atakujących guzy natychmiast, jak również komórek prekursorowych pamięci i komórek o cechach „pniowych” pamięci, które mogą przetrwać i ponownie odpowiedzieć w przyszłości. Co ważne, FB także rozszerzał populację tak zwanych prekursorowych komórek wyczerpanych (Tpex) w guzach — komórek stojących na granicy między wyczerpaniem a pełną aktywnością, szczególnie responsywnych na leki anty–PD‑1. Gdy myszy, które wyczyściły guzy, zostały po długim czasie poddane wyzwaniu wysoką dawką komórek nowotworowych, większość powstrzymała odrost, co dowodzi trwałej pamięci odpornościowej. Zablokowanie wychodzenia komórek odpornościowych z węzłów chłonnych znosiło korzyści FB, wskazując, że komórki T zabijające guz były inicjowane w tych węzłach przez cDC1, a następnie migrowały do guza.
Mocniejsi razem: szczepionki plus blokada punktów kontroli
Ponieważ terapia anty–PD‑1 działa najlepiej, gdy istnieje już pula responsywnych komórek T, zespół połączył szczepienie z adiuwantem FB z przeciwciałem anty–PD‑1. W modelu guza HPV dodanie anty–PD‑1 do szczepienia FB jeszcze bardziej spowolniło wzrost guza, zwiększyło liczbę myszy, które całkowicie oczyściły guzy, i zapewniło pełną ochronę przed bardzo wysokodawkowym ponownym wyzwaniem nowotworowym. Precyzyjne dobranie czasu miało znaczenie: rozpoczęcie terapii anty–PD‑1 po drugiej, a nie po pierwszej dawce szczepionki, nieco poprawiło całkowite eliminowanie guzów, zgodnie z ideą poczekania, aż populacje Tpex się rozrosną. Adiuwant FB poprawiał też odpowiedzi na szczepionki peptydowe, w tym na swoiste dla guza neoantygeny w modelu raka jelita grubego, co sugeruje, że ta strategia może mieć szerokie zastosowanie poza chorobami związanymi z HPV.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że praca ta dopracowuje sposób „uczenia” układu odpornościowego walki z rakiem. Poprzez połączenie czynnika wzrostu komórek dendrytycznych z silnym sygnałem niebezpieczeństwa w jednym, stabilnym białku, adiuwant FB tworzy więcej właściwych komórek prezentujących antygen, pomaga im skuteczniej prezentować antygeny nowotworowe i kształtuje populację komórek T zabójczych, które są zarówno potężne teraz, jak i gotowe odpowiedzieć później na terapię punktami kontrolnymi. Choć rezultaty uzyskano w myszach i przed wprowadzeniem do użycia u ludzi pozostało wiele kroków, badanie wyznacza jasną mapę drogową: inteligentniejsze adiuwanty, które koordynują przekrojową prezentację i „pniowość” komórek T, mogą uczynić terapeutyczne szczepionki przeciwnowotworowe znacznie silniejszym partnerem dla leków takich jak anty–PD‑1, co potencjalnie prowadzi do głębszej i dłużej utrzymującej się kontroli nad guzami u pacjentów.
Cytowanie: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Słowa kluczowe: szczepionki przeciwnowotworowe, immunoterapia, komórki dendrytyczne, blokada PD‑1, nowotwory związane z HPV