Clear Sky Science · pl
Pokonanie oporności na inhibitory kinazy tyrozynowej związanej z naczyniową niszą w ostrej białaczce szpikowej poprzez inhibicję miR-126
Dlaczego to ma znaczenie dla pacjentów z rakiem
Ostra białaczka szpikowa (AML) jest jednym z najbardziej agresywnych nowotworów krwi, a mimo nowoczesnych leków celowanych wielu pacjentów doświadcza nawrót choroby. To badanie stawia pozornie proste pytanie o dużych implikacjach: czy część problemu tkwi nie tylko w samych komórkach nowotworowych, lecz także w „sąsiedztwie”, w którym żyją w szpiku kostnym? Budując szczegółowy model komputerowy oparty na danych z laboratorium, autorzy badają, w jaki sposób drobne naczynia krwionośne mogą osłaniać komórki macierzyste białaczki przed lekami — i jak zablokowanie jednego małego sygnału RNA może zniszczyć tę ochronę.
Ukryte schronienie w szpiku
AML rozwija się w szpiku kostnym, gdzie złośliwe komórki blastyczne wypierają prawidłową produkcję krwi. Wśród tej masy ukrywa się mniejsza populacja komórek macierzystych białaczki, które potrafią samoodnawiać się i przetrwać leczenie, dając początek nawrotom. Te komórki macierzyste nie unoszą się swobodnie; wchodzą w specjalne zakamarki wokół małych tętnic i naczyń włosowatych, zwane łącznie niszą naczyniową. Badanie koncentruje się na pacjentach, których komórki białaczkowe niosą mutacje FLT3-ITD, leczenie których obejmuje inhibitory kinazy tyrozynowej (TKI). Chociaż leki te mogą znacząco zmniejszyć masę guza, wielu pacjentów i tak doświadcza nawrotu, co sugeruje, że niektóre komórki są ukrywane lub chronione.
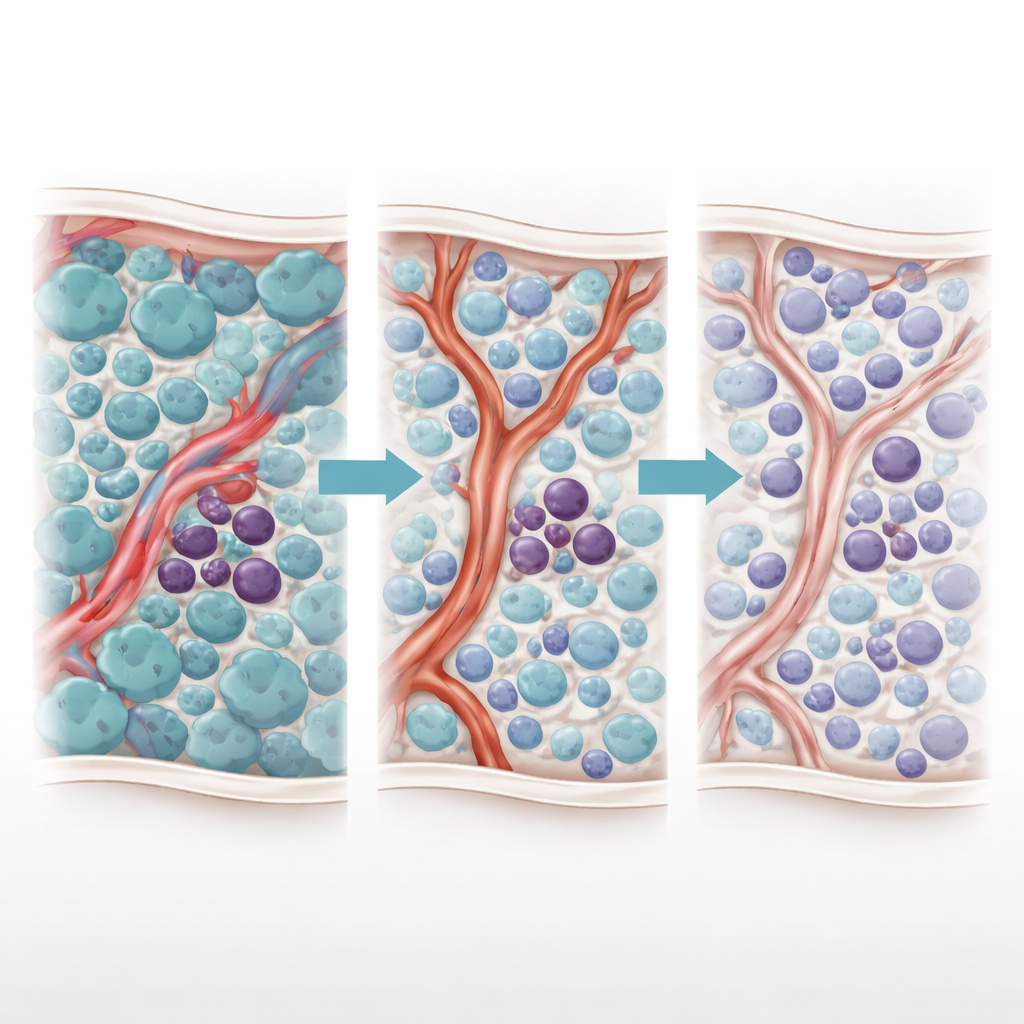
Dwoista reakcja na leczenie
Autorzy wcześniej odkryli zagadkowe „zjawisko Janusa” — dwoistą odpowiedź na terapię TKI. W miarę jak TKI zabijają szybko dzielące się komórki blastyczne, poziomy cząsteczki zapalnej TNF-α spadają. Ten spadek niespodziewanie pozwala pobliskim komórkom śródbłonka naczyń zwiększyć produkcję małego regulatorowego RNA o nazwie miR-126. miR-126 jest przekazywany z komórek śródbłonka do komórek macierzystych białaczki, skłaniając je do stanu cichego, niewchodzącego w cykl komórkowy, co czyni je wysoce opornymi na leki. Innymi słowy, samo leczenie, które usuwa większość komórek nowotworowych, przebudowuje szpik kostny w sposób, który chroni najniebezpieczniejsze komórki.
Budowa wirtualnego szpiku
Aby rozłożyć tę dynamikę na czynniki, zespół stworzył model obliczeniowy oparty na agentach, odwzorowujący szpik kostny w AML. Każdy kluczowy element — komórki blastyczne, komórki macierzyste białaczki oraz komórki śródbłonka wyściełające naczynia — jest reprezentowany jako indywidualny „agent” działający według reguł opartych na biologii. Dyfundujące cząsteczki takie jak TNF-α, miR-126, inhibitor TKI AC220 oraz lek blokujący miR-126 zwany miRisten rozprzestrzeniają się po symulowanej tkance. Model został skalibrowany na danych obrazowych myszy, które odwzorowują rzeczywiste wzory naczyń, w tym obszary bogate lub ubogie w naczynia produkujące miR-126. W symulacjach standardowe leczenie TKI powtarzalnie reprodukowało efekt Janusa: liczba blastów malała, TNF-α spadał, miR-126 z naczyń wzrastał, komórki macierzyste wycofywały się do ochronnych nisz, a choroba później odradzała się.
Wyłączenie tarczy przy precyzyjnym harmonogramie
Wyposażeni w ten wirtualny system, badacze testowali sposoby przerwania błędnego cyklu. Zwykłe dodanie miRistenu jednocześnie z TKI pomagało, lecz rzadko prowadziło do wyleczenia w modelu. Bardziej strategiczne podejście okazało się silniejsze: krótka „przedterapia” samym miRistenem w celu stłumienia naczyniowego miR-126, a następnie podanie samego TKI lub kontynuacja terapii skojarzonej. W wielu symulowanych układach naczyniowych już kilka dni przedterapii miRistenem przed rozpoczęciem AC220 dramatycznie zmniejszało lub eliminowało ryzyko nawrotu przy jednoczesnym ograniczeniu całkowitej ekspozycji na leki. Model ujawnił również, że odległość komórek macierzystych białaczki od naczyń krwionośnych silnie wpływa na ich los — komórki przylegające bezpośrednio do naczyń zyskują największą ochronę, chyba że miR-126 zostanie zablokowany.
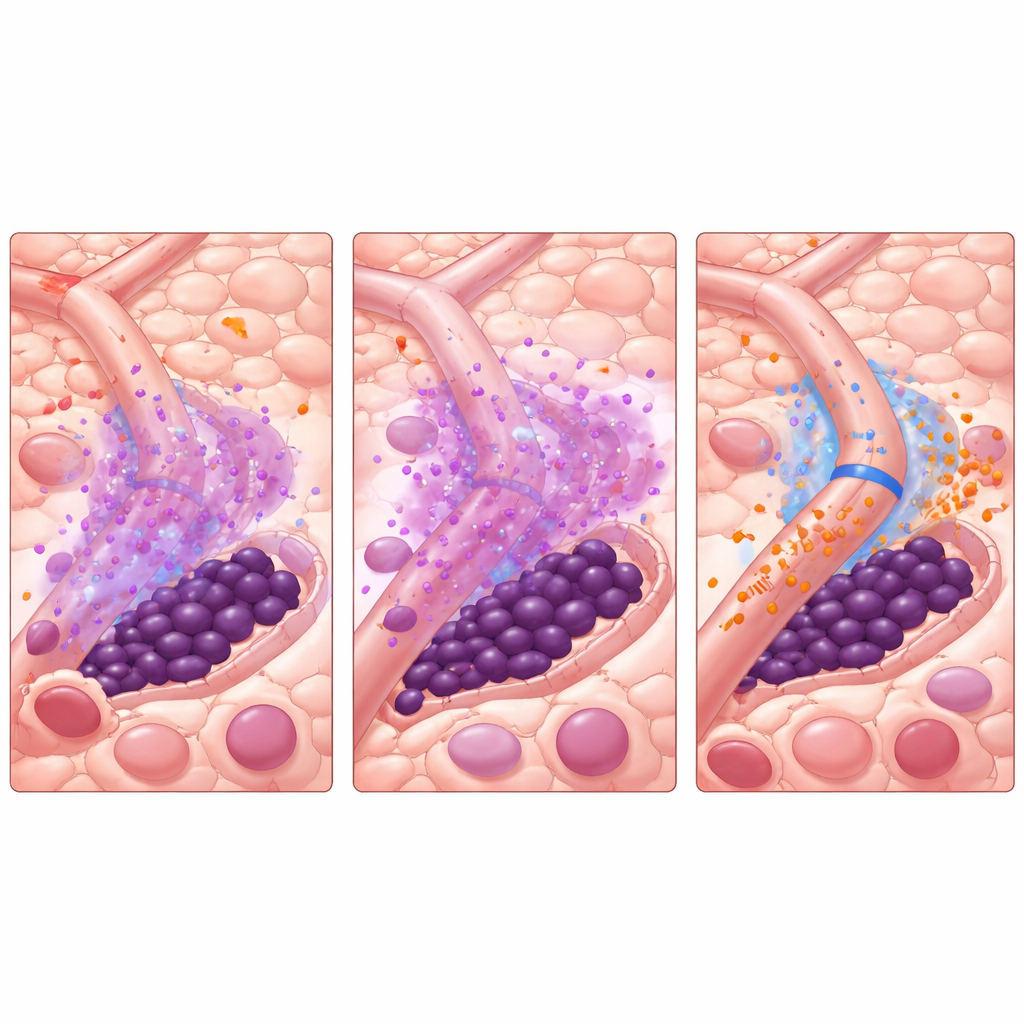
Co to może znaczyć dla przyszłej opieki
Mówiąc wprost, badanie sugeruje, że niektóre komórki macierzyste białaczki przetrwają nie dlatego, że TKI są słabe, lecz dlatego, że drobne naczynia krwionośne w szpiku tymczasowo przełączają się w tryb „opiekuna” podczas leczenia. Krótkie wyłączenie pojedynczego sygnału, miR-126, przed podaniem TKI może umożliwić zdjęcie tej tarczy, wypchnięcie komórek macierzystych z kryjówek i uczynienie ich podatnymi na zabicie przez istniejące leki. Choć praca opiera się na symulacjach komputerowych zakotwiczonych w danych laboratoryjnych — a nie jeszcze na badaniach klinicznych — proponuje konkretną strategię: zsynchronizować podanie leku celującego mikrośrodowisko tuż przed i w trakcie standardowej terapii. Jeśli zostanie to potwierdzone, podejście to mogłoby nie tylko poprawić wyniki u osób z AML z mutacją FLT3, lecz także zainspirować podobne taktyki w innych chorobach nowotworowych krwi i guzach litych, gdzie „sąsiedztwo” guza pomaga mu unikać leczenia.
Cytowanie: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Słowa kluczowe: ostra białaczka szpikowa, komórki macierzyste białaczki, mikrośrodowisko szpiku kostnego, oporność na inhibitory kinazy tyrozynowej, inhibicja miR-126