Clear Sky Science · pl
Opracowanie ciężkiego modelu zespołu ponownego żywienia u szczurów i modelowanie matematyczne związanej z nim hipofosfatemii
Dlaczego ponowne jedzenie może być niebezpieczne
Gdy osoby ciężko niedożywione w końcu otrzymują pokarm lub żywienie dożylne, lekarze muszą postępować ostrożnie. Nagły dopływ kilokalorii może wywołać „zespół ponownego żywienia” — powikłanie zaburzające gospodarkę elektrolitową i zagrażające sercu, mięśniom oraz płucom. Kluczową rolę odgrywa fosfor, minerał niezbędny do wytwarzania energii w każdej komórce. W badaniu wykorzystano szczury i modelowanie komputerowe, aby wyjaśnić, dlaczego poziom fosforu we krwi może gwałtownie spaść podczas ponownego żywienia i jak można lepiej zapobiegać temu niebezpiecznemu spadkowi.
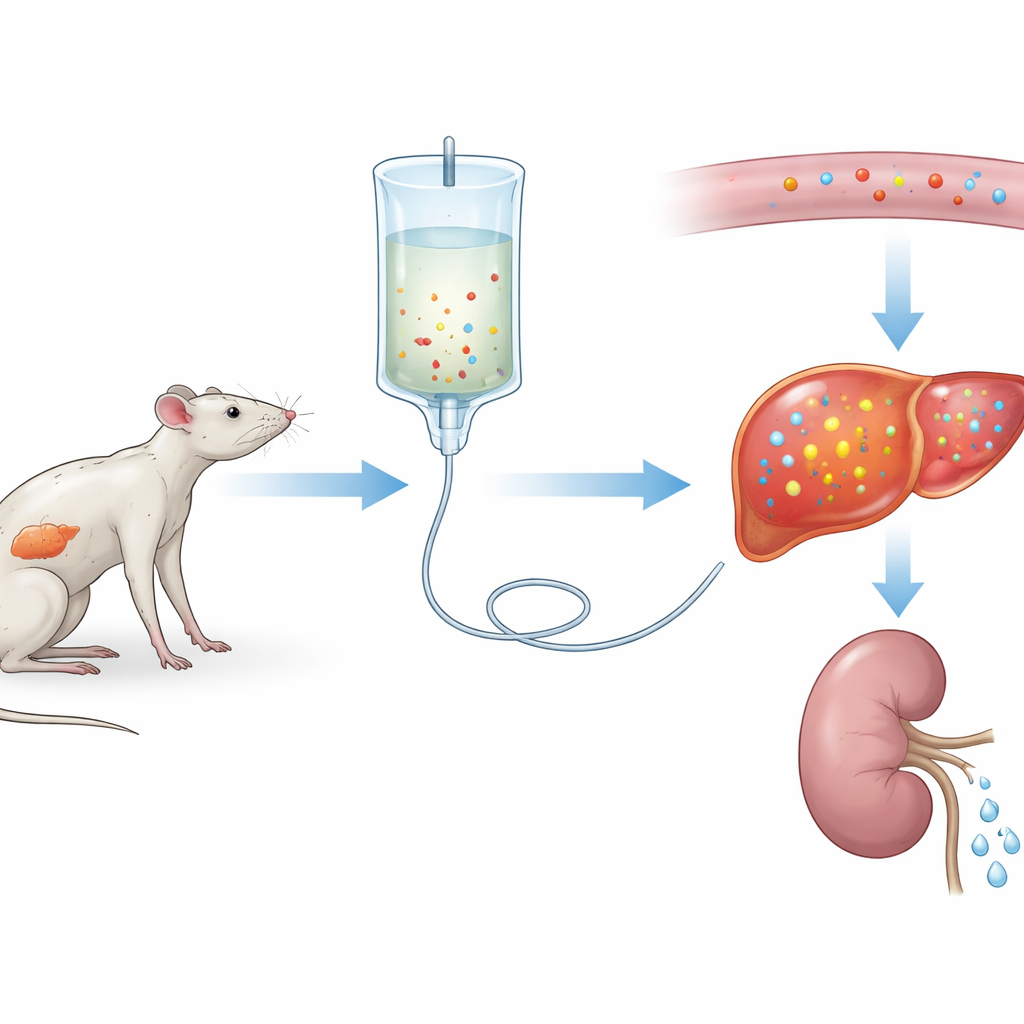
Bliższe spojrzenie na problemy przy ponownym żywieniu
Naukowcy najpierw opracowali ciężką postać zespołu ponownego żywienia u szczurów. Przez trzy tygodnie jedna grupa otrzymywała normalną dietę, podczas gdy druga miała bardzo mało białka, naśladując długotrwałe niedożywienie. Następnie obie grupy otrzymywały to samo żywienie dożylne przez trzy dni. Szczury na diecie ubogobiałkowej wykazały gwałtowny spadek stężenia fosforu we krwi — około 75% — wraz ze zmianami innych elektrolitów i cechami uszkodzenia narządów, szczególnie wątroby i mięśni. Zmiany przypominały ciężki zespół ponownego żywienia u pacjentów, co sugeruje, że zespół zbudował wiarygodny model eksperymentalny.
Co dzieje się z fosforem podczas ponownego żywienia
Aby zrozumieć, jak fosfor przemieszcza się w organizmie w czasie, naukowcy wielokrotnie pobierali próbki krwi i moczu od tych samych szczurów. Stwierdzili, że poziom fosforu we krwi spadał zarówno u zwierząt odżywianych normalnie, jak i u głodzonych białkowo po rozpoczęciu żywienia, ale spadek był znacznie głębszy i dłużej utrzymujący się w grupie niedożywionej. Co zaskakujące, nerki faktycznie zmniejszały utratę fosforu z moczem tuż po ponownym żywieniu, więc minerał nie był wydalany. Zamiast tego fosfor był przyswajany z krwiobiegu do tkanek, szczególnie do wątroby, gdzie zapasy zostały wyczerpane przez tygodnie złej diety. Obliczenia komputerowe potwierdziły, że niedożywione szczury zaczynały z dużo niższą zawartością fosforu wewnątrzkomórkowego, a następnie intensywnie go uzupełniały, gdy pojawiły się składniki odżywcze.
Insulina to nie wszystko
Ponieważ ponowne żywienie podnosi poziom glukozy we krwi i hormonu insuliny, lekarze od dawna obwiniali insulinę za przesuwanie fosforu do komórek. Zespół przetestował ten pomysł, tłumiąc wydzielanie insuliny za pomocą hormonu somatostatyny. Jak przewidywano, poziom glukozy wzrósł, ale spadek fosforu we krwi ledwie się poprawił. Jednocześnie wzrosły poziomy wolnych aminokwasów — budulca białek. W osobnym eksperymencie usunięto aminokwasy z infuzji. Wówczas poziomy fosforu pozostały znacznie stabilniejsze, a ciężki spadek został zapobiegnięty, mimo podobnych stężeń insuliny. Wyniki te wskazują na efekt skojarzony: zarówno insulina, jak i aminokwasy, a nie sama insulina, pobudzają komórki do pobrania dodatkowego fosforu podczas ponownego żywienia.
Ukryta sieć regulacyjna w wątrobie i nerkach
Idąc dalej, badacze zbadali białka wątroby zaangażowane w wykrywanie składników odżywczych, koncentrując się na szlaku znanym jako mTOR, który reaguje na insulinę i aminokwasy. U szczurów na diecie niskobiałkowej ponowne żywienie silnie aktywowało ten szlak i zwiększało poziomy transportera fosforanowego zwanego Pit2, który pomaga komórkom wątroby pobierać fosfor. Wzorzec pasował do zachowania przewidywanego przez ich model matematyczny, który zgrupował tę sieć w pojedynczy sygnał kontrolny nazwany „simTOR”. Model wymagał także odrębnego czynnika sprzężenia zwrotnego, aby wyjaśnić, jak nerki dostosowują utratę fosforu z moczem. Pomiary hormonu pochodzącego z kości, FGF-23, dobrze pasowały do tej roli: jego poziomy gwałtownie spadły po rozpoczęciu żywienia, ograniczając wydalanie fosforu, a następnie rozeszły się między szczurami normalnymi i niedożywionymi w sposób odzwierciedlający symulowany sygnał sprzężenia zwrotnego.
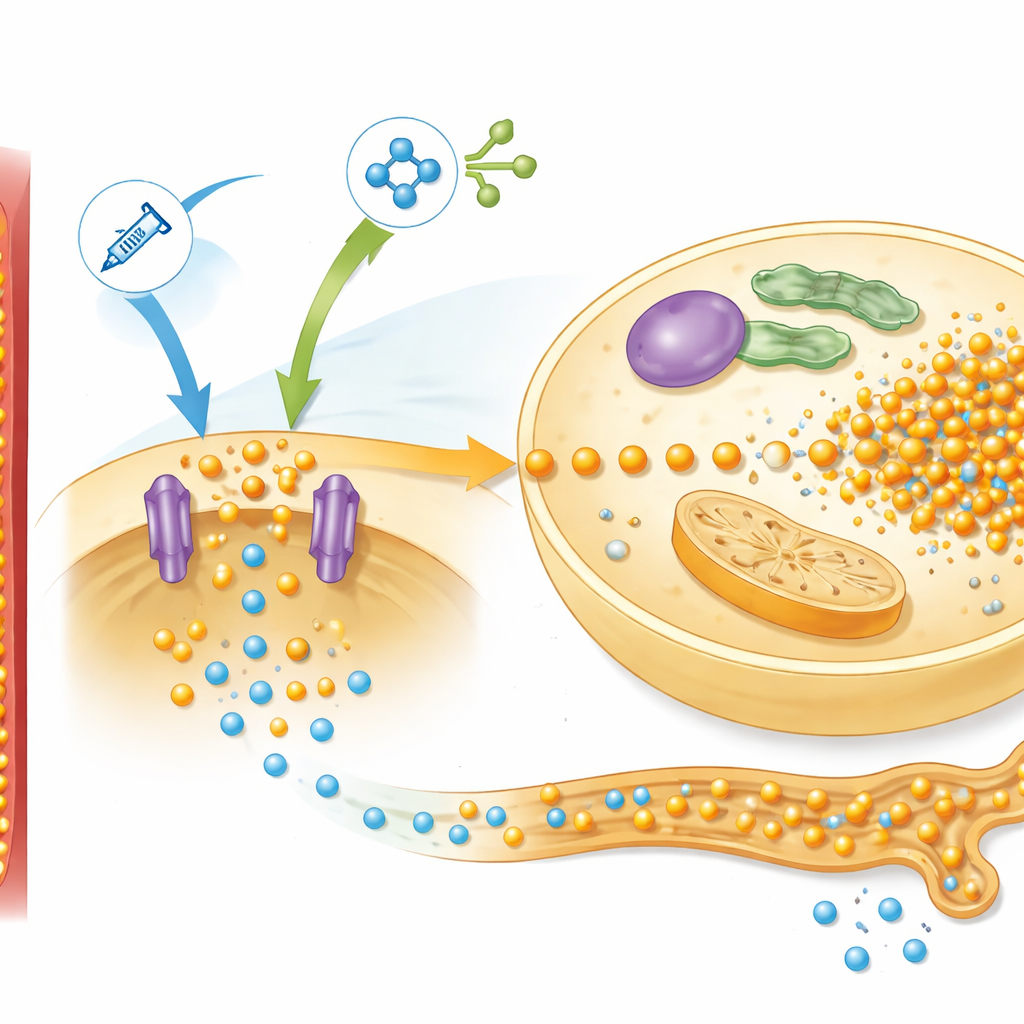
Wykorzystanie matematyki do testowania strategii zapobiegania
Dopasowując różne parametry w modelu komputerowym, autorzy mogli zadawać pytania „co by było gdy”, które trudno lub ryzykownie byłoby testować bezpośrednio u pacjentów. Analiza wskazała trzy główne czynniki wpływające na głębokość i odzyskiwanie po spadku fosforu: początkowa zawartość fosforu wewnątrz komórek, siła układu pobierania napędzanego przez mTOR oraz tempo dostarczania fosforu z żywienia. Symulacje sugerowały, że proste podanie dużej ilości fosforanów w momencie ponownego żywienia byłoby trudne do bezpiecznego wyważenia. Natomiast podanie dodatkowego fosforu przed ponownym żywieniem — pozwalając organom spokojnie odbudować wewnątrzkomórkowe zasoby — mogłoby złagodzić późniejszy spadek poziomów we krwi. Zmniejszenie obciążenia aminokwasami, zwłaszcza tymi silnie aktywującymi mTOR i insulinę, także wydawało się ochronne w eksperymentach na zwierzętach.
Co to oznacza dla pacjentów
Dla osób zagrożonych zespołem ponownego żywienia — takich jak chorzy z długotrwałymi zaburzeniami odżywiania lub ciężką słabością — praca ta sugeruje, że niebezpieczeństwo wynika z czegoś więcej niż tylko skoku glikemii. Głodowane narządy przystępują do ponownego żywienia z pustymi zapasami fosforu, a następnie pod wspólnym wpływem insuliny i aminokwasów szybko pochłaniają minerał z krwi, podczas gdy nerki chwilowo go zatrzymują. W rezultacie powstaje ostry, przejściowy niedobór w krążeniu, który może uszkadzać istotne tkanki. Model na szczurach i opracowana tu rama matematyczna wskazują na bardziej ukierunkowane strategie zapobiegania: ostrożne wczesne stosowanie suplementów fosforu, uważna kontrola żywienia bogatego w aminokwasy oraz uwaga na hormony regulujące wydalanie przez nerki. Wspólnie podejścia te mogą pomóc klinicystom bezpieczniej karmić pacjentów narażonych na ryzyko.
Cytowanie: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Słowa kluczowe: zespół ponownego żywienia, hipofosfatemia, metabolizm fosforu, szlak mTOR, żywienie pozajelitowe