Clear Sky Science · pl
Spatial FBA ujawnia heterogeniczne nisze Warburga w guzach nerek oraz konsumpcję mleczanu w raku jelita grubego
Dlaczego przestrzenne ujęcie metabolizmu guza ma znaczenie
Komórki nowotworowe nie zachowują się jednakowo, nawet w obrębie jednego guza. Niektóre znajdują się blisko naczyń krwionośnych, inne w głębi słabiej ukrwionych obszarów, a te lokalizacje kształtują sposób, w jaki pozyskują i wykorzystują paliwo. W tym badaniu przedstawiono nowy sposób odczytywania ukrytej „mapy metabolicznej” z zaawansowanych danych o przestrzennej ekspresji genów. Dzięki temu autorzy odkrywają zaskakujące wzory w sposobie, w jaki różne guzy gospodarują kluczową cząsteczką — mleczanem — kwestionując klasyczny pogląd, że nowotwory jedynie wypuszczają mleczan jako odpad.
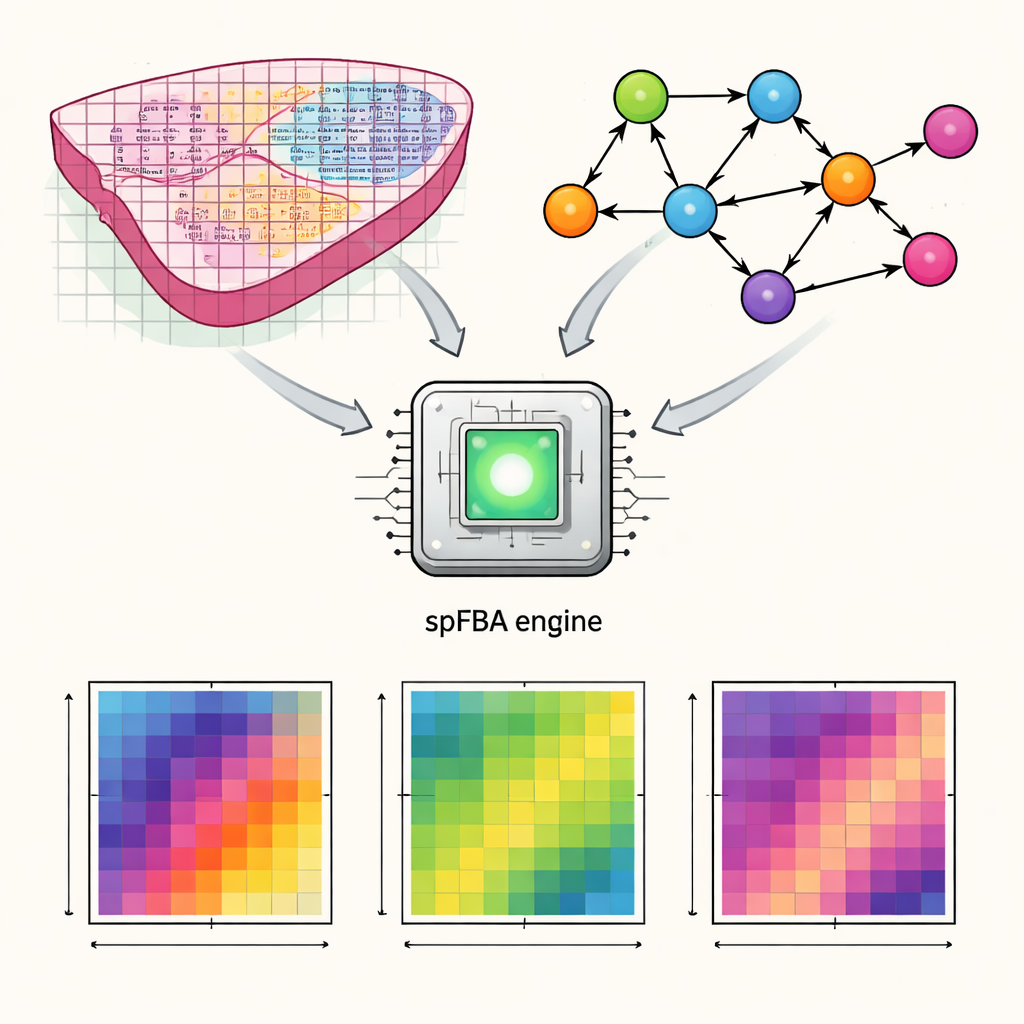
Przekształcanie map genów w aktywność metaboliczną
Autorzy opracowali ramę obliczeniową nazwaną spatial Flux Balance Analysis, w skrócie spFBA. Technologie transkryptomiki przestrzennej mierzą, które geny są aktywne w tysiącach drobnych punktów na cienkim przekroju tkanki. spFBA łączy te przestrzenne mapy aktywności genów z szczegółowymi modelami metabolizmu człowieka, które opisują, jak substancje odżywcze takie jak glukoza, tlen i aminokwasy są przekształcane wewnątrz komórek. Zamiast zakładać, że każdy obszar tkanki ma ten sam cel metaboliczny, spFBA traktuje każde miejsce niezależnie, badając, jakie wzorce reakcji są tam możliwe zgodnie z prawami chemii i bilansu masy. Wynikiem są zbiór „wskaźników wzbogacenia przepływów”, które wskazują, dla każdej lokalizacji, jak silnie różne reakcje metaboliczne prawdopodobnie przepływają i w którym kierunku.
Testowanie metody w guzach nerkowych
Aby sprawdzić, czy spFBA daje biologicznie sensowne rezultaty, zespół najpierw zwrócił się ku jasnokomórkowemu rakowi nerkowemu, nowotworowi nerek znanemu z silnego polegania na rozkładzie cukru (glikolizie) i uwalnianiu mleczanu, zjawisku nazywanym efektem Warburga. Korzystając z opublikowanych danych przestrzennych z dziesięciu próbek guzów nerkowych, badacze sprawdzili, czy przewidywane wzorce metaboliczne odpowiadają znanej strukturze tkanki. Stwierdzili, że miejsca pogrupowane według wywnioskowanych strumieni metabolicznych dobrze pokrywały się z organizacją histologiczną widoczną w mikroskopie oraz z klastrami opartymi jedynie na ekspresji genów. Co ważne, spFBA odtworzyła oczekiwany kontrast metaboliczny między tkanką nowotworową a zdrową nerką: obszary guza wykazywały wyższe wykorzystanie glukozy, silniejszą produkcję biomasy (jako przybliżenie wzrostu komórek) oraz intensywne wydzielanie mleczanu. Jednocześnie wykorzystanie tlenu pozostawało znaczne, ujawniając, że różne części tego samego guza mogą łączyć fermentację i respirację w zależności od lokalnego ukrwienia.
Rak jelita grubego odsłania inną historię mleczanu
Następnie badacze zastosowali ten sam pipeline do nowych wysokorozdzielczych zestawów danych przestrzennych pochodzących od pacjenta z pierwotnym rakiem jelita grubego i dopasowanymi przerzutami w wątrobie, a także do niezależnego publicznego zestawu danych colorectal uzyskanego inną technologią. Wyniki były zdecydowanie inne. Zamiast eksportować mleczan jako odpad, większość regionów raka jelita grubego — zarówno w pierwotnym guzie okrężnicy, jak i w przerzutach w wątrobie — przewidywano jako importujące mleczan z otoczenia. Komórki zrębu w pobliskiej tkance wspierającej miały tendencję do uwalniania niewielkich ilości mleczanu, podczas gdy komórki nowotworowe zachowywały się jak silni konsumenci. Śledząc wzorce strumieni reakcji, autorzy pokazują, że te komórki przerzutowe nie spalają mleczanu jedynie w zwykłym cyklu energetycznym w mitochondriach. Raczej przekształcają mleczan w składniki budulcowe, które zasilają szlaki syntezy tłuszczów i innych elementów potrzebnych do wzrostu komórek — „pseudo–odwrotny efekt Warburga”, w którym mleczan staje się surowcem do biosyntezy.
Nisze metaboliczne i granica guz–zrąb
Ponieważ spFBA zachowuje układ przestrzenny, potrafi wskazać, gdzie zachodzą konkretne wymiany metaboliczne. W guzach nerkowych metoda ujawniła współistniejące „sąsiedztwa” metaboliczne: lepiej natlenione, bogate w naczynia interfejsy, gdzie komórki nowotworowe jednocześnie oddychają i fermentują, oraz głębsze, słabo unaczynione rdzenie, które silniej polegają na fermentacji. W przerzutach raka jelita grubego w wątrobie spFBA uwydatniła ostre kontrasty na granicy między guzem a zrębem, gdzie kierunek obróbki glutaminianu i mleczanu się zmieniał, sugerując intensywną wymianę na froncie inwazyjnym. We wszystkich zestawach danych przewidywane strumienie związane ze wzrostem skorelowane były z niezależnymi miarami proliferacji opartymi na genach, co wspiera biologiczny realizm modelu. Co kluczowe, ten sam algorytm przewidział wydzielanie mleczanu w raku nerek, ale pobieranie mleczanu w raku jelita grubego, wskazując, że obserwowane różnice wynikają z danych, a nie z wbudowanych uprzedzeń modelu.
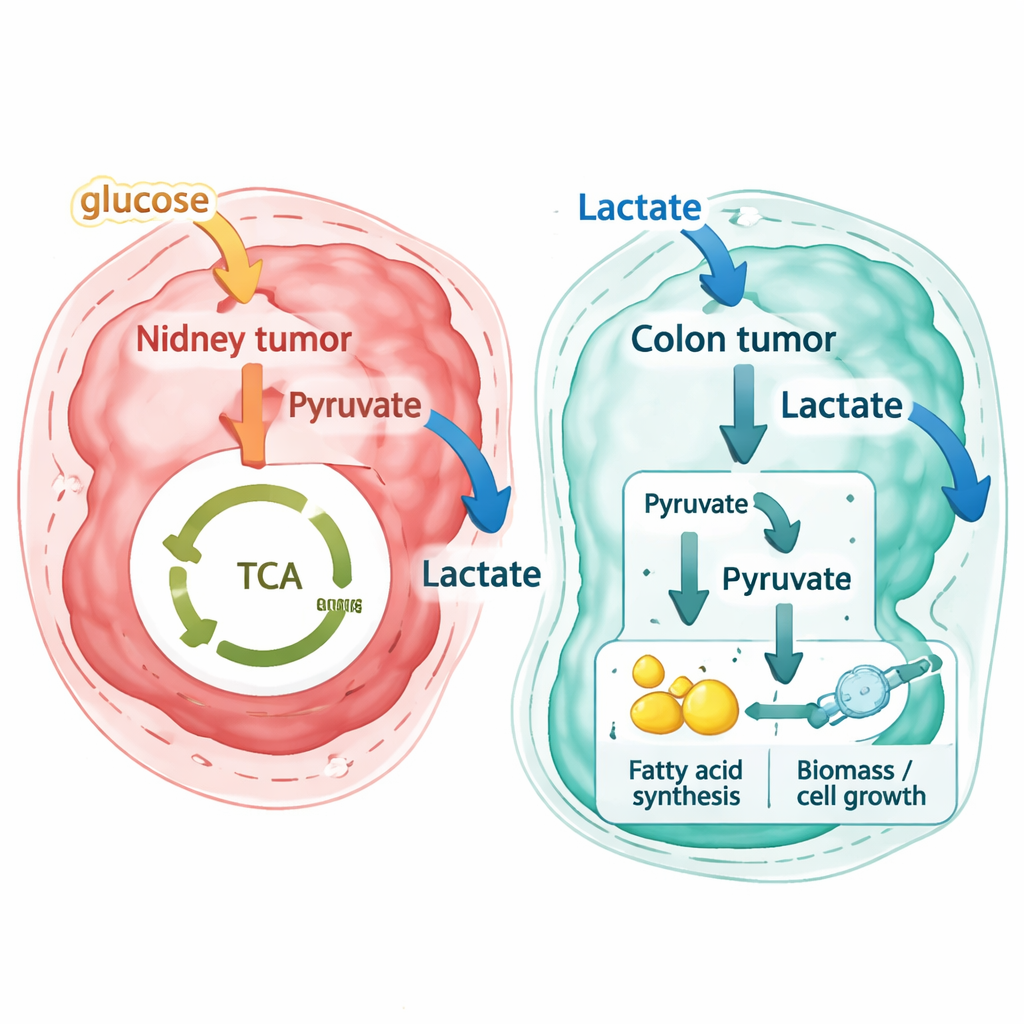
Co to znaczy dla zrozumienia i leczenia nowotworów
Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że metabolizm nowotworów nie jest tylko nieprawidłowy — jest też wysoce lokalny. Ten sam guz może gościć wiele nisz metabolicznych, a podobnie wyglądające guzy w różnych narządach mogą wykorzystywać te same cząsteczki w przeciwny sposób. Praca ta pokazuje, że nakładając przestrzenną ekspresję genów na szczegółowe modele metaboliczne, badacze mogą wnioskować, gdzie guzy prawdopodobnie będą głodne określonych składników odżywczych, takich jak mleczan. W raku jelita grubego odkrycie, że komórki nowotworowe w znacznym stopniu konsumują mleczan i kierują go do procesów związanych ze wzrostem, rodzi nowe pytania o to, jak dieta, mikrobiota jelitowa i metabolizm wątroby wpływają na przebieg choroby oraz czy blokowanie wykorzystania mleczanu mogłoby uczynić te guzy bardziej podatnymi na terapię.
Cytowanie: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Słowa kluczowe: metabolizm nowotworów, transkryptomika przestrzenna, mleczan, efekt Warburga, rak jelita grubego