Clear Sky Science · pl
Analiza sieci dynamicznych ujawnia długodystansowe sprzężenia reszt w interfejsie pMHC odpowiadające za zwiększoną immunogenność
Jak drobne fragmenty wirusa sterują naszą obroną immunologiczną
Nasze cytotoksyczne limfocyty T patrolują organizm w poszukiwaniu śladów infekcji lub nowotworu. Robią to, skanując drobne fragmenty białek, zwane peptydami, prezentowane na powierzchni komórek przez cząsteczki klasy I MHC. Badanie stawia subtelne, lecz istotne pytanie: jak pojedyncza niewielka zmiana w jednym z tych peptydów może sprawić, że limfocyty T zareagują znacznie silniej — albo wcale? Okazuje się, że odpowiedź dotyczy nie tylko statycznej struktury, lecz także tego, jak cała molekularna zabudowa porusza się i ugina w czasie.
Zamek, klucz i ruchome części
Aby zrozumieć to badanie, warto wyobrazić sobie kompleks peptyd–MHC (pMHC) jako zamek, a receptor limfocytu T (TCR) jako klucz. Peptyd siedzi w rowku cząsteczki MHC i razem tworzą powierzchnię, którą bada TCR. Wcześniejsze badania wykazały, że zarówno dokładna sekwencja peptydu, jak i wariant MHC silnie wpływają na to, czy limfocyt T zareaguje. Naukowcy inżynierowali też „zmienione ligandy peptydowe”, wprowadzając niewielkie zmiany, aby modulować odpowiedzi immunologiczne, również w immunoterapii nowotworów. Jednak choć dużo wiemy o statycznych kształtach tych kompleksów, znacznie mniej o tym, jak ruchy w jednym miejscu peptydu mogą wpływać na odległe fragmenty interfejsu, tam gdzie TCR faktycznie się wiąże.
Przypadek wirusowy z czterema niemal identycznymi peptydami
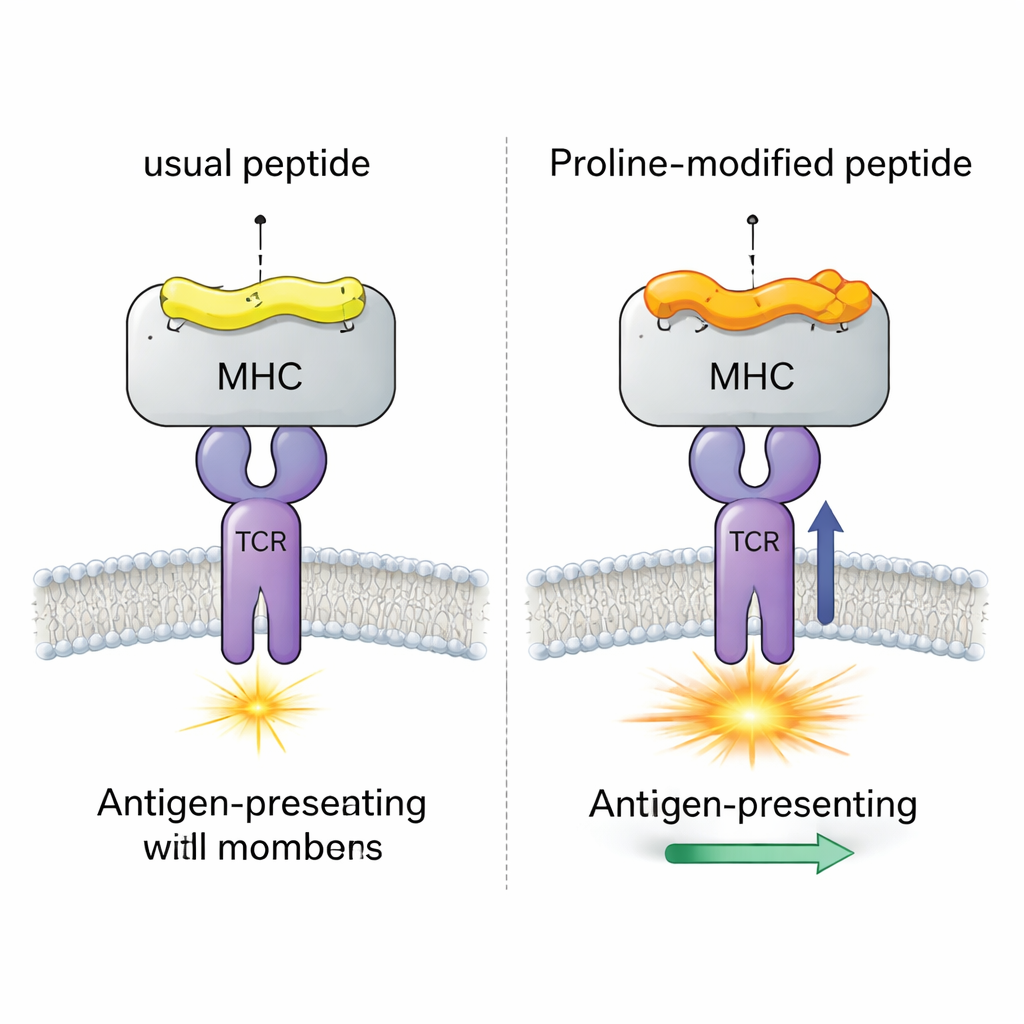
Zespół skupił się na dobrze zbadanym układzie wirusa mysiego (LCMV) obejmującym peptyd gp33, który zwykle wywołuje silne odpowiedzi limfocytów CD8+. Porównali cztery blisko spokrewnione wersje tego peptydu, wszystkie związane z tym samym molekułą MHC (H-2Db). Jedna wersja to oryginalny wirusowy peptyd; jedna zawiera mutację umożliwiającą ucieczkę przed układem odpornościowym, którą limfocyty T ledwie rozpoznają; a dwie to kandydaci na szczepionkę zmodyfikowani proliną, gdzie pojedynczy aminokwas blisko początku peptydu został zamieniony na prolinę. Wcześniejsze eksperymenty pokazały, że ta zamiana na prolinę zwiększa spójność kompleksu peptyd–MHC i siłę odpowiedzi modelowego TCR (nazwanego P14), lecz szczegółowy mechanizm pozostawał niejasny.
Obserwacja drgań cząsteczek: symulacje napotykają krystalografię
Aby odkryć, co się dzieje, autorzy połączyli struktury krystaliczne o wysokiej rozdzielczości z długimi, atomowymi symulacjami komputerowymi każdego kompleksu pMHC w ruchu. Badali, jak bardzo każdy reszt aminokwasowych waha się w czasie i jak te wahania zmieniają się, gdy trzecia pozycja peptydu zostaje zmieniona na prolinę. Poprzez korelację wzorców ruchu w wielu sparowanych symulacjach stworzyli „mapę dynamiczną” ukazującą, które reszty poruszają się razem, nawet gdy są daleko od siebie w przestrzeni. Następnie przekształcili tę mapę w sieć, gdzie każda reszta to węzeł, a krawędzie reprezentują statystycznie powiązane ruchy, i analizowali tę sieć za pomocą narzędzi teorii grafów podobnych do tych używanych w analizie sieci społecznych.
Komunikacja na duże odległości wewnątrz zamka odpornościowego
Główne odkrycie polega na tym, że zmiana trzeciej reszty peptydu na prolinę robi więcej niż tylko usztywnia lokalne miejsce. Zmienia sposób, w jaki ruch jest przekazywany wzdłuż jednej z helis MHC, która graniczy z rowkiem wiążącym peptyd. To z kolei wpływa na zachowanie innej reszty peptydu, pozycji szóstej, która znajduje się tuż pod obszarem kontaktu TCR i jest kluczowa dla rozpoznania. W „dobrych” wersjach zmodyfikowanych proliną ta reszta próbkuje szerszy zakres konformacji, w tym te optymalne do wiązania z TCR. W wariancie umożliwiającym ucieczkę przed immunologią, bez proliny, ta reszta jest bardziej zablokowana i rzadko przyjmuje orientację sprzyjającą TCR. Analiza sieci ujawnia, że wpływ ten podróżuje poprzez konkretne aminokwasy w rowku MHC, tworząc łańcuch dynamicznie sprzężonych reszt, który łączy miejsce zmiany proliny z regionem kontaktu TCR.
Dlaczego to ma znaczenie dla szczepionek i immunoterapii
Wyniki pokazują, że immunogenność — jak silnie peptyd pobudza limfocyty T — to nie tylko kwestia dopasowania kształtów w jednym momencie, lecz także tego, jak kompleks „oddycha” i wygina się w czasie. Subtelna zmiana w jednej pozycji może rozlać się przez molekularną sieć, zwiększając prawdopodobieństwo, że kluczowe reszty kontaktowe pokażą się w konformacjach kompatybilnych z TCR. Proponowany przez autorów workflow obliczeniowy daje sposób na systematyczne wykrywanie takich długodystansowych sprzężeń, co może pomóc w projektowaniu zmienionych peptydów do szczepionek i terapii przeciwnowotworowych. Mówiąc prosto: pokazują, że poprzez przemyślane wybieranie miejsca modyfikacji peptydu, można nakłonić cały zamek do bardziej „gotowego-do-otwarcia” stanu dynamicznego dla klucza układu odpornościowego.
Cytowanie: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Słowa kluczowe: rozpoznawanie przez limfocyty T, peptyd MHC, dynamika białek, zmienione ligandy peptydowe, immunogenność