Clear Sky Science · pl
Poruszanie się po obszarze bezpośredniego przeprogramowywania komórek z DiReG
Przekształcanie jednego typu komórki w inny
Wyobraź sobie, że można w razie potrzeby przemienić komórkę skóry w komórkę serca lub wątrobę. Tego rodzaju bezpośrednie przeobrażanie, zwane przeprogramowywaniem komórkowym, mogłoby pozwolić lekarzom hodować tkanki do przeszczepów, modelować choroby w laboratorium i testować leki w bezpieczniejszy sposób. Znalezienie właściwych molekularnych „przełączników”, które trzeba w komórce odwrócić, przypomina jednak zgadywanie kombinacji sejfu: możliwości są tysiące, a testowanie ich po kolei jest wolne i kosztowne. Artykuł opisuje, jak naukowcy próbują użyć komputerów, by zawęzić wybór, i przedstawia nowy internetowy przewodnik DiReG, który pomaga projektować i weryfikować receptury przeprogramowywania w sposób bardziej przemyślany.
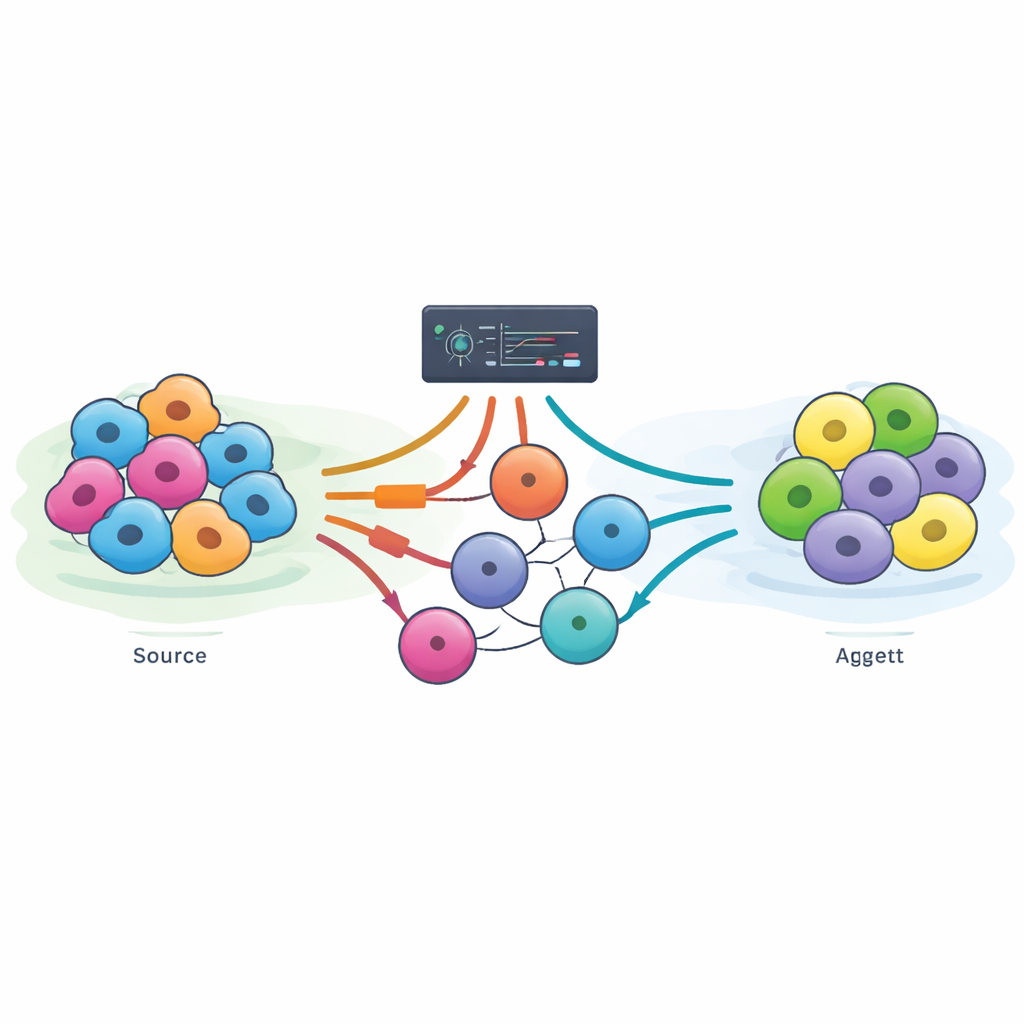
Od przypadkowych odkryć do systematycznego projektowania
Historia przeprogramowywania komórek zaczęła się, gdy badacze odkryli, że wymuszenie ekspresji pojedynczego genu MyoD1 w komórkach tkanki łącznej może przekształcić je w komórki mięśniowe. Później znaleziono inne kombinacje, które potrafią wywołać powstawanie neuronów lub komórek produkujących insulinę, a także cztery „czynniki Yamanaki”, które cofają dojrzałe komórki do stanu podobnego do komórek macierzystych. Te przełomy pokazały, co jest możliwe, lecz sposób ich odkrywania opierał się w dużej mierze na ekspertowym zgadywaniu i długotrwałej pracy laboratoryjnej. Bezpośrednie przeprogramowywanie — przejście bezpośrednio z jednego dojrzałego typu komórki w inny — pozostaje szczególnie trudne, ponieważ wiele prób zatrzymuje się w połowie drogi, daje niestabilne „hybrydowe” komórki lub nie usuwa w pełni poprzedniej tożsamości komórkowej.
Komputery jako wyszukiwarki receptur
W ciągu ostatniej dekady stworzono kilka narzędzi obliczeniowych, które mają pomóc wybrać obiecujące zestawy czynników transkrypcyjnych — genów działających jak główne przełączniki tożsamości komórkowej. Artykuł przegląda sześć wiodących metod, które przesiewają duże zbiory danych dotyczących aktywności genów i regulacji DNA, by zasugerować, które czynniki mogą spowodować zmianę z jednego typu komórki na inny. Niektóre skupiają się głównie na tym, które geny są włączone lub wyłączone, inne budują diagramy połączeń w postaci sieci regulacyjnych, a nowsze uwzględniają dostępność DNA i informacje o enhancerach — miejscach, gdzie znajduje się wiele przełączników kontrolnych. Każdy postęp dodaje użyteczne szczegóły, ale żadna z metod nie wyłoniła się jako jednoznaczny zwycięzca, częściowo dlatego, że testowano je na różnych zestawach danych i w różnych warunkach, co uniemożliwia uczciwe porównania.
Ukryte złożoności wewnątrz komórki
Autorzy zwracają uwagę, że wszystkie obecne narzędzia pomijają kilka warstw biologicznych niuansów. Pojedynczy „gen” może istnieć w wielu nieco różnych wersjach białkowych (izoformach), które zachowują się inaczej, a dzisiejsze modele zwykle traktują je jako jedną całość. Chemiczne znaczniki na DNA, takie jak metylacja, mogą blokować lub przyciągać białka regulatorowe, jednak większość algorytmów ignoruje, czy dane miejsce docelowe w ogóle jest użyteczne. Wiele kluczowych pomocników — partnerów białkowych, konkurencyjnych członków rodziny walczących o te same miejsca wiązania czy małych regulatorowych RNA wyciszających niepożądane komunikaty — również jest pomijanych. Na to wszystko nakłada się fakt, że większość metod opiera się na sygnałach uśrednionych z mieszanin komórek i na poziomach RNA, które jedynie przybliżają rzeczywistą aktywność białek, a to właśnie białka rzeczywiście napędzają zmiany.
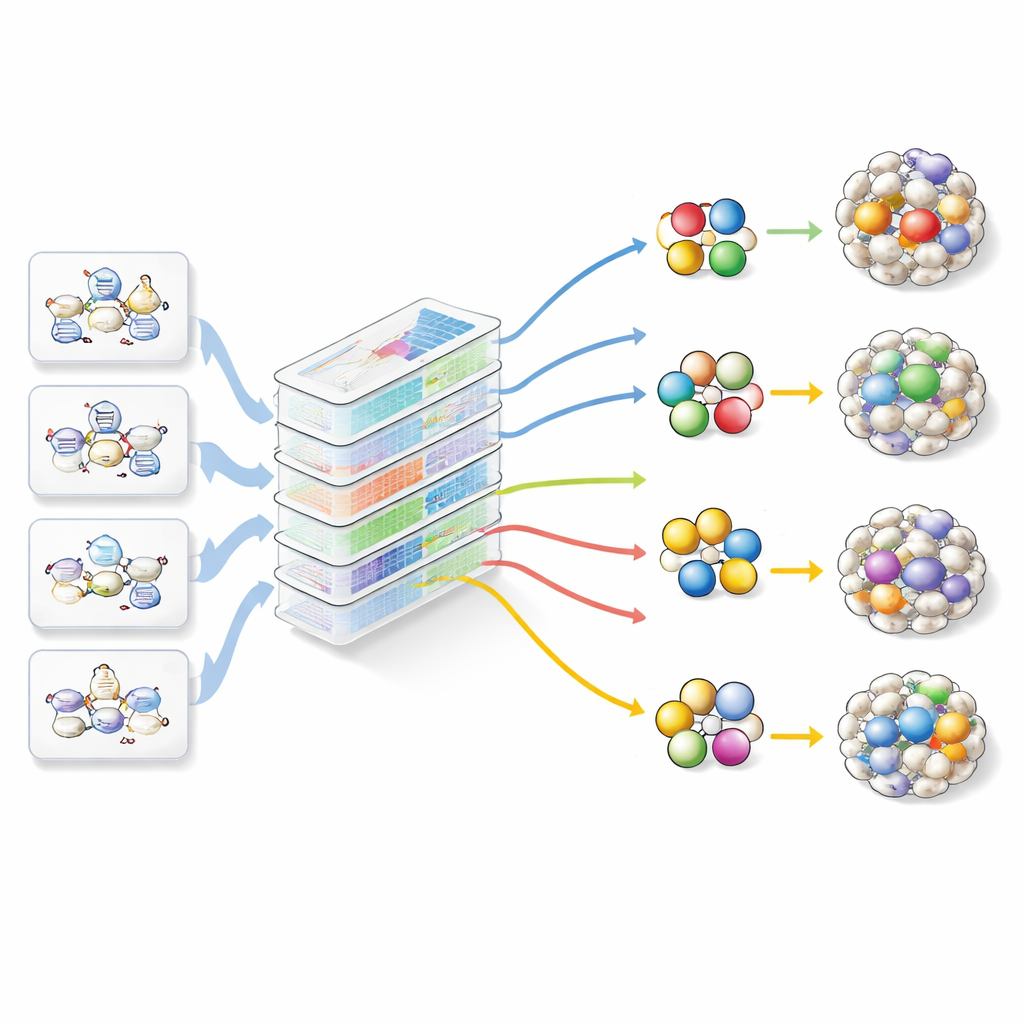
Nowy przewodnik po opcjach
Aby zrobić postęp mimo tych luk, autorzy stworzyli DiReG (Direct Reprogramming Guide), aplikację internetową, która działa mniej jak nowy wszechwiedzący algorytm, a bardziej jak centrum kontroli. DiReG zbiera prognozy z głównych istniejących narzędzi, dodaje prostą metodę opartą na motywach działającą bezpośrednio na danych o otwartości chromatyny i łączy to wszystko z kuratorowaną biblioteką setek prac na temat przeprogramowywania. Dzięki wbudowanym systemom pytań i odpowiedzi badacze mogą szybko znaleźć protokoły, kombinacje czynników i szczegóły eksperymentalne w literaturze. Mogą następnie przenieść kandydackie zestawy czynników do przestrzeni analitycznej, gdzie DiReG rysuje ich sieci regulacyjne, sprawdza, czy dotknięte geny przypominają te z pożądanej tkanki, weryfikuje, gdzie czynniki są naturalnie aktywne, i wyróżnia znanych partnerów interakcji oraz izoformy, które mogą wzmocnić lub utrudnić konwersję.
Krok w stronę mądrzejszej konwersji komórek
Dla osób spoza specjalizacji kluczowy przekaz jest taki, że ta praca nie dostarcza jeszcze przepisu na zasadzie „naciśnij przycisk”, który pozwoli przekształcić dowolną komórkę w dowolną inną. Zamiast tego oferuje scentralizowaną, interaktywną mapę tego, co wiadomo, co było wypróbowane i które genetyczne przełączniki najprawdopodobniej będą współdziałać. Poprzez umożliwienie badaczom szybkiego łączenia prognoz komputerowych z kontekstem biologicznym, DiReG ma na celu ograniczenie prób prowadzących donikąd i uczynienie projektowania protokołów bardziej racjonalnym. Autorzy wskazują też, czego nadal brakuje — bogatszych danych o formach białek, oznaczeniach chemicznych, interakcjach komórka‑komórka i prawdziwej aktywności białek. W miarę jak nowe technologie wypełnią te warstwy, przyszłe narzędzia oparte na pomysłach zaprezentowanych tutaj mogą uczynić bezpośrednie przeprogramowywanie komórek bardziej niezawodnym, bezpieczniejszym i bliższym zastosowań medycznych w praktyce.
Cytowanie: Lauber, M., List, M. Navigating the landscape of direct cellular reprogramming with DiReG. npj Syst Biol Appl 12, 35 (2026). https://doi.org/10.1038/s41540-026-00652-z
Słowa kluczowe: przeprogramowywanie komórek, czynniki transkrypcyjne, biologia obliczeniowa, regulatory genów, medycyna regeneracyjna