Clear Sky Science · pl
Modelowanie in silico różnicowania endodermy przedniego jelita w kierunku progenitorów nabłonka płucnego
Przekształcanie komórek macierzystych w komórki budujące płuca
Naukowcy uczą się, jak nakłonić komórki macierzyste pochodzące od pacjenta, aby stały się zastępczą tkanką płucną, co kiedyś mogłoby naprawiać uszkodzenia wywołane chorobami takimi jak POChP, włóknienie czy ciężkie infekcje. Artykuł opisuje, jak badacze zastosowali modelowanie komputerowe, aby odwzorować i dopracować kluczowy etap tej drogi: przekształcenie pośredniego typu komórki, zwanego endodermą przedniego jelita, w wczesne progenitory nabłonka płucnego — komórki startowe, które ostatecznie mogą tworzyć drogi oddechowe i pęcherzyki płucne.
Dlaczego komórki startowe płuc są ważne
Ludzkie komórki indukowane pluripotentne (iPSCs) można przeprogramować z tkanek dorosłego organizmu i następnie ukierunkować na rozwój różnych organów. Aby zbudować tkankę płucną, komórki te przechodzą przez kilka etapów rozwojowych. Jednym z nich jest endoderma przedniego jelita, warstwa, która w embrionie daje początek częściom układu oddechowego i pokarmowego. Stamtąd, przy odpowiednich sygnałach chemicznych, komórki mogą stać się progenitorami nabłonka płucnego, noszącymi wczesne markery płuc i później dojrzewającymi do wyspecjalizowanych komórek dróg oddechowych lub pęcherzykowych. Ponieważ przyszłe terapie komórkowe będą wymagać miliardów takich komórek, badacze potrzebują sposobów na niezawodne zwiększanie wydajności i dostosowywanie protokołów do różnych linii komórkowych pacjentów bez niekończących się prób i błędów w laboratorium.
Budowanie wirtualnej wersji różnicowania komórek
Zespół rozszerzył wcześniejsze ramy matematyczne, tworząc, według ich wiedzy, pierwszy model populacyjny tego konkretnego przejścia od endodermy przedniego jelita do progenitorów płucnych. Rozważali dwa sposoby reprezentacji komórek: prostą wersję śledzącą tylko całkowitą liczbę żywych komórek oraz bardziej szczegółową, która osobno obserwuje komórki endodermy przedniej i progenitory płucne. W obu przypadkach model śledził też poziomy glukozy i mleczanu w pożywce, reprezentujące substancje odżywcze i produkty odpadowe. Korzystając z narzędzi biologii systemów, badacze skonstruowali wiele kandydackich równań opisujących wzrost, śmierć i różnicowanie komórek, a następnie użyli testów identyfikowalności, by odrzucić modele, których parametrów nigdy nie dałoby się jednoznacznie oszacować, nawet przy idealnych danych.
Projektowanie mądrzejszych eksperymentów z pomocą modelu
Zamiast dopasowywać model do dostępnych danych w sposób przypadkowy, badacze pozwolili modelowi kierować tym, jak powinny być prowadzone nowe eksperymenty. Użyli danych symulowanych, aby ustalić, jak często należy mierzyć liczby komórek i poziomy substancji odżywczych, by dokładnie oszacować parametry modelu, równoważąc precyzję statystyczną z kosztami i pracochłonnością częstego pobierania próbek. Doprowadziło to do praktycznego planu: codzienne pomiary glukozy i mleczanu oraz liczenia komórek co jeden do dwóch dni, w czterech warunkach różniących się stopniem rozdziału kultur w dniu 10 oraz tym, czy pożywka była odnawiana codziennie. Przeprowadzili potem te eksperymenty, mierząc zarówno całą populację komórek, jak i — za pomocą cytometrii przepływowej — ułamki komórek pozostających endodermą przednią lub przekształconych w progenitory płucne.
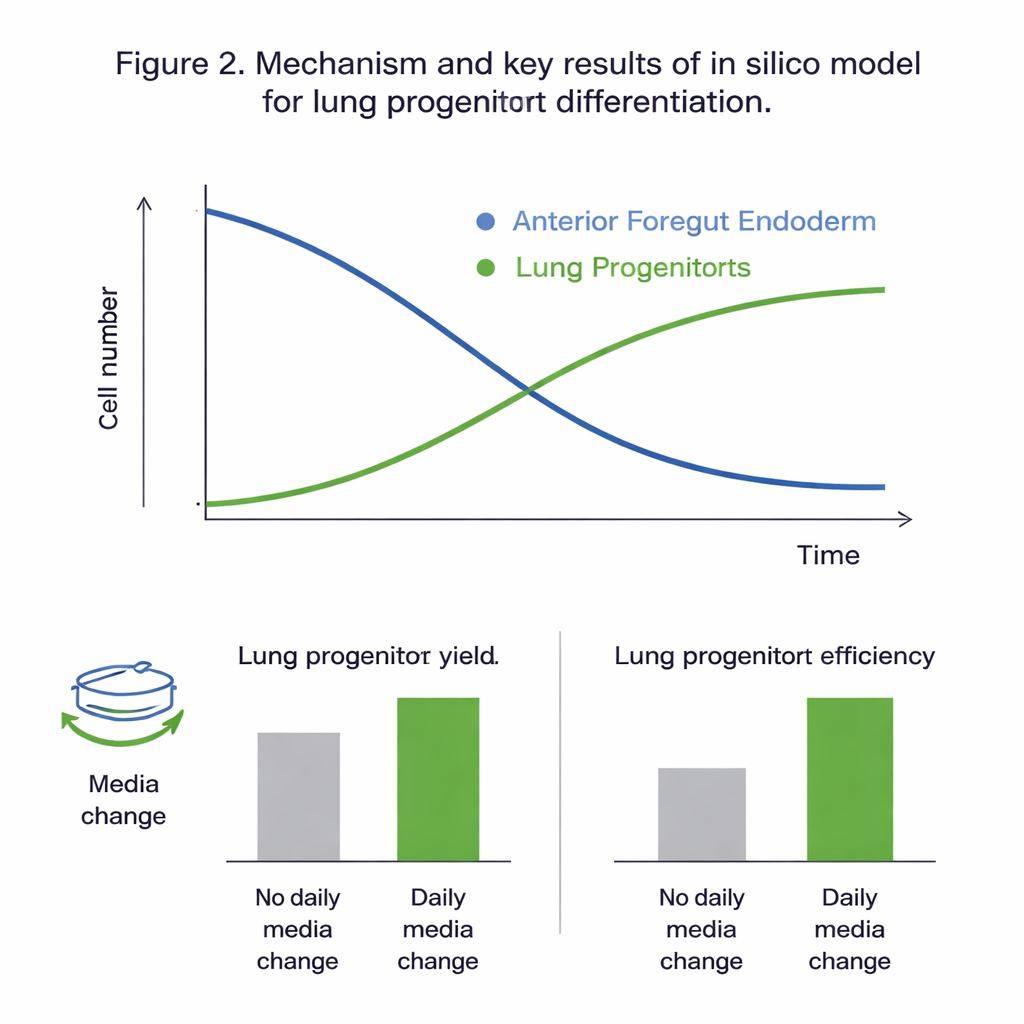
Co ujawniły eksperymenty wirtualne
Dopasowanie wszystkich kandydackich modeli do danych eksperymentalnych wykazało, że model dwupopulacyjny, który osobno śledzi komórki endodermy i progenitory płucne, dał się wiarygodnie skalibrować i najlepiej odzwierciedlał obserwowane zachowanie. Kontrole statystyczne wskazały, że w badanym oknie czasowym (dni 11–15 protokołu) dynamikę napędzały głównie proliferacja i różnicowanie komórek endodermy przedniej, podczas gdy proliferacja samych progenitorów płucnych miała niewielki udział. Globalna analiza wrażliwości wzmocniła ten obraz, wskazując jako główne dźwignie sterujące wynikiem tempo wzrostu, śmierci i różnicowania komórek endodermy oraz wpływ glukozy. Skalibrowany model odtwarzał niepokazywane wcześniej dane z błędami porównywalnymi do naturalnej zmienności eksperymentów, co sugeruje, że jest wystarczająco dokładny, by badać scenariusze „co‑by‑było‑gdyby” in silico.
Optymalizacja zmiany pożywki i rozdzielania komórek
Mając godny zaufania system wirtualny, zespół przetestował, jak dwie praktyczne decyzje protokołowe wpływają na wyniki: jak bardzo rozcieńczyć kulturę (współczynnik rozdziału) w dniu 10 oraz czy pożywka jest wymieniana codziennie. Symulacje przewidziały, że codzienne zmiany pożywki niemal podwajają liczbę progenitorów płucnych i wydajność względem komórki wyjściowej, głównie przez zapobieganie wyczerpaniu substancji odżywczych oraz nagromadzeniu odpadów i niestabilnych cząsteczek sygnałowych. Eksperymenty zgadzały się ściśle z tymi przewidywaniami. Model sugerował też, że zastosowanie wyższych współczynników rozdziału — rozprowadzanie komórek bardziej rozrzedzenie w dniu 10 — poprawia „wydajność na komórkę wejściową” o około jedną czwartą, mimo że zmniejsza absolutną liczbę komórek. W obu przypadkach zmiany te niewiele wpływały na końcowy udział progenitorów płucnych w kulturze, głównie przesuwając liczbę komórek, które można efektywnie wyprodukować.
Co to oznacza dla przyszłych terapii płuc
Dla czytelnika niebędącego specjalistą kluczowe jest to, że autorzy zbudowali coś w rodzaju symulatora lotu dla istotnego etapu hodowli komórek płuc z komórek macierzystych. Łącząc starannie zaprojektowane eksperymenty z rygorystycznym modelowaniem matematycznym, pokazują, jak proste decyzje protokołowe — takie jak częstotliwość wymiany pożywki czy gęstość zaszczepienia komórek — mogą znacząco wpłynąć na liczbę wyprodukowanych komórek budujących płuca, bez zmiany ich jakości. Tego rodzaju modelowanie in silico może pomóc usprawnić przyszłe protokoły, zmniejszyć eksperymentalne zgadywanie i ostatecznie wspierać bardziej niezawodną i skalowalną produkcję progenitorów płucnych do badań, modelowania chorób i w przyszłości terapii regeneracyjnych.
Cytowanie: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Słowa kluczowe: komórki progenitorowe płuca, komórki indukowane pluripotentne, modelowanie in silico, różnicowanie komórek, medycyna regeneracyjna