Clear Sky Science · pl
Wnioskowanie oparte na symulacjach dotyczące dynamiki migracji komórek w złożonych środowiskach przestrzennych
Jak komórki odpornościowe odnajdują drogę przez zatłoczone tkanki
Nasze komórki odpornościowe często muszą przeciskać się przez gęste, przypominające labirynt tkanki, aby dotrzeć do miejsc infekcji lub węzłów chłonnych. To badanie stawia pozornie proste pytanie o dużych implikacjach: jak komórki te nawigują w tak zagraconych środowiskach i jak można wiarygodnie odczytać ich zachowania z nieporządnych danych mikroskopowych? Łącząc precyzyjnie zaprojektowane laboratoryjne „labirynty” z zaawansowanymi symulacjami komputerowymi i nowoczesnymi narzędziami uczenia maszynowego, autorzy pokazują nowe podejście do dekodowania reguł kierujących ruchem komórek w złożonym otoczeniu.
Budowa maleńkiego labiryntu dla komórek odpornościowych
Aby zbadać, jak środowisko kształtuje ruch, badacze skupili się na komórkach dendrytycznych — strażnikach układu odpornościowego, które muszą przemieszczać się z tkanek obwodowych do węzłów chłonnych, prowokowane przez chemokiny. Zbudowali mikrostrukturę: płaski „las filarów” z regularnie rozmieszczonymi słupkami wykonanymi z silikonu (PDMS), z wąskimi szczelinami o szerokości 10 mikrometrów, które naśladują ciasne przestrzenie w prawdziwych tkankach. Po jednej stronie chipu umieszczono dziesiątki tysięcy komórek dendrytycznych; po drugiej umieszczono źródło chemokiny CCL19, które tworzy stabilny gradient przez filary. Przy użyciu mikroskopii z zapisem w czasie śledzono jądra pojedynczych komórek co 30 sekund, gdy próbowały poruszać się w kierunku źródła chemokiny. 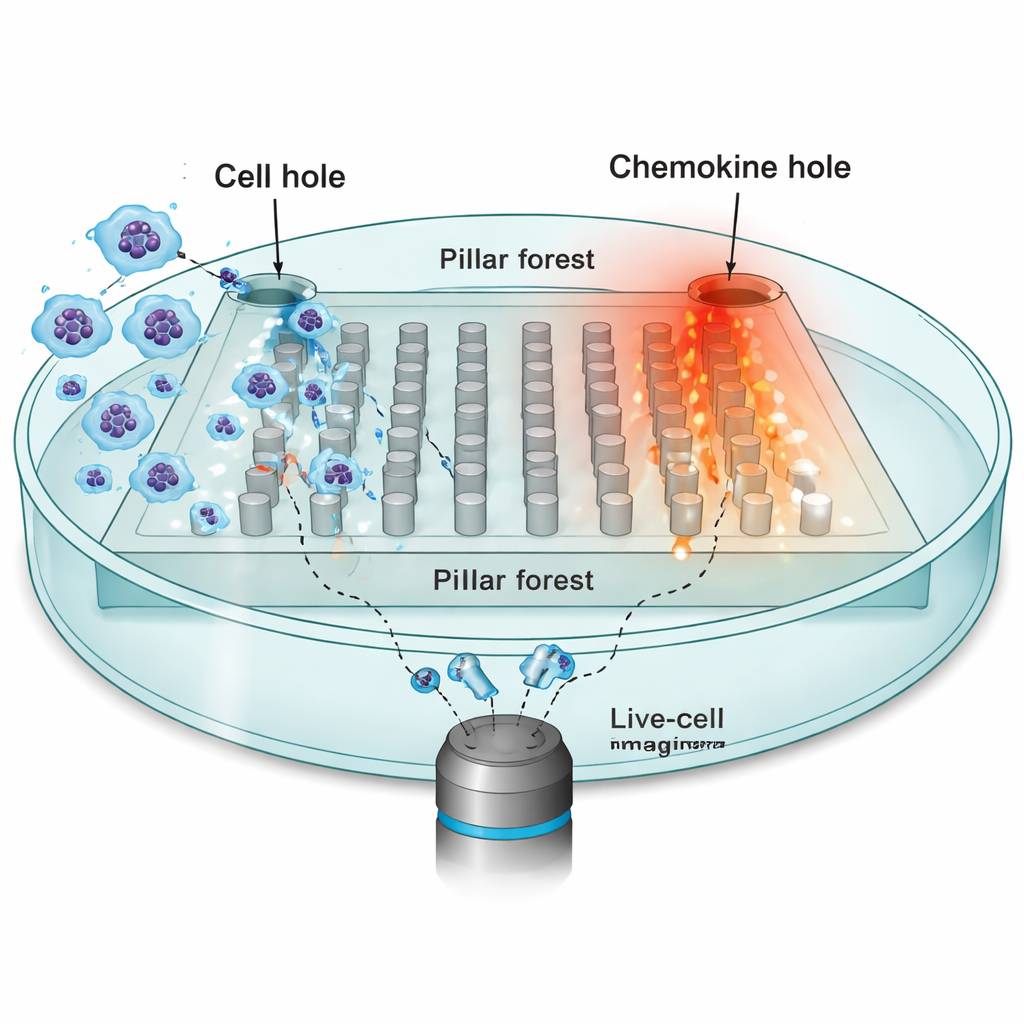
Przekształcanie biologii w eksperyment wirtualny
Aby zrozumieć tę różnorodność, zespół zbudował szczegółowy model komputerowy migracji komórek, korzystając z ram znanych jako model Pottsa komórkowego (Cellular Potts model). Zamiast traktować komórkę jako prosty punkt, podejście to reprezentuje każdą komórkę jako rozciągniętą płaszczyznę na siatce, co pozwala jej zmieniać kształt, wciskać się między filary i reagować na sygnały chemiczne. Model obejmuje cztery kluczowe składniki: jak mocno komórka jest przyciągana przez gradient chemokiny (mdir), jak bardzo ma tendencję do utrzymywania kierunku ruchu (mrand), jak często się reorientuje (opisana stawką λ) oraz jej efektywny rozmiar (a). Poprzez dostosowywanie tych parametrów i uruchamianie symulacji model generuje syntetyczne tory, które można porównać bezpośrednio z zarejestrowanymi ścieżkami komórek w lesie filarów.
Dlaczego ręcznie wybierane miary zawodzą
Tradycyjnie badacze streszczają takie dane o ruchu kilkoma dobrze znanymi statystykami — jak daleko przebyła komórka (przemieszczenie), jak szybko się porusza (prędkość) i jak zmienia się jej kierunek w czasie (kąty skrętu). Autorzy najpierw użyli tych ręcznie skonstruowanych miar w technice zwanej przybliżonym wnioskowaniem bayesowskim (ABC), które poszukuje zestawów parametrów sprawiających, że symulowane tory przypominają eksperymentalne. Stwierdzili, że chociaż te podsumowania oddają ogólne trendy, pomijają wiele drobnych struktur w danych. W efekcie niektóre parametry modelu, szczególnie dotyczące losowej trwałości ruchu i czasu reorientacji, pozostały słabo określone lub nawet obciążone. Ponadto ABC wymagało setek tysięcy symulacji i wielu godzin obliczeń, by osiągnąć akceptowalną zgodność.
Pozwolenie sieciom neuronowym nauczyć się, co ma znaczenie
Aby pokonać te ograniczenia, badanie zwróciło się do nowszej rodziny metod zwanych estymacją posterioru przy użyciu sieci neuronowych (NPE). Tutaj sieć neuronowa jest trenowana bezpośrednio na wielu parach symulowanych danych i odpowiadających im parametrów. Jedna część sieci automatycznie uczy się własnego zwięzłego zbioru „cech podsumowujących” z całych zbiorów torów komórkowych; inna część uczy się, jak te cechy mapować z powrotem na prawdopodobne wartości parametrów. Co kluczowe, wyuczone cechy są optymalizowane wyraźnie pod kątem dokładnego wnioskowania parametrów, a nie dla ludzkiej interpretowalności. Autorzy następnie ponownie wykorzystali wyuczone podsumowania wewnątrz ram ABC, tworząc hybrydowy łańcuch łączący odporność ABC z elastycznością sieci neuronowych. 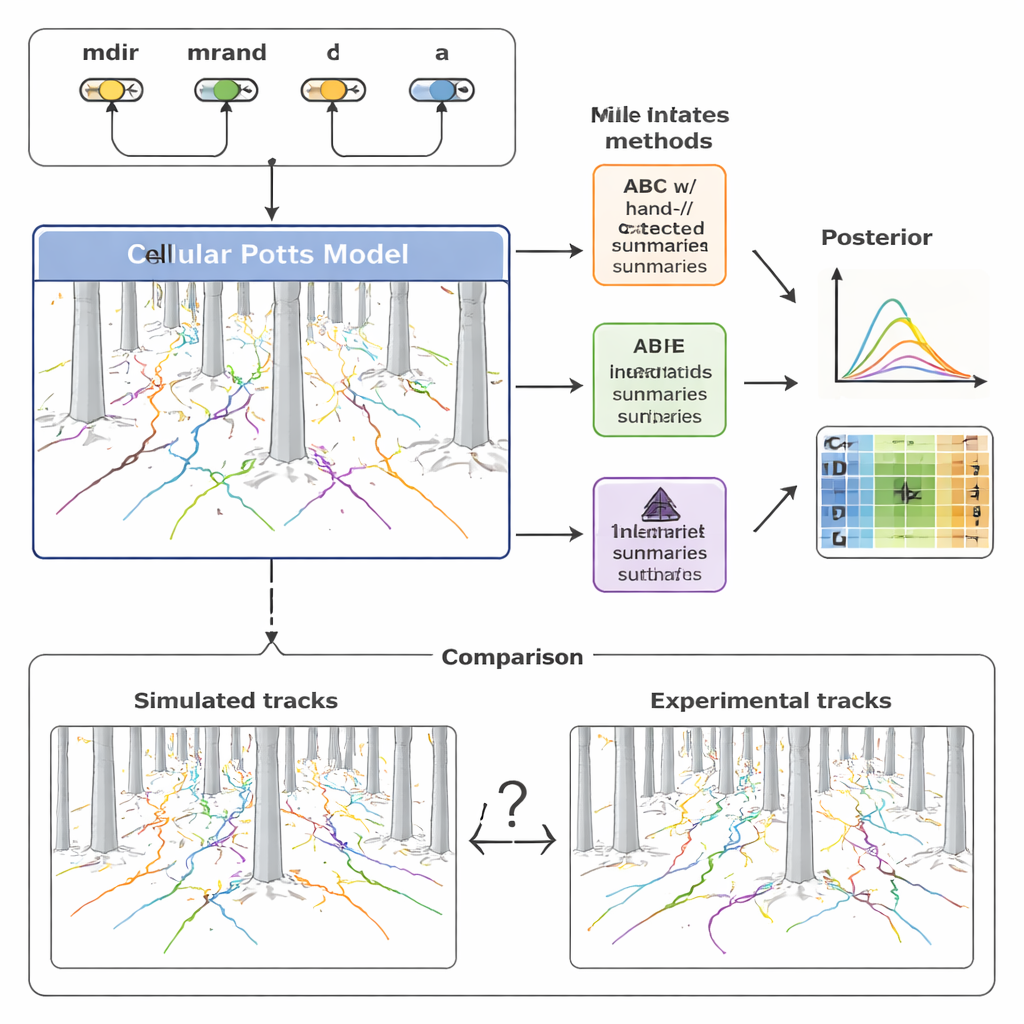
Co nowe podejście ujawnia o nawigacji komórek
Wyposażeni w skalibrowany model, badacze zbadali, jak sygnały chemokinowe i przeszkody fizyczne wspólnie kształtują migrację. Wnioski dotyczące rozmiaru komórek sugerowały, że komórki dendrytyczne efektywnie się kurczą i odkształcają, aby zmieścić się w szczelinach o szerokości 10 mikrometrów, co zgadza się z ich znaną elastycznością. Symulacje wskazały, że uporczywy losowy ruch jest głównym czynnikiem determinującym, jak szeroko komórki się rozprzestrzeniają, nawet bez przewodnictwa chemokin, oraz że las filarów może uwięzić komórki, gdy silne wskazówki kierunkowe i utrzymywanie kierunku działają razem. Co zaskakujące, model przewiduje, że sygnał chemokiny krótko aktywny na początku eksperymentu może w niektórych przypadkach pomóc większej liczbie komórek dotrzeć do celu niż sygnał stały, ponieważ przedłużone przyciąganie może utrzymywać komórki w krążeniu w obrębie przeszkód zamiast pozwolić im się wydostać.
Dlaczego to ma znaczenie dla biologii i modelowania
Dla osób niebędących specjalistami kluczowe przesłanie jest dwojakie. Po pierwsze, migracja komórek odpornościowych w tkankach to nie tylko podążanie za chemicznym śladem; wyłania się ona z subtelnej interakcji między sygnałami kierunkowymi, własnymi tendencjami ruchowymi komórek i fizycznym układem ich otoczenia. Po drugie, wydobycie tych reguł z danych obrazowych wymaga pozwolenia komputerowi na naukę, które wzorce w danych są najbardziej informatywne, zamiast polegać wyłącznie na prostych, zaprojektowanych przez człowieka miarach. Poprzez integrację mikroinżynieryjnych eksperymentów, symulacji uwzględniających kształt oraz wnioskowania opartego na sieciach neuronowych, praca ta dostarcza potężnego wzorca do badania, jak różne typy komórek poruszają się w złożonych środowiskach, z potencjalnymi zastosowaniami od zrozumienia nadzoru immunologicznego po projektowanie lepszych terapii przeciwnowotworowych.
Cytowanie: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
Słowa kluczowe: migracja komórek, komórki dendrytyczne, gradienty chemokin, wnioskowanie oparte na symulacjach, mikrofluidyczne lasy filarów