Clear Sky Science · pl
Kontrola wzrostu glejaka nerwu wzrokowego związana z astmą poprzez interakcje limfocytów T z mikroglejem: model matematyczny
Kiedy problemy z oddychaniem łączą się z guzami mózgu
Astma i guzy mózgu wydają się odległe: jedna wpływa na sposób oddychania, druga na wzrok, myślenie i ruchy. A jednak lekarze zauważyli zagadkowy wzorzec — dzieci z astmą wydają się rzadziej rozwijać niektóre guzy nerwu wzrokowego. Ten artykuł bada, jak przewlekła choroba płuc może niespodziewanie chronić mózg, sięgając po model matematyczny do śledzenia ukrytych chemicznych rozmów między komórkami układu odpornościowego a komórkami nowotworowymi.
Wolno rosnący guz o poważnych konsekwencjach
Glejaki nerwu wzrokowego to na ogół guzy rosnące powoli, które powstają wzdłuż nerwu wzrokowego, najczęściej u dzieci z zaburzeniem genetycznym zwanym nerawłókniakowatością typu 1 (NF1). Mimo że te guzy uważa się za „niski stopień złośliwości”, mogą powodować utratę wzroku i problemy hormonalne. W NF1 uszkodzony gen powoduje nadaktywność białka sygnałowego RAS. Ta nadaktywność uruchamia produkcję innej cząsteczki, midkiny, która działa jak głośnik w nerwie wzrokowym — przyciąga komórki odpornościowe i przekształca lokalne środowisko w sposób, który zwykle sprzyja guzkowi, zamiast go zwalczać.
Rozmowa między komórkami nerwowymi a odpornościowymi, która karmi guz
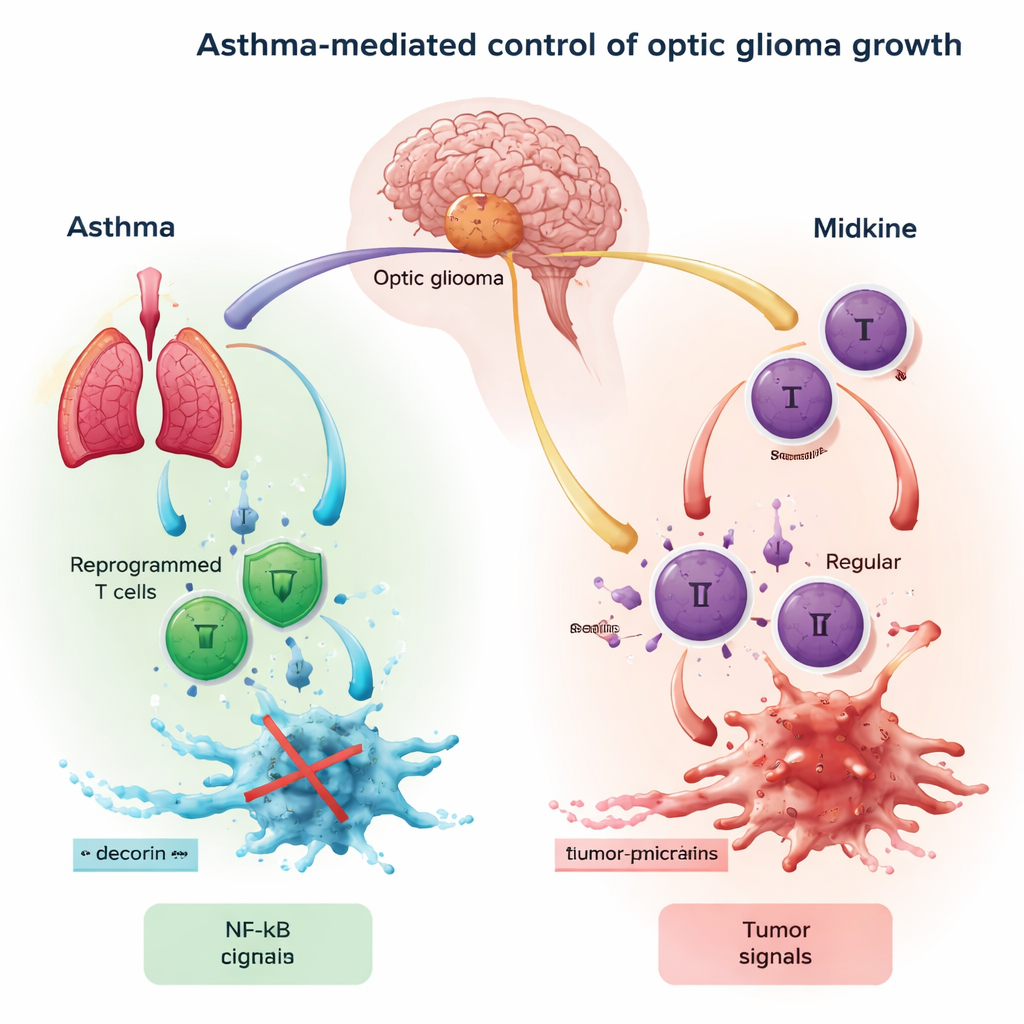
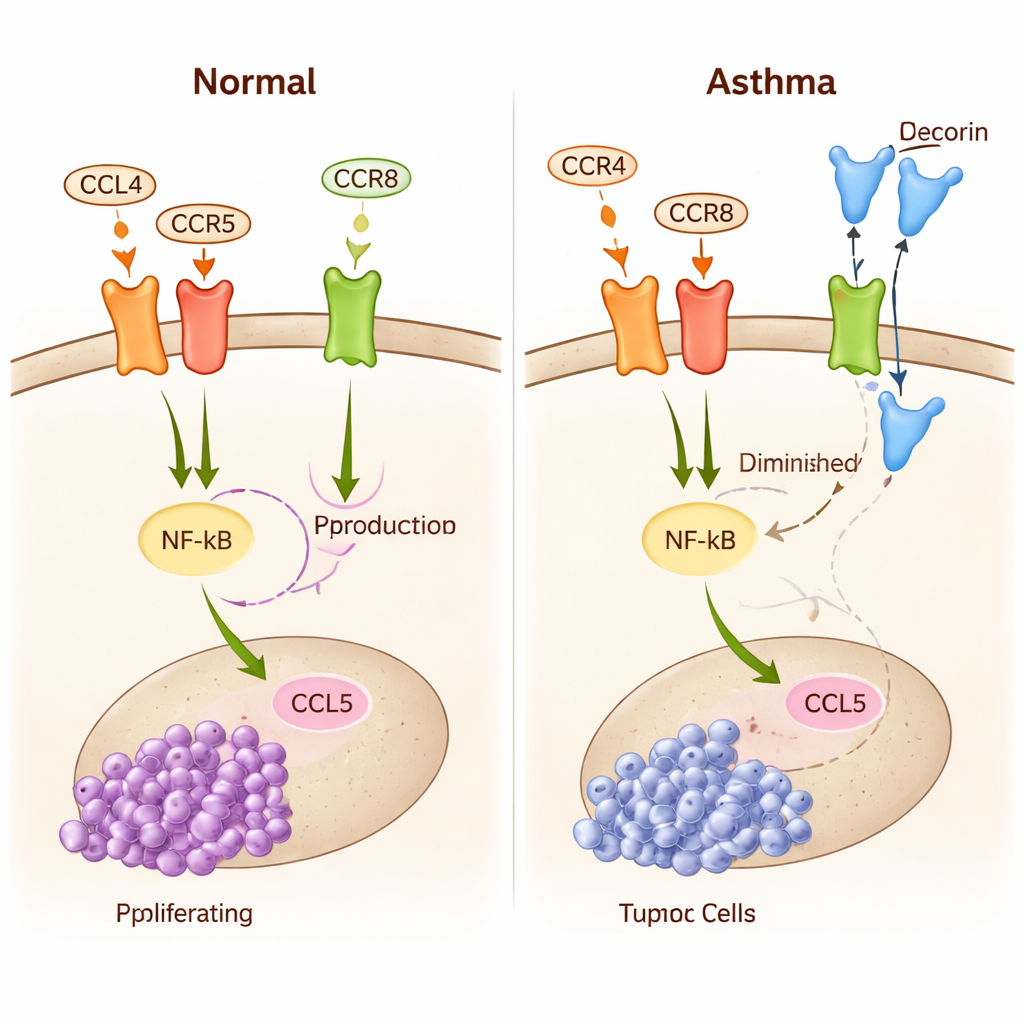
Autorzy skupiają się na łańcuchu zdarzeń łączącym nerw wzrokowy, komórki odpornościowe i wzrost guza. Midkina z nerwu wzrokowego najpierw aktywuje limfocyty T, rodzaj białych krwinek, skłaniając je do wydzielania sygnału zwanego CCL4. Ten sygnał wiąże się z receptorami (CCR5 i CCR8) na mikrogleju, będącym rodzimymi komórkami odpornościowymi mózgu. Gdy wystarczająca ilość CCL4 przyłącza się do tych receptorów, w mikrogleju uruchamiany jest główny przełącznik znany jako NF-κB. Po aktywacji NF-κB napędza produkcję kolejnego sygnału, CCL5, który zachęca komórki glejaka nerwu wzrokowego do wzrostu, migracji i unikania ataku immunologicznego. W efekcie oś midkina–CCL4–NF-κB–CCL5 tworzy obwód „startowy” sprzyjający ekspansji guza.
Jak astma przeprogramowuje limfocyty T, by hamowały guz
Astma jest powszechnie postrzegana jako choroba przewlekłego zapalenia dróg oddechowych. Jednak u osób z astmą niektóre limfocyty T ulegają „przeprogramowaniu” w inny stan: tracą dużą część swojej bezpośredniej zdolności niszczenia komórek, a zamiast tego wydzielają molekuły przekształcające otoczenie. Jedną z tych molekuł jest dekorina, małe białko o udokumentowanych właściwościach przeciwnowotworowych. Kluczowy pomysł tej pracy polega na tym, że limfocyty T „zaprzyjaźnione” z astmą mogą przemieszczać się z płuca do mózgu i uwalniać dekorinę w pobliżu glejaka nerwu wzrokowego. Dekorina konkuruje z CCL4 o receptor CCR8 na mikrogleju, skutecznie blokując część rozmowy, która karmi guz, i osłabiając NF-κB oraz produkcję CCL5 w komórkach odpornościowych mózgu.
Użycie matematyki do śledzenia niewidocznej sieci
Ponieważ ta sieć sygnalizacyjna jest zbyt skomplikowana, by pojąć ją intuicyjnie, badacze zbudowali szczegółowy model matematyczny wykorzystujący równania różniczkowe. Model śledzi poziomy kluczowych molekuł (midkina, CCL4, dekorina, NF-κB, CCL5), aktywność receptorów na mikrogleju oraz wzrost komórek guza w czasie. Wykorzystali dane eksperymentalne do skalibrowania siły poszczególnych interakcji, a następnie zasymulowali wiele scenariuszy. Model pokazuje, jak niewielkie zmiany w sile wiązania — jak łatwo CCL4 lub dekorina przyłączają się do swoich receptorów — mogą przełączyć mikroglej między dwoma trybami: stanem sprzyjającym guzowi z wysokim poziomem NF-κB i CCL5 oraz stanem hamującym guz z silnym wiązaniem dekoriny i słabymi sygnałami CCL4. Prosty wskaźnik oparty na stosunku receptorów związanych z dekoriną do receptorów związanych z CCL4 dokładnie przewiduje, czy guz ma tendencję do wzrostu czy zatrzymania.
Projektowanie mądrzejszych terapii opartych na układzie odpornościowym
Poza wyjaśnieniem, dlaczego astma może chronić przed glejakiem nerwu wzrokowego, model służy do badania strategii leczenia. Sugeruje, że terapie zwiększające poziomy dekoriny lub osłabiające przyczepność CCL4 do receptorów mogłyby spowolnić wzrost guza. Autorzy cyfrowo testują podejścia, takie jak wielokrotne podawanie limfocytów T produkujących dekorinę lub użycie przekaźnika immunologicznego IL-2 do ekspansji tych korzystnych komórek w organizmie. Co ciekawe, symulacje wykazują, że ważne jest nie tylko całkowite dawkowanie, lecz także jego rozłożenie w czasie: umiarkowane, odpowiednio rozłożone dawki mogą utrzymywać mikroglej w stanie hamującym guz równie skutecznie jak większe, rzadsze dawki, przy potencjalnie mniejszych skutkach ubocznych.
Co to oznacza dla pacjentów i rodzin
Dla osób niebędących specjalistami główne przesłanie jest takie, że przewlekłe zapalenie związane z astmą, zwykle postrzegane jako szkodliwe, czasem może przekształcić układ odpornościowy w sposób utrudniający rozwój niektórych guzów mózgu. Przez przekształcenie limfocytów T w fabryki dekoriny astma wydaje się przechylać równowagę w nerwie wzrokowym z środowiska sprzyjającego wzrostowi ku środowisku bardziej wrogiego nowotworowi. Nikt oczywiście nie sugeruje traktowania astmy jako terapii, ale mechanizmy odkryte w tym badaniu mogą zainspirować nowe leki kopiujące jej ochronne aspekty — wykorzystujące dopasowane terapie limfocytów T lub leki naśladujące blokujące działanie dekoriny — w celu ochrony dzieci zagrożonych glejakiem nerwu wzrokowego.
Cytowanie: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Słowa kluczowe: glejak nerwu wzrokowego, astma, dekorina, limfocyty T, modelowanie matematyczne