Clear Sky Science · pl
Postbiotyki Lacticaseibacillus paracasei klasy spożywczej hamują tworzenie biofilmu Streptococcus mutans w jamie ustnej i jego kariogenność
Walka z ubytkami przy pomocy składników pochodzących z żywności
Próchnica jest jednym z najpowszechniejszych problemów zdrowotnych na świecie, napędzana w dużej mierze przez bakterie uwielbiające cukier, które niszczą szkliwo. W tym badaniu analizuje się nowe podejście: zamiast polegać wyłącznie na silnych płukankach czy żywych „dobrych bakteriach” (probiotykach), moglibyśmy chronić zęby przy użyciu bezpiecznych, trwałych substancji wytworzonych przez przyjazne mikroby spożywcze. Badacze wykazują, że postbiotyki pochodzące od bakterii klasy spożywczej Lacticaseibacillus paracasei osłabiają kluczowego sprawcę próchnicy i jego lepką płytkę nazębną, wskazując drogę do nowych rodzajów produktów do pielęgnacji jamy ustnej i płukanek.
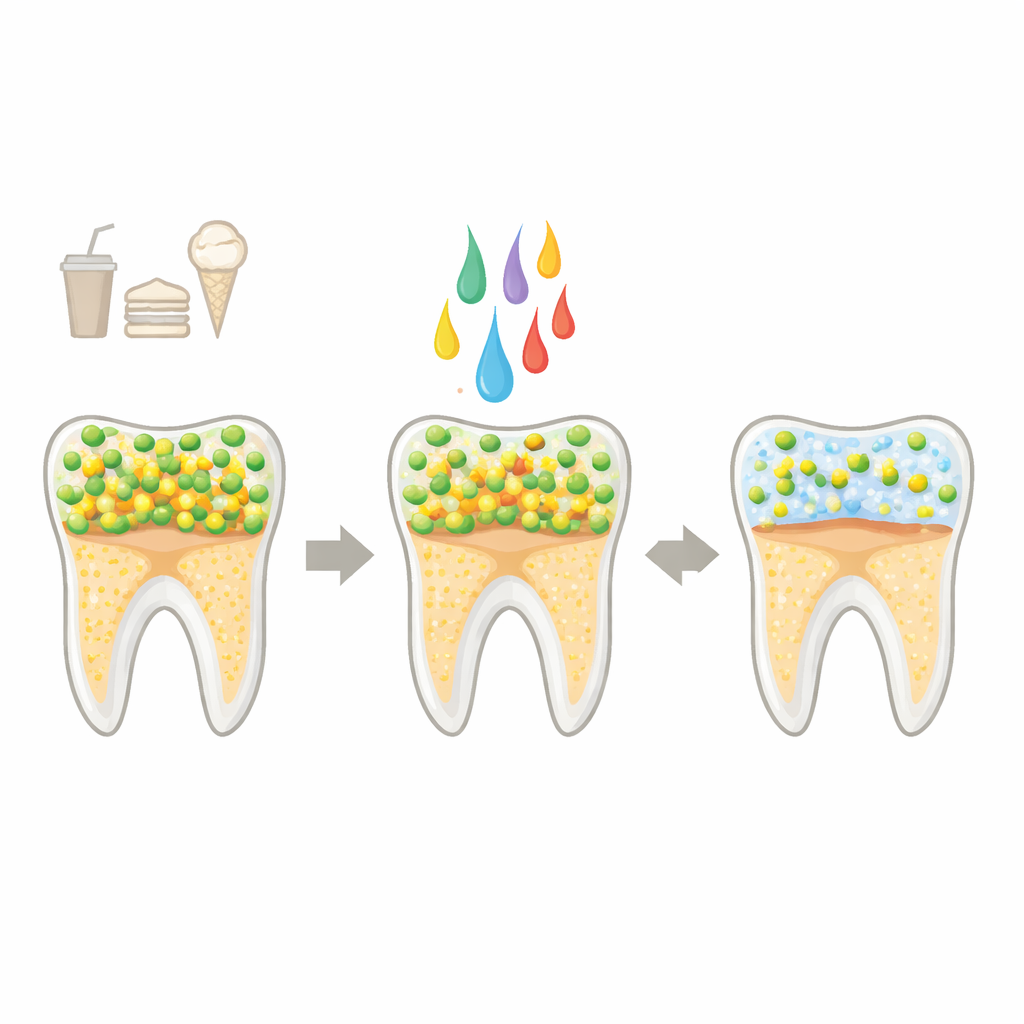
Sprawca próchnicy i nowy rodzaj sojusznika
Próchnica rozpoczyna się, gdy równowaga naturalnej społeczności jamy ustnej zostaje zaburzona. Częste spożycie cukru karmi bakterie produkujące kwasy, takie jak Streptococcus mutans, które tworzą grube, klejące warstwy (biofilmy) na zębach. Te biofilmy zatrzymują kwasy przy szkliwie, rozpuszczając minerały i w efekcie prowadząc do ubytków. Szczotkowanie, nitkowanie i chemiczne płukanki pomagają, ale trudno je stosować idealnie każdego dnia i mogą powodować skutki uboczne. Produkty probiotyczne z żywymi bakteriami są obiecujące, ale rodzą pytania dotyczące stabilności, przechowywania i bezpieczeństwa. Postbiotyki — nieaktywne preparaty wykonane z korzystnych bakterii lub ich wydzielin — oferują rozwiązanie pośrednie: mogą być klasy spożywczej, długotrwałe i łatwiejsze w użyciu, jednocześnie kierując szkodliwe mikroby w zdrowszym kierunku.
Jak postbiotyki osłabiają szkodliwe bakterie jamy ustnej
Zespół skoncentrował się na pozakomórkowym supernatancie (CFS) z L. paracasei, zasadniczo bulionie pozostałym po usunięciu bakterii. Testowali, jak ten płyn wpływa na S. mutans unoszący się wolno i rozwijający się w biofilmach. W hodowlach laboratoryjnych CFS niemal całkowicie zatrzymał namnażanie S. mutans. Pod mikroskopem elektronowym komórki po traktowaniu wyglądały pomarszczone i uszkodzone, z chropowatymi powierzchniami i odłamkami. Pomiary przepływowe potwierdziły, że ich błony stały się przeciekające, wewnętrzna równowaga elektryczna uległa załamaniu, a znacznie mniej komórek pozostało metabolicznie aktywnych. CFS także uczynił powierzchnię bakterii mniej hydrofobową, co jest istotne, ponieważ bardziej przylegające, hydrofobowe komórki łatwiej przywierają do zębów i do siebie podczas tworzenia płytki.
Rozbijanie lepkiej płytki i ochrona szkliwa
Kiedy S. mutans tworzył biofilmy, postbiotyki nadal wywierały silny efekt. CFS zmniejszał ogólną masę biofilmu, a skoncentrowana postać redukowała ją jeszcze bardziej. Bakterie wewnątrz tych warstw rosły słabo, tworzyły krótsze łańcuchy i produkowały mniej cukrowej „klejącej” substancji (egzopolisacharydów), która nadaje płytce strukturę. Obrazowanie trójwymiarowe ujawniło cieńsze, bardziej nieciągłe biofilmy z mniejszą liczbą żywych, nienaruszonych komórek i osłabioną matrycą. Aby odtworzyć warunki zbliżone do prawdziwych zębów, badacze hodowali S. mutans na syntetycznych dyskach szkliwa pokrytych ludzkim śliną, a następnie poddawali je cyklom „dokarmiania” i „płukania” za pomocą CFS, standardowej płukanki (chlorheksydyna) lub roztworu kontrolnego. Biofilmy traktowane CFS były gładsze i jaśniejsze, a co najważniejsze — uwalniały mniej wolnego wapnia ze szkliwa, co jest bezpośrednim wskaźnikiem zmniejszonej demineralizacji zęba, mimo że otaczający płyn pozostawał dość kwaśny.
Wgląd w molekularne strategie
Aby ustalić, co w CFS odpowiada za efekt, naukowcy selektywnie unieczynniali kandydatów. Rozkładanie białek, usuwanie nadtlenku wodoru czy dodanie wyekstrahowanych cukrów z bulionu nie zmieniało w znaczący sposób działania przeciwbakteryjnego. Natomiast zobojętnienie jego kwaśności wyraźnie osłabiło moc, co sugeruje, że kluczową rolę odgrywają kwasy organiczne. Kwasy te to nie tylko niskie pH: podobne zakwaszenie uzyskane jedynie kwasem mineralnym nie tłumiło S. mutans tak skutecznie, co wskazuje na współdziałanie konkretnych mieszanin kwasów organicznych. Zespół następnie zbadał, które geny bakteryjne i małe cząsteczki zmieniały ekspresję przy wzroście S. mutans w obecności CFS. Stwierdzono obniżoną aktywność genów związanych z przyleganiem, produkcją „kleju”, odpornością na stres oraz systemami komunikacji bakteryjnej (quorum sensing), które koordynują zachowania grupowe. Niektóre metabolity, takie jak kreatyna i fosfoenolopirogronian, zmieniały się w sposób zgodny z mniejszą produkcją kwasów i osłabioną zjadliwością, pomagając wyjaśnić, dlaczego tracono mniej minerałów szkliwa.
Co to może znaczyć dla codziennej pielęgnacji jamy ustnej
Mówiąc wprost, praca ta pokazuje, że bezpieczne, klasy spożywczej postbiotyki z L. paracasei mogą nadrywać pancerz kluczowego szczepu powodującego próchnicę, przerzedzać jego płytkę, osłabiać obronę i zmniejszać uszkodzenia szkliwa przypominającego zęby. Ponieważ te postbiotyki są odporne na ciepło, przechowywanie i różne warunki, można je byłoby łączyć w pastylki do ssania, płukanki lub żywność funkcjonalną jako łagodna, długotrwała pomoc obok szczotkowania i nitkowania. Nie zastępują one dobrej higieny jamy ustnej ani regularnych wizyt u dentysty, ale wskazują na przyszłość, w której inteligentne, pochodzące z żywności składniki cicho przekształcają mikroskopijną społeczność w ustach, aby dłużej utrzymać zęby w lepszym stanie.
Cytowanie: Luo, SC., Hu, PF., Wei, SM. et al. Food-grade Lacticaseibacillus paracasei postbiotics suppress oral Streptococcus mutans biofilm formation and cariogenicity. npj Sci Food 10, 89 (2026). https://doi.org/10.1038/s41538-026-00742-6
Słowa kluczowe: próchnica, mikrobiom jamy ustnej, postbiotyki, Streptococcus mutans, żywność funkcjonalna