Clear Sky Science · pl
Strategia z małymi cząsteczkami: forskolina i inhibitor p38 do ekspansji komórek macierzystych mięśni w medium bezsurowiczym
Hodowanie mięsa bez zwierząt
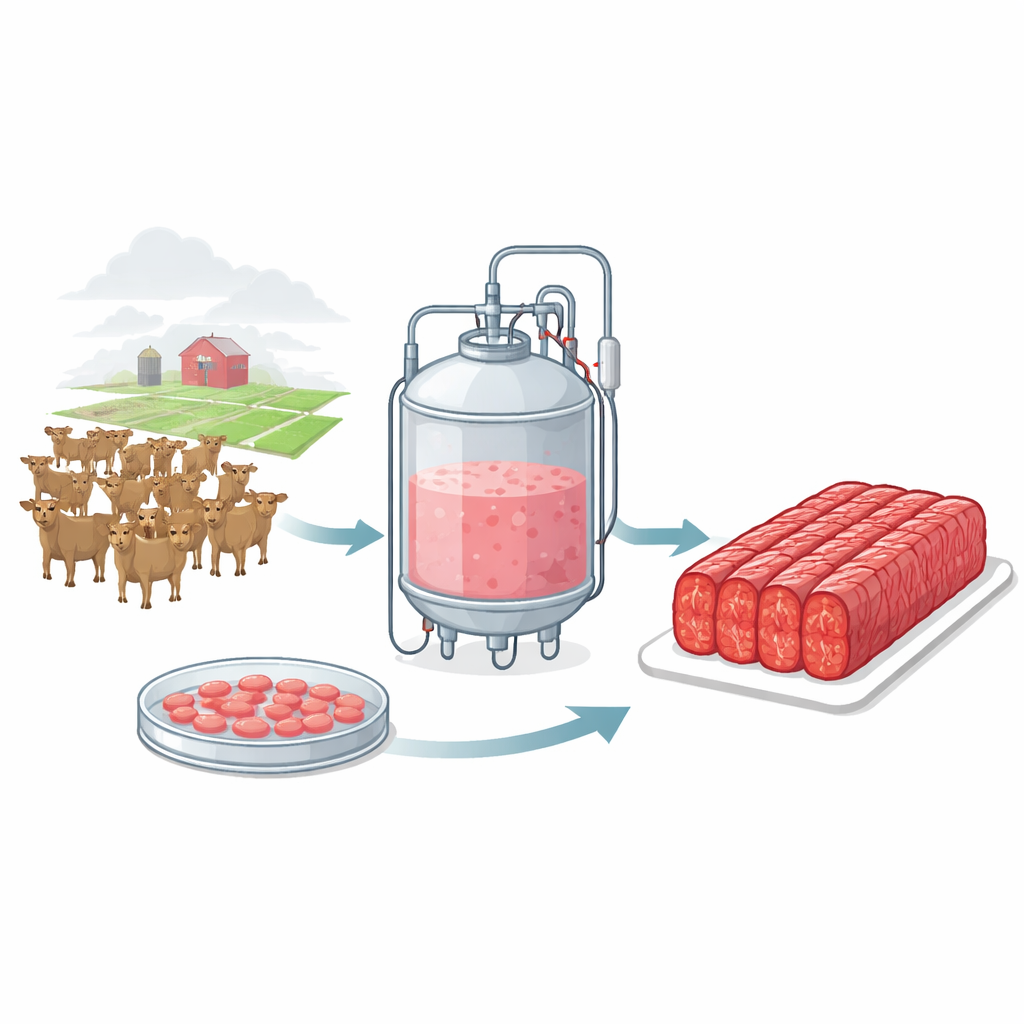
Wyobraź sobie soczysty stek, który nigdy nie pochodził z zabitej krowy. Mięso hodowane ma na celu namnażanie prawdziwych komórek mięśniowych w stalowych zbiornikach zamiast na farmie, obiecując znaczne ograniczenie zużycia ziemi, emisji i cierpienia zwierząt. Jednym z głównych problemów pozostaje jednak sposób odżywiania tych komórek w sposób przystępny cenowo, powtarzalny i wolny od produktów pochodzenia zwierzęcego. W tym badaniu zaproponowano nowy przepis, wykorzystujący tylko dwie starannie dobrane małe cząsteczki, które pomagają młodym bydlnym komórkom mięśniowym intensywnie się mnożyć w całkowicie medium bezsurowiczym, przybliżając wołowinę hodowaną do realiów skali przemysłowej.
Dlaczego zastąpienie surowicy ma znaczenie
Obecnie większość komórek zwierzęcych wykorzystywanych w badaniach lub prototypach żywności hoduje się w płynnych mieszankach wzbogaconych o surowicę płodową bydła, składnik pozyskiwany od nienarodzonych cieląt. Surowica jest silnym stymulantem, ale problematycznym: jest droga, zmienna między partiami, może przenosić patogeny i budzi poważne wątpliwości etyczne. Naukowcy zaczęli opracowywać media bezsurowicze, zastępując surowicę precyzyjnie zdefiniowanymi składnikami, ale te mieszanki często wciąż są kosztowne i nie dorównują zdolności surowicy do napędzania szybkiego, długotrwałego wzrostu komórek. Aby mięso hodowane mogło konkurować z tradycyjną wołowiną, potrzebny jest prostszy, tańszy sposób utrzymania podziałów komórek macierzystych mięśni bez utraty ich zdolności do różnicowania się w dojrzałe włókna mięśniowe.
Sprytne skróty z małymi pomocniczymi cząsteczkami
W tej pracy zespół skupił się na bydlnych komórkach macierzystych mięśni — podstawowych jednostkach, które potrafią zarówno samoodnawiać się, jak i tworzyć nową tkankę mięśniową. Badacze rozpoczęli od istniejącego bezsurowicznego medium dla tych komórek i przesiewali 24 różne małe cząsteczki znane z wpływu na wzrost, podziały lub specjalizację komórek. Po krótkoterminowych testach i kilkukrotnych pasażach jeden kandydat wyróżnił się: forskolina, związek roślinny zwiększający wewnątrzkomórkowy drugi przekaźnik cAMP. W starannie dobranej niskiej dawce forskolina pozwalała komórkom zachować typowy zaokrąglony kształt macierzysty, zwiększała aktywność genów miogenicznych definiujących tożsamość mięśniową i, co istotne, powodowała szybsze dzielenie się komórek przez wiele rund hodowli. Naukowcy nazwali to medium wzbogacone o forskolinę „Beefy‑F”. W ciągu sześciu pasaży Beefy‑F wyprodukowało prawie dwa razy więcej komórek niż oryginalne medium bezsurowicze i osiągnęło plony porównywalne z tradycyjnymi hodowlami na surowicy, przy zachowaniu zdolności komórek do łączenia się w przypominające mięsień włókna.
Dodanie drugiego wzmocnienia dla jeszcze szybszego wzrostu
Po zidentyfikowaniu obiecującej bazy badacze sprawdzili, czy inne związki mogą współdziałać z forskoliną, by jeszcze bardziej przyspieszyć wzrost. Testowali kilka inhibitorów szlaków sygnałowych, które zwykle spowalniają lub kierują zachowaniem komórek, w tym dwa blokujące stresowo‑odpowiedź zwaną p38 MAPK. Jednym z nich, SB202190, okazał się najlepszym partnerem. Gdy 1 mikromolowy SB202190 dodano do Beefy‑F, tworząc medium „Beefy‑F + S”, bydle komórki macierzyste mięśni rozszerzały się znacznie szybciej niż w pozostałych mieszankach. Po trzech pasażach Beefy‑F + S dało około 60 procent więcej komórek niż oryginalny bezsurowiczy kontrolnik i około 30 procent więcej niż sama forskolina lub sam inhibitor p38. Komórki pozostały zdrowe i zwarte, wykazywały wyższy poziom PAX7 — markera „macierzystości” — i nadal tworzyły liczne, dobrze zorganizowane włókna mięśniowe w kilku różnych bezsurowiczych warunkach różnicowania.
Co dzieje się wewnątrz komórek
Aby zrozumieć zmiany zachodzące w komórkach, zespół porównał aktywność genów w pięciu warunkach hodowli: standardowa surowica, bazowe medium bezsurowicze, forskolina sama, hamowanie p38 samo oraz połączony system Beefy‑F + S. Sekwencjonowanie RNA obejmujące cały genom wykazało, że media bezsurowicze, szczególnie te zawierające forskolinę, utrzymywały silne wytwarzanie genów definiujących tożsamość mięśniową. Jednocześnie inhibitor p38 silnie zwiększał ekspresję genów zaangażowanych w cykl komórkowy, ułatwiając komórkom przechodzenie przez podziały. Razem, w Beefy‑F + S, oba te efekty łączyły się: geny tożsamości mięśniowej pozostawały wysokie, podczas gdy programy dzielenia komórek były wzmocnione. Komórki dodatkowo przebudowywały swoje otoczenie, tłumiąc ekspresję kilku genów kolagenowych i zwiększając czynniki pomagające rozkładać nadmiar macierzy — co sugeruje, że tworzyły bardziej elastyczne mikrośrodowisko sprzyjające stałemu wzrostowi.
Co to oznacza dla przyszłości mięsa hodowanego
Mówiąc wprost, badanie pokazuje, że prosta strategia dwuskładnikowa może w dużej mierze zastąpić surowicę zwierzęcą przy hodowli bydlnych komórek macierzystych mięśni. Forskolina pomaga komórkom „pamiętać”, że są prekursorami mięśni, natomiast inhibitor p38 zachęca je do szybkiego mnożenia i dostosowywania interakcji z otoczeniem. Powstałe medium Beefy‑F + S jest stosunkowo tanie w przygotowaniu, zwiększa plon komórek ponad półtora raza w porównaniu z wcześniejszymi opcjami bezsurowiczymi i utrzymuje zdolność komórek do tworzenia tkanki mięśniowej — co jest kluczowe, by przekształcić je w jadalne mięso. Chociaż potrzebne są dalsze prace nad zastąpieniem składników w pełni spożywczymi oraz testami z większą liczbą dawców zwierzęcych, podejście oparte na małych cząsteczkach oferuje praktyczny plan skalowania hodowli komórek bez surowicy, przybliżając wołowinę hodowaną do sklepowych półek.
Cytowanie: Lu, H., Liu, Z., Liu, X. et al. A small molecule strategy with forskolin and p38 inhibitor for serum-free muscle stem cell expansion. npj Sci Food 10, 81 (2026). https://doi.org/10.1038/s41538-026-00732-8
Słowa kluczowe: mięso hodowane, medium bez surowicy, komórki macierzyste mięśni, forskolina, inhibitor p38