Clear Sky Science · pl
Metabolomika wspomagana uczeniem maszynowym odszyfrowuje adaptacyjne przebudowy biofilmów Bacillus w odpowiedzi na stres pasteryzacji
Dlaczego pijący mleko powinni się tym zainteresować
Mleko pasteryzowane ma być bezpieczne i trwałe, jednak niektóre odporne bakterie potrafią przetrwać obróbkę cieplną i po cichu tworzyć śliskie społeczności — zwane biofilmami — wewnątrz urządzeń przetwórczych. Badanie stawia niepokojące, a jednocześnie praktyczne pytanie: czy pasteryzacja czasem może pogorszyć te biofilmy, a jeśli tak, to jakie ukryte zmiany chemiczne wewnątrz bakterii są tego przyczyną?
Uparte mikropy w nowoczesnych zakładach mleczarskich
Mleko jest bogate w składniki odżywcze i zasila rozwijający się sektor produktów chłodzonych i niskotemperaturowych. Jednocześnie stanowi siedlisko dla Bacillus — grupy bakterii tworzących twarde przetrwalniki i przyczepiających się do powierzchni metalowych. Mikroorganizmy te tworzą biofilmy — ochronne warstwy komórek i lepka substancji — które opierają się czyszczeniu, utrudniają wymianę ciepła i zwiększają ryzyko zepsucia albo chorób przenoszonych przez żywność. Autorzy wyizolowali 14 szczepów Bacillus z surowego mleka na chińskich farmach i zbadali, jak dobrze tworzyły biofilmy przed i po symulowanej pasteryzacji w 75 °C przez 15 sekund. Zaskakująco, podczas gdy wiele szczepów tworzyło słabsze biofilmy po ogrzewaniu, kilka z nich stało się w rzeczywistości silniejszymi i bardziej lepkimi budowniczymi.
Ciepło, które wzmacnia niektóre biofilmy, a osłabia inne
Aby naśladować rzeczywiste wyposażenie mleczarni, badacze hodowali wybrane szczepy na płytkach ze stali nierdzewnej 304 zanurzonych w sterylnym mleku. Następnie barwili i mierzyli całą pozostałą warstwę — bakterie wraz z resztkami mleka — na metalu. Dwa szczepy, jeden Bacillus cereus (BC01) i jeden Bacillus subtilis (BS01), przesunęły się z słabej do silnej adhezji po pasteryzacji, podczas gdy blisko spokrewnione odmiany (BC02 i BS02) wykazały przeciwny trend. Obrazy z mikroskopu elektronowego ukazały, jak zmieniła się architektura biofilmu: w szczepach wzmocnionych przez ciepło zwykła cienka włóknista sieć substancji pozakomórkowych zlewała się w grube, blokowe agregaty, które zatrzymywały więcej komórek i białek mleka, tworząc twardszą, bardziej rozległą powłokę. W szczepach osłabionych przez ciepło macierz stała się rzadka i fragmentaryczna.
Gdy lepkość powierzchni łamie zasady
Konwencjonalna wiedza głosi, że im bardziej przetrwalnik odpycha wodę (jest hydrofobowy), tym lepiej się przyczepia i łatwiej tworzy biofilm. Zespół przetestował hydrofobowość przetrwalników przy użyciu układu olej‑woda i odkrył wynik odwrotny do podręcznikowych przewidywań. Po pasteryzacji szczepy, które zyskały na sile biofilmu, wykazywały niższą hydrofobowość przetrwalników, natomiast te, które utraciły zdolność do tworzenia biofilmu, stały się bardziej hydrofobowe. Nawet wewnątrz biofilmów przetrwalniki silnych formujących były mniej hydrofobiczne niż ich wolno pływające odpowiedniki. Ta sprzeczność wskazywała na głębszy czynnik: indukowane ciepłem zmiany w metabolizmie i aktywności genów, które mogą przeważać nad prostymi właściwościami fizycznymi, takimi jak lepkość powierzchni.
Chemiczne przebudowanie pod wpływem stresu cieplnego
Wykorzystując nieukierunkowaną metabolomikę — szerokie badanie małych cząsteczek wewnątrz komórek — w połączeniu z analizą uczenia maszynowego, autorzy odwzorowali, jak ciepło przekształciło chemię biofilmu każdego szczepu. Wszystkie cztery szczepy wykazały duże zmiany w setkach metabolitów, zwłaszcza w układach transportowych i szlakach aminokwasowych, ale szczegóły znacznie się różniły. W BC01 ogrzewanie wydawało się aktywować enzym zwany glutaminazą, co opróżniało pulę mlecznego składnika L‑glutaminy i aminokwasu histydyny. Ta zmiana dostarczała zarówno cegieł budulcowych dla matrycy biofilmu, jak i znosiła naturalne hamulce tworzenia biofilmu. Stężenia ksantozyny, związku który zwykle skłania bakterie do unikania biofilmów, również spadły, co prawdopodobnie sprzyjało stabilnemu, przyczepionemu stylowi życia. W BS01 ciepło zmniejszyło poziomy argininy i kilku D‑aminokwasów, dopaminy i kwasu arachidonowego — cząsteczek, które w innych badaniach destabilizowały biofilmy lub blokowały ich formowanie. Niższe ilości tych inhibitorów, wraz ze zmienionym metabolizmem energetycznym, przesunęły równowagę w stronę bardziej odpornych biofilmów. Dla porównania, BC02 i BS02 doświadczyły niedoborów kluczowych prekursorów polisacharydów i składników cyklu energetycznego, a w BS02 zwiększyły się antybiofilmowe metabolity, takie jak D‑tryptofan i D‑arabinoza, co łącznie osłabiło wzrost biofilmu.
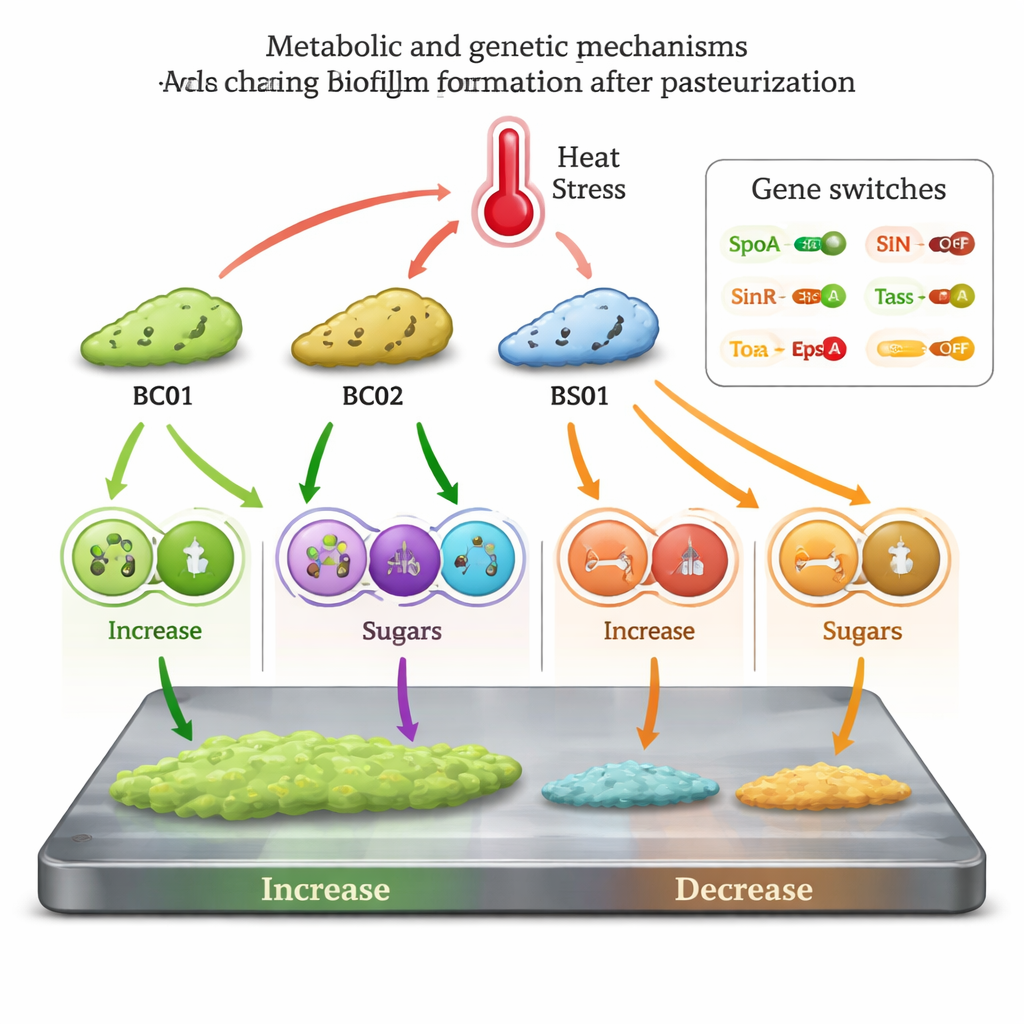
Geny, które przełączają tworzenie biofilmu
Aby powiązać chemię z zachowaniem, zespół zmierzył kluczowe geny związane z biofilmem. W szczepach wzmocnionych przez ciepło, BC01 i BS01, regulatorzy główni promujące tworzenie biofilmu (Spo0A, TasA i EpsA) były podwyższone, podczas gdy SinR, gen który zwykle hamuje geny biofilmu, był wyciszony. Przeciwna mozaika pojawiła się w BC02 i BS02. Razem dane metaboliczne i odczyty genetyczne wspierają model, w którym pasteryzacja działa jako sygnał stresowy, z którego niektóre linie Bacillus potrafią skorzystać: przełączają swój metabolizm, pozbywają się pewnych naturalnych anty‑biofilmowych cząsteczek i odwracają genetyczne przełączniki, aby produkować więcej matrycy i grubsze powłoki, nawet gdy ich ogólna aktywność spada.
Co to oznacza dla bezpieczniejszego mleka
Dla konsumentów przekaz nie brzmi: mleko pasteryzowane jest niebezpieczne, lecz że drobnoustroje, które przetrwają obróbkę cieplną, mogą być bardziej adaptowalne, niż się spodziewano. Zamiast jedynie wzmacniać przetrwalniki, pasteryzacja może skierować niektóre szczepy Bacillus w tryb „przyczepienia się”, w którym budują mocniejsze biofilmy wewnątrz rur i zbiorników. Identyfikując konkretne metabolity i ścieżki genetyczne napędzające tę zmianę, badanie sugeruje nowe sposoby przeciwdziałania: zamiast polegać wyłącznie na wyższej temperaturze lub dłuższym ogrzewaniu, przetwórcy mogliby w przyszłości stosować łagodne blokery metaboliczne lub dopasowane procedury czyszczenia, które zakłócają chemiczne zaplecze tych biofilmów. W istocie zrozumienie, jak ciepło przekształca chemię bakterii, otwiera drogę do mądrzejszych strategii utrzymania produktów mlecznych zarówno pożywnych, jak i czystych.
Cytowanie: Liang, L., Wang, P., Zhao, X. et al. Metabolomics aided by machine learning decodes adaptive remodeling of Bacillus biofilms in response to pasteurization stress. npj Sci Food 10, 62 (2026). https://doi.org/10.1038/s41538-026-00712-y
Słowa kluczowe: mleko pasteryzowane, biofilmy Bacillus, bezpieczeństwo żywności, przetwórstwo mleczarskie, metabolizm bakteryjny