Clear Sky Science · pl
Hamowanie CDK8 ratuje upośledzone gojenie złamań niedokrwiennych
Dlaczego przepływ krwi ma znaczenie przy złamaniach
Większość złamań ostatecznie zrasta się sama, ale u milionów ludzi każdego roku ten proces się zatrzymuje. Słabe ukrwienie wokół złamania — zwane niedokrwieniem — znacząco zwiększa ryzyko, że pęknięcie będzie goić się wolno, nieprawidłowo lub wcale. W badaniu tym analizowano, dlaczego tak się dzieje na poziomie komórkowym, oraz testowano eksperymentalną tabletkę, która wydaje się przesuwać organizm z trybu bliznowatej naprawy z powrotem w kierunku prawdziwej regeneracji kości.
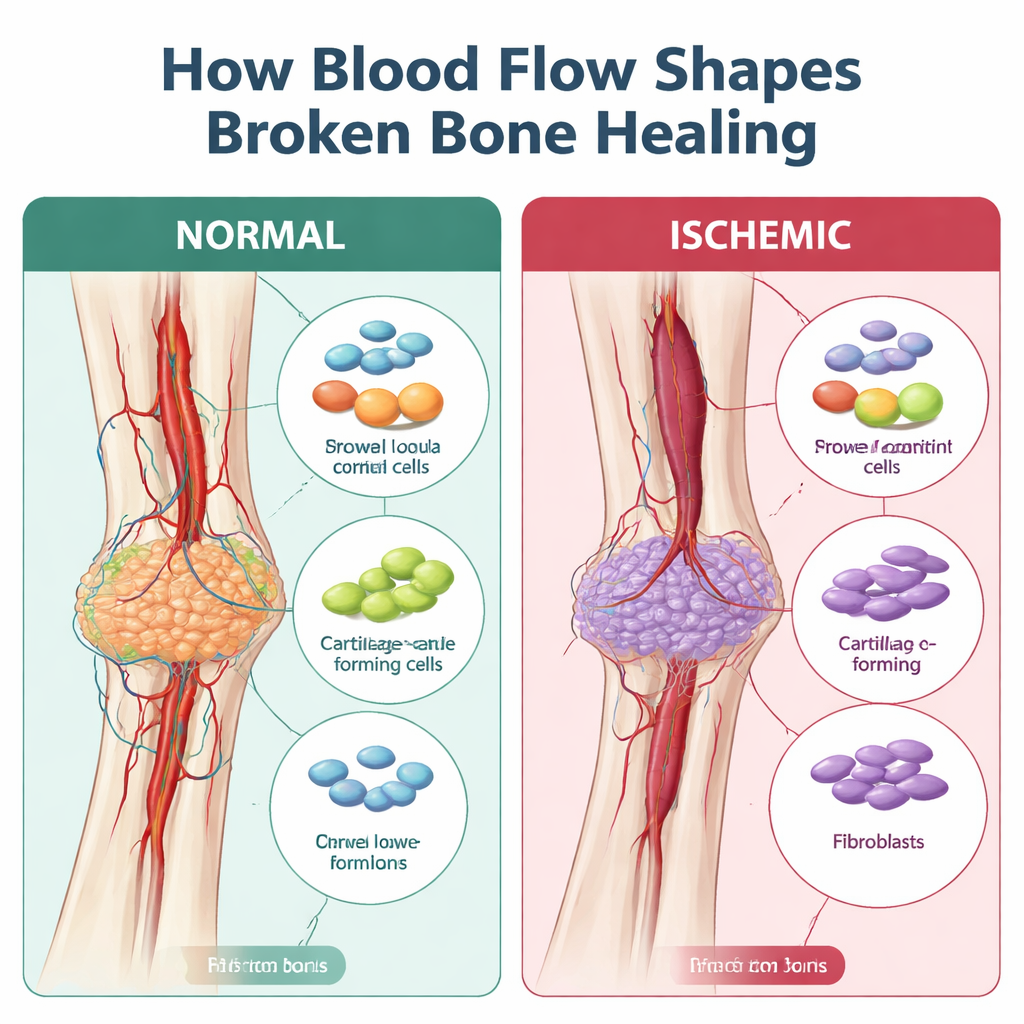
Kiedy gojenie zamienia się w bliznę zamiast odbudowy
Kość zwykle goi się przez zbudowanie miękkiego mostka z chrząstki, który stopniowo zostaje zastąpiony twardą kością. Ten mostek, zwany kostnieniem okołozłamanowym (callus), zależy od dostaw komórek macierzystopodobnych, komórek odpornościowych i naczyń krwionośnych koordynujących naprawę. W złamaniach niedokrwiennych wcześniejsze prace wykazały, że callus bywa mniejszy, słabszy i wypełniony tkanką włóknistą — bardziej przypominającą bliznę niż solidną łatę nowej kości. Brakowało jednak szczegółowej mapy, które komórki zawodziły i kiedy w trakcie tego odchylenia od prawidłowego gojenia.
Pojedyncze komórki ujawniają odchylenie ku włóknieniu
Naukowcy zastosowali model myszy, w którym tętnica nogi jest chirurgicznie uszkadzana w momencie złamania, co wiernie odtwarza utratę przepływu krwi obserwowaną przy poważnych urazach lub u osób z chorobami naczyń czy palących. Następnie użyli sekwencjonowania RNA pojedynczych komórek — techniki odczytującej aktywne geny w tysiącach pojedynczych komórek — w callusach cztery i siedem dni po urazie. W dobrze ukrwionych złamaniach wczesny callus był pełen komórek odpornościowych, które wkrótce ustępowały miejsca ekspandującym komórkom zrębowym — komórkom podporowym, które przekształcają się w chrząstkę i kość. W warunkach niedokrwiennych było jednak znacznie mniej komórek tworzących chrząstkę i kość oraz znacznie więcej fibroblastów — komórek odkładających tkankę włóknistą. Analiza trajektorii komputerowej wykazała, że zamiast płynnie dojrzewać od wczesnych progenitorów do chrząstki, komórki zrębowe w kości niedokrwiennej często kierowały się przez stan podobny do fibroblastów, co odpowiada bardziej bliznowatemu callusowi widocznemu w mikroskopie.
Molekularny hamulec dla komórek budujących kość
Zgłębiając aktywność genów w tych komórkach, zespół odnalazł silny sygnał stresu komórkowego w callusach niedokrwiennych, w tym wysokie poziomy białek szoku cieplnego. Jedną z najbardziej uderzających zmian był wzrost aktywności genu o nazwie Cdk8, który koduje enzym regulatorowy będący częścią dużego kompleksu transkrypcyjnego i może spowalniać lub przekierowywać odpowiedzi komórek na sygnały. Cdk8 był wcześniej znany z blokowania różnicowania w innych kontekstach. Tutaj był szczególnie podwyższony we wczesnych progenitorach zrębowych w kości niedokrwiennej. Ludzkie mezenchymalne komórki zrębowe hodowane w warunkach niskiego tlenu — naśladujących słabe ukrwienie — również zwiększały ekspresję CDK8, łącząc niedobór tlenu bezpośrednio z tym potencjalnym „hamulcem” dla tworzenia chrząstki i kości.
Wyłączenie CDK8 przywraca naprawę
Następnie badacze sprawdzili, czy zablokowanie CDK8 może uwolnić komórki zrębowe, by wznowiły prawidłowe gojenie. W hodowlach komórkowych leczenie mysich i ludzkich komórek progenitorowych selektywnymi inhibitorami CDK8 zwiększało ekspresję kluczowych genów chrząstki i podnosiło produkcję macierzy chrząstkowej, a także zwiększało mineralizację, gdy te same komórki były kierowane ku tworzeniu kości. Zespół przetestował następnie doustnie dostępny inhibitor CDK8/19 nazwany SNX631-6 u myszy ze złamaniami niedokrwiennymi. Podawany w wczesnym okresie formowania chrząstki, lek zwiększał ilość chrząstki w callusie. Gdy leczenie przedłużono na późniejszy etap przejścia od chrząstki do kości, callusy wykazywały więcej całkowitej tkanki kostnej, wyższą zawartość minerałów i większe rozmiary w skanach mikro-CT oraz w przekrojach tkankowych, co wskazuje na bardziej solidną naprawę strukturalną.
Od laboratoryjnego wglądu do możliwych terapii
Podsumowując, wyniki sugerują, że niedokrwienie kieruje komórki gojące ku zestresowanemu, włókniejącemu losowi częściowo przez zwiększenie aktywności CDK8, który ogranicza ich zdolność do przekształcania się w chrząstkę i kość. Zablokowanie tego enzymu zdaje się zwalniać ten hamulec, pozwalając na powstanie większej ilości chrząstki we wczesnej fazie i na odkładanie większej ilości tkanki kostnej w fazie późniejszej, nawet przy ograniczonym dopływie krwi. Ponieważ inhibitory CDK8 są już testowane u pacjentów onkologicznych, mogłyby pewnego dnia zostać przekierowane do pomocy osobom o wysokim ryzyku złego gojenia złamań — takim jak starsi dorośli, palacze czy chorzy naczyniowo — by odrastali mocną kość zamiast kruchej tkanki bliznowatej.
Cytowanie: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Słowa kluczowe: gojenie złamań kości, niedokrwienie, inhibitor CDK8, mezenchymalne komórki zrębowe, fibroza