Clear Sky Science · pl
Przeszczepienie prawidłowych pęcherzykowych komórek nabłonkowych typu II u myszy pozbawionych białka surfaktantu C
Dlaczego naprawa maleńkich pęcherzyków ma znaczenie
Oddychanie może wydawać się bezwysiłkowe, ale zależy od delikatnej warstewki zwanej surfaktantem, która pokrywa miliony drobnych pęcherzyków płucnych. Gdy surfaktant jest nieobecny lub wadliwy, jak w niektórych rzadkich chorobach płuc u dzieci, pacjenci mogą cierpieć z powodu uporczywych problemów z oddychaniem i bliznowacenia płuc. Obecnie jedynym prawdziwym lekarstwem jest przeszczep płuca — opcja ograniczona dostępnością dawców i poważnymi ryzykami. W tym badaniu badacze rozważają inną ideę: naprawę uszkodzonych płuc poprzez przeszczepienie zdrowych komórek wytwarzających surfaktant, co potencjalnie otwiera drogę do łagodniejszych, bardziej ukierunkowanych terapii.
Gdy opiekunowie płuc zawodzą
W każdym pęcherzyku (alveolus) żyją wyspecjalizowane „komórki opiekuńcze” zwane pęcherzykowymi komórkami typu II. Produkują i odzyskują surfaktant, który zapobiega zapadaniu się pęcherzyków i ułatwia oddychanie. U niektórych dzieci mutacje w genach niezbędnych do produkcji surfaktantu, w tym w genie surfaktantowego białka C (SFTPC), zaburzają funkcję tych komórek. W efekcie pojawia się dziecięca śródmiąższowa choroba płuc (chILD), charakteryzująca się zapaleniem, pogrubieniem tkanki płucnej, bliznowaceniem i czasem niewydolnością oddechową. Lekarze mogą zaoferować jedynie leczenie wspomagające i tlen; dla najbardziej dotkniętych ostatnią deską ratunku pozostaje przeszczep płuca. Autorzy postanowili sprawdzić, czy zastąpienie części wadliwych komórek opiekuńczych zdrowymi mogłoby spowolnić lub odwrócić uszkodzenia płuc.
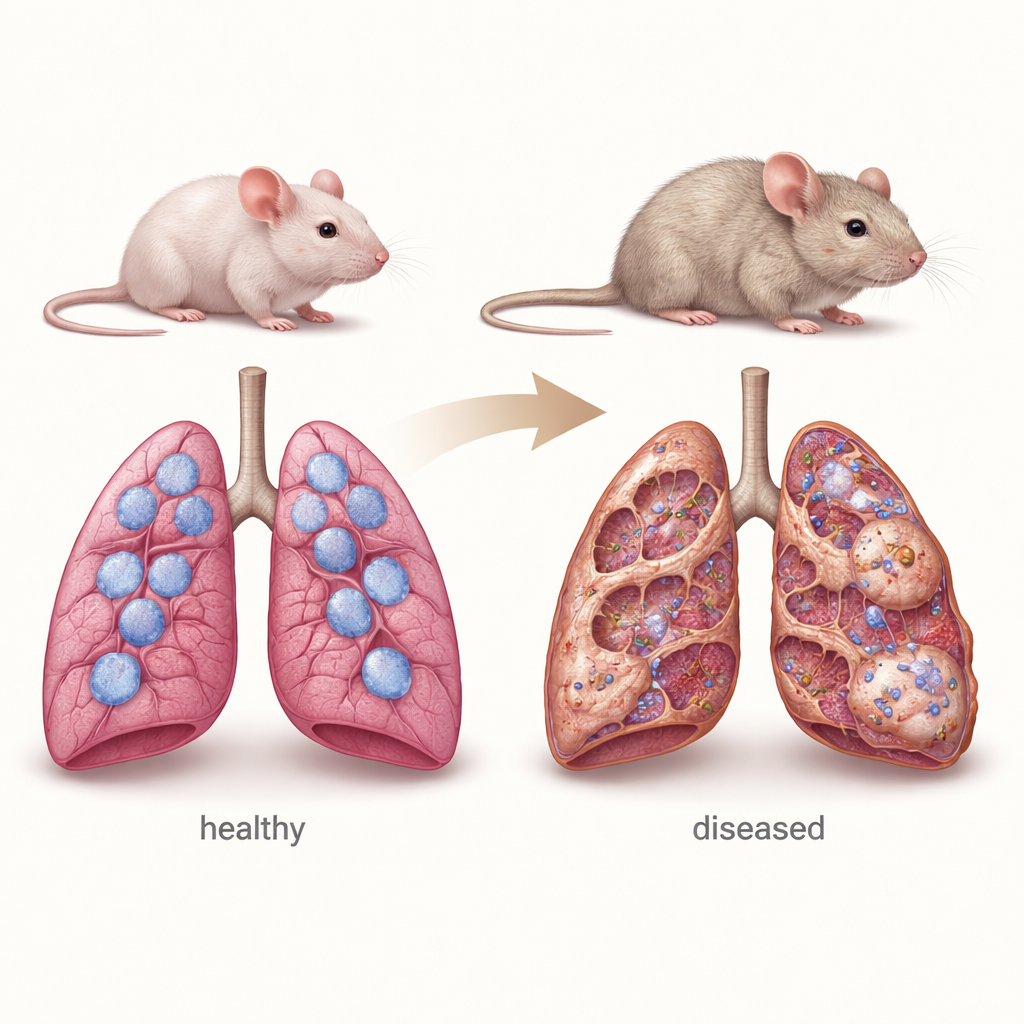
Mysz jako model dziecięcej choroby płuc
Aby naśladować kluczowe cechy chILD, badacze użyli myszy całkowicie pozbawionych genu Sftpc. Zwierzęta te rodzą się z pozornie prawidłowymi płucami, ale w miarę starzenia rozwijają cechy przewlekłej choroby płuc: pogrubione przegrody między pęcherzykami, dodatkową tkankę bliznowatą bogatą w kolagen, przerost komórek typu II i gromadzenie się komórek układu odpornościowego. Szczegółowe pomiary wykazały, że ich architektura płuc stopniowo się pogarsza między 4 a 12 miesiącem życia, przypominając powolny postęp obserwowany u wielu pacjentów. Zespół zauważył również, że te myszy są wyjątkowo wrażliwe na stosowany w badaniach lek chemioterapeutyczny bleomycynę, która często służy w laboratoriach do wywoływania uszkodzeń płuc i zwłóknienia, co dodatkowo podkreśla podatność ich płuc pozbawionych surfaktantu.
Przygotowanie uszkodzonych płuc do przyjęcia nowych komórek
Skuteczne przeszczepienie nowych komórek do już zatłoczonego narządu nie jest trywialne. Autorzy sprawdzili, czy starannie dobrana, niska dawka bleomycyny może działać jako swego rodzaju „kondycjonowanie” — uszkadzając część wadliwych komórek gospodarza i tworząc miejsce dla przybyszów bez niszczenia płuca. U myszy pozbawionych Sftpc nawet niewielkie ilości bleomycyny pogłębiły bliznowacenie i obniżyły poziomy kilku kluczowych markerów komórek typu II, potwierdzając uraz. Jednak przy najniższej dawce uszkodzenia były ograniczone, a własna odpowiedź naprawcza płuca pozostała aktywna. Ta równowaga sugerowała okno, w którym komórki przeszczepione miały największe szanse na przyjęcie się, przeżycie i udział w gojeniu.
Zdrowe komórki surfaktantowe zasiedlają i przystępują do pracy
Zespół następnie wyizolował zdrowe komórki typu II od normalnych myszy i wprowadził milion tych komórek bezpośrednio do dróg oddechowych myszy pozbawionych Sftpc dziesięć dni po podaniu niskiej dawki bleomycyny. Przy użyciu kombinacji barwień białkowych i testów genetycznych wykazali, że komórki dawcy skutecznie się ukorzeniły, szczególnie u młodszych osobników. Przeszczepione komórki produkowały dojrzałe białko surfaktantu C — całkowicie nieobecne u gospodarza — co wskazywało, że nie były tylko obecne, lecz funkcjonalnie aktywne. Nowe komórki utrzymywały się co najmniej przez dwa miesiące. Co ważne, myszy, które otrzymały przeszczep komórek, miały mniej uszkodzeń płuc i mniej poważnie zniszczonych obszarów w porównaniu z myszami otrzymującymi jedynie bleomycynę, co sugeruje, że nawet częściowa wymiana chorych komórek może złagodzić postępujące uszkodzenia.
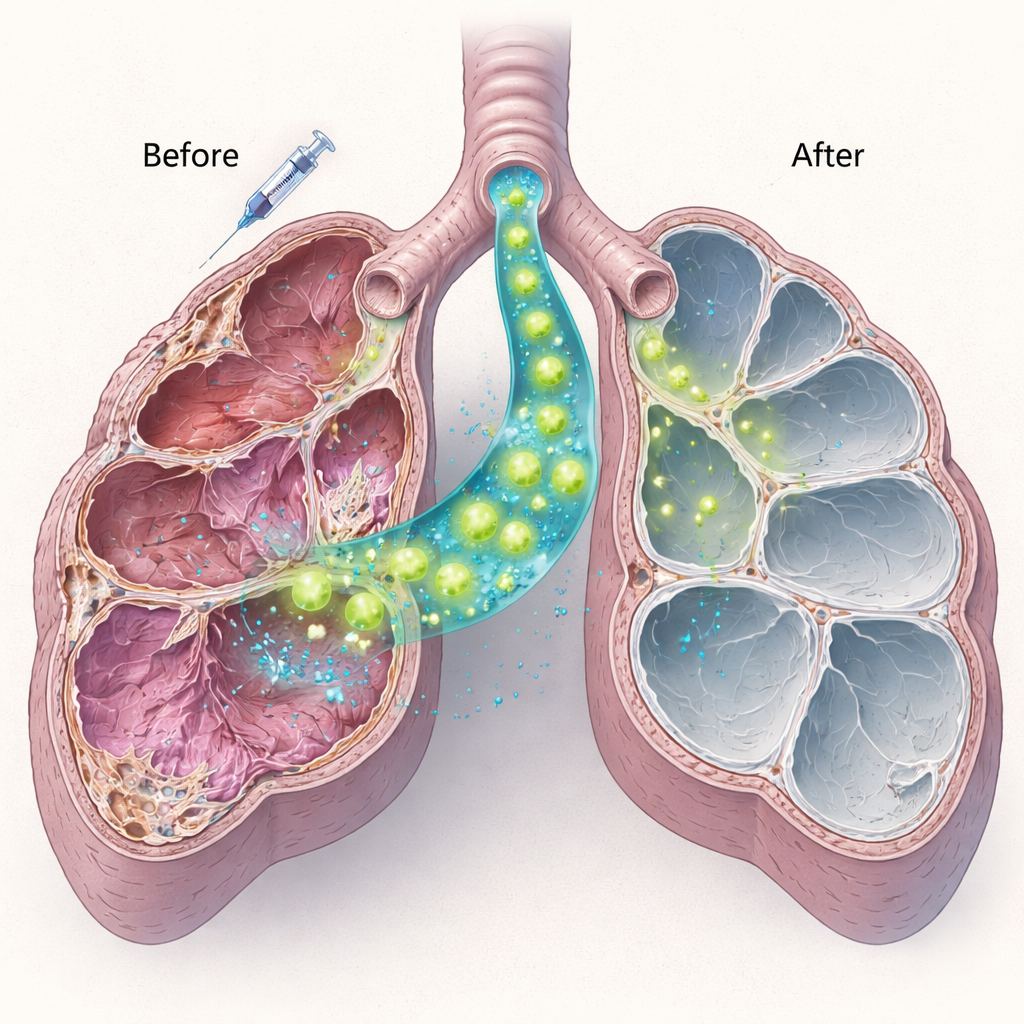
Od dowodu koncepcji do przyszłych terapii
Dla osób nietechnicznych kluczowy przekaz jest taki, że to badanie pokazuje realistyczną drogę do naprawy, a nie zastąpienia, płuc w niektórych genetycznych chorobach dziecięcych. Demonstrując, że umiarkowana liczba zdrowych komórek wytwarzających surfaktant może zadomowić się w przewlekle chorym płucu, wytwarzać brakujące białko i łagodzić uraz, praca ta stanowi fundament dla przyszłych terapii opartych na komórkach poprawionych genetycznie lub pochodzących z komórek macierzystych. Wciąż pozostaje wiele przeszkód, w tym znalezienie bezpieczniejszych sposobów przygotowania ludzkich płuc do takiego leczenia i zapewnienie długotrwałych korzyści. Mimo to badanie to przesuwa dyskusję z zarządzania objawami w stronę potencjalnego odbudowywania własnego mechanizmu płuc dla zdrowego oddychania.
Cytowanie: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Słowa kluczowe: dziecięca śródmiąższowa choroba płuc, białko surfaktantu C, pęcherzykowe komórki typu II, terapia komórkowa, zwłóknienie płuc