Clear Sky Science · pl
Aktywacja szlaku Hedgehog w keratocytach prowadzi do usztywnienia zrębu i zaburza regenerację rogówki
Dlaczego przezroczyste okno oka może zmętnieć
Rogówka jest przednim oknem oka, a jej przezroczystość jest niezbędna dla ostrego widzenia. Tymczasem oparzenia, urazy i niektóre choroby mogą sprawić, że ta przejrzysta tkanka staje się zmętniała i zbliznowaciała, co czasem prowadzi do ślepoty. Badanie stawia proste, lecz ważne pytanie: dlaczego niektóre rogówki goją się czysto, podczas gdy inne pozostają trwale uszkodzone? Autorzy skupiają się na ukrytej rozmowie między komórkami podporowymi wewnątrz rogówki a komórkami powierzchniowymi, które odtwarzają gładką, przezroczystą powłokę po urazie.
Ukryte komórki podporowe pod powierzchnią
Większą część rogówki stanowi twarda, przezroczysta warstwa pośrednia zwana zrębem. Jest wypełniona uporządkowanymi włóknami kolagenu i rozmieszczonymi komórkami zwanymi keratocytami. W zdrowych oczach dorosłych keratocyty są spokojne, lecz aktywne: utrzymują rusztowanie z kolagenu i wydzielają czynniki wzrostu odżywiające nabłonek powierzchniowy, który jest stale odnawiany przez komórki macierzyste na obrzeżu rogówki. Badacze pokazują, że u młodych myszy szlak molekularny zwany Hedgehog jest aktywny w tych keratocytach, a następnie wycisza się w miarę dojrzewania oka. Gdy genetycznie zablokowali sygnalizację Hedgehog w dojrzałych keratocytach, rogówki wyglądały normalnie, co sugeruje, że stan spoczynkowy — a nie ciągła aktywność — jest naturalnym stanem tego szlaku w zdrowej, przejrzystej rogówce.
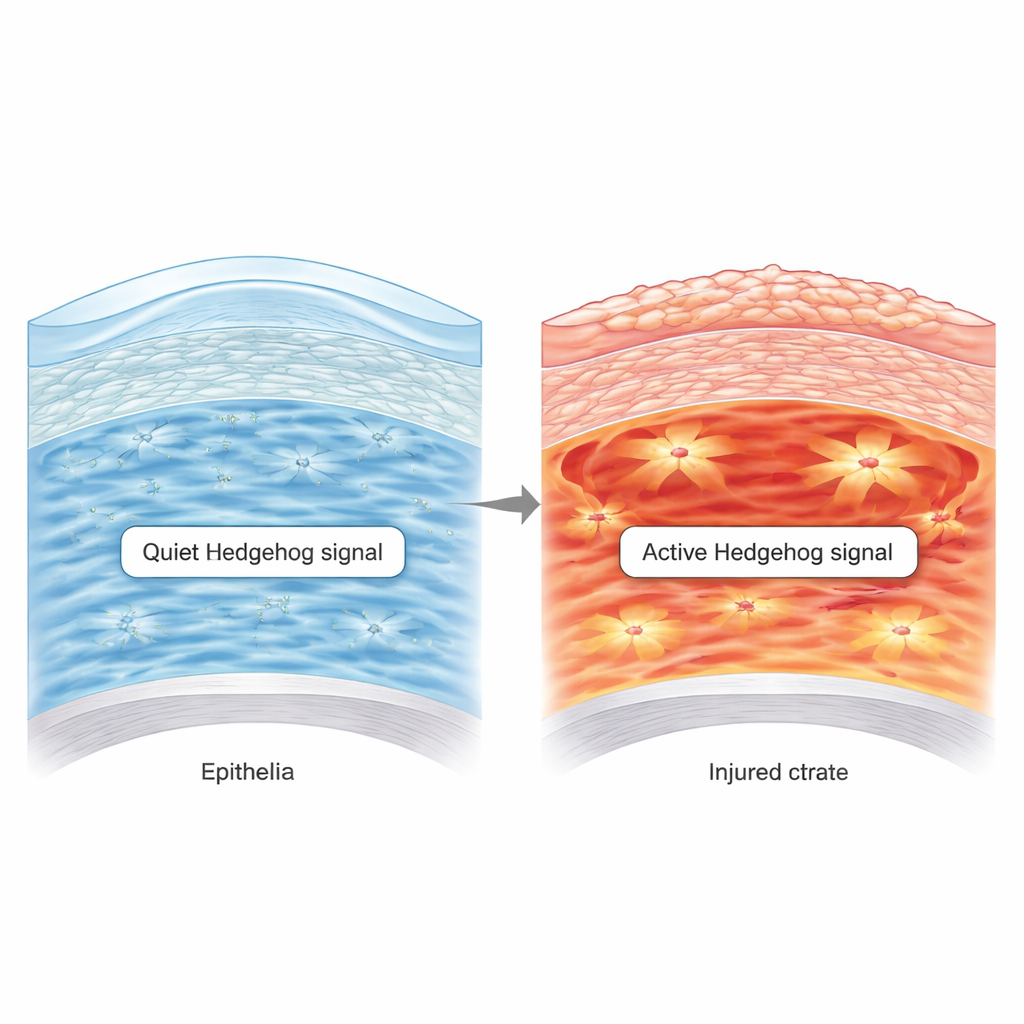
Gdy oparzenia chemiczne budzą uśpiony szlak
Płytkie zadrapania rogówki zwykle goją się w ciągu dnia lub dwóch: komórki macierzyste dzielą się, nowe komórki nabłonka wślizgują się, a zrąb pozostaje w dużej mierze niezakłócony. Oparzenia chemiczne są znacznie bardziej destrukcyjne. W modelu myszy z oparzeniem alkalicznym zespół zaobserwował długotrwałe defekty — cienkie, źle ułożone komórki powierzchniowe nad zdezorganizowanym zrębem. Stwierdzili, że sygnalizacja Hedgehog była silnie reaktywowana w keratocytach po uszkodzeniu chemicznym, ale nie po prostym zarysowaniu. Ten wzrost aktywności wiązał się z cząsteczkami zapalnymi, szczególnie cytokiną TNF‑α, którą autorzy wykazali jako zdolną bezpośrednio włączyć program Hedgehog w hodowanych keratocytach. Wyniki sugerują, że silne zapalenie po oparzeniu popycha zwykle spokojne komórki zrębu w szkodliwy, nadaktywny stan.
Z pomocników konserwujących do sztywnych budowniczych blizn
Aby zrozumieć, co się dzieje, gdy Hedgehog pozostaje włączony, naukowcy zaprojektowali myszy, u których keratocyty mają przewlekle aktywną sygnalizację Hedgehog. Nawet bez urazu te rogówki stopniowo rozwijały cieńszy, sztywniejszy zrąb. Profilowanie genów izolowanych keratocytów ujawniło, że zmieniają identyfikację: klasyczne markery keratocytów spadały, podczas gdy geny typowe dla fibroblastów i komórek podobnych do mezenchymalnych macierzystych wzrastały. Równocześnie spadła produkcja kluczowych składników macierzy zewnątrzkomórkowej — takich jak kolagen i białko strukturalne zwane keratokanem. Pod mikroskopem włókna kolagenowe zbliżyły się do siebie, a testy mechaniczne wykazały, że tkanka zrębu stała się ponad dwukrotnie sztywniejsza niż normalnie. Zmiany te przemieniły wspierające rusztowanie w sztywną konstrukcję, co jest cechą charakterystyczną tkanki bliznowatej.
Jak twarde podłoże hamuje gojenie powierzchni
Zaskakujący zwrot akcji pochodził z powierzchni rogówki. U myszy z przewlekle aktywnym Hedgehog w keratocytach nabłonek początkowo zamykał rany zgodnie z harmonogramem, lecz potem nie dojrzewał prawidłowo. Warstwa powierzchniowa pozostała cienka, z wieloma niedojrzałymi komórkami i niewielką liczbą w pełni zróżnicowanych, specyficznych dla rogówki komórek. Zespół powiązał ten defekt z mechanicznym systemem sygnalizacyjnym w komórkach nabłonka znanym jako szlak Hippo–YAP, który wyczuwa sztywność leżącej poniżej tkanki. W usztywnionym zrębie sygnalizacja Hippo została włączona, co z kolei wyłączyło YAP — białko, które normalnie sprzyja zdrowemu różnicowaniu. Gdy badacze zastosowali małą cząsteczkę hamującą sygnalizację Hippo, aktywność YAP powróciła, a nabłonek odzyskał niemal normalną grubość i strukturę — choć sam zrąb pozostał cienki. Wskazuje to, że sztywność stromalnego „łóżka” może bezpośrednio decydować o tym, czy powierzchnia potrafi się prawidłowo odbudować.
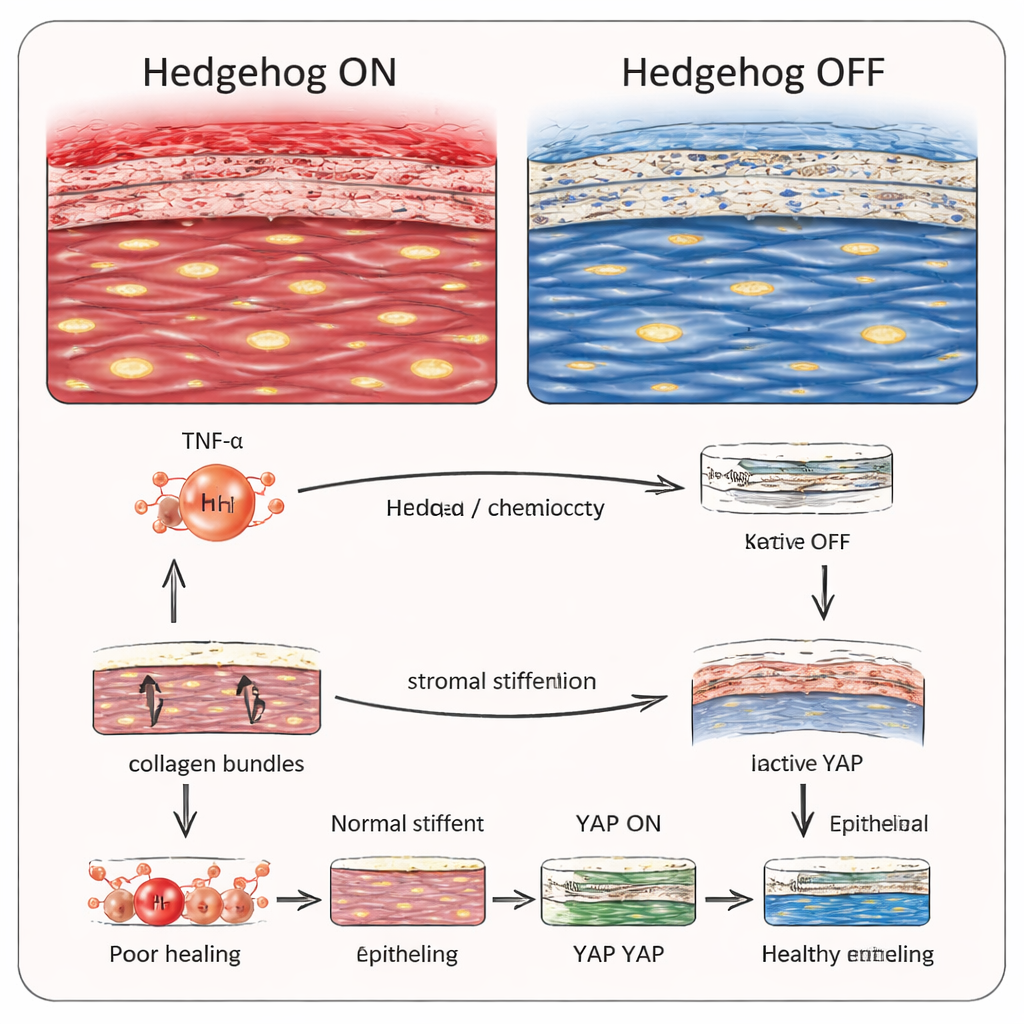
Wyłączanie Hedgehog by uratować wzrok
Najbardziej obiecująca część pracy pochodzi z eksperymentów, które przyciszały sygnalizację Hedgehog. U myszy z genetycznie aktywowanym Hedgehog leczenie lekiem blokującym kluczowe czynniki transkrypcyjne tego szlaku przywróciło organizację zrębu i uratowało różnicowanie komórek powierzchniowych. W oddzielnych eksperymentach myszy pozbawione podstawowego składnika szlaku Hedgehog w keratocytach były chronione przed typowym bliznowaceniem i defektami nabłonka po oparzeniach chemicznych. Wreszcie zastosowanie leku blokującego Hedgehog do oczu normalnych myszy po urazie alkalicznym znacząco poprawiło strukturę rogówki bez widocznych skutków ubocznych. Dla czytelnika nieprofesjonalnego przekaz jest taki: nadmiernie pobudzony „naprawczy” szlak w komórkach podporowych rogówki może faktycznie sabotować gojenie, usztywniając tkankę i dezorientując komórki powierzchniowe. Poprzez ostrożne przyciszenie tego szlaku może być możliwe skierowanie rogówki do gojenia się w sposób przejrzysty zamiast zmętniałego, co otwiera nową drogę leczenia oparzeń chemicznych i być może innych schorzeń, takich jak choroby oczu związane z cukrzycą, gdzie gojenie ran jest przewlekle zaburzone.
Cytowanie: Yu, Q., Li, P., Du, Z. et al. Activated Hedgehog signaling in keratocytes leads to stromal stiffness and impairs corneal regeneration. npj Regen Med 11, 9 (2026). https://doi.org/10.1038/s41536-026-00453-2
Słowa kluczowe: gojenie ran rogówki, szlak Hedgehog, usztywnienie zrębu, keratocyty, chemiczne uszkodzenie oka