Clear Sky Science · pl
Przedstawiamy PIGMO, nowy PIGmentowany model myszy choroby Parkinsona
Dlaczego zabarwienie komórek mózgu może mieć dla ciebie znaczenie
Choroba Parkinsona jest najbardziej znana z drżeń i sztywności, ale głęboko w mózgu wiąże się z ciemnym pigmentem, który stopniowo gromadzi się w określonych komórkach nerwowych. Nowe badanie wprowadza model myszy nazwany PIGMO, który celowo barwi te kluczowe komórki na brązowo‑czarno, podobnie jak w mózgu człowieka. Robiąc to w kontrolowany i stopniowy sposób, badacze mogą obserwować rozwój uszkodzeń przypominających Parkinsona krok po kroku i testować terapie ukierunkowane nie tylko na łagodzenie objawów, lecz także na spowolnienie lub zatrzymanie samej choroby. 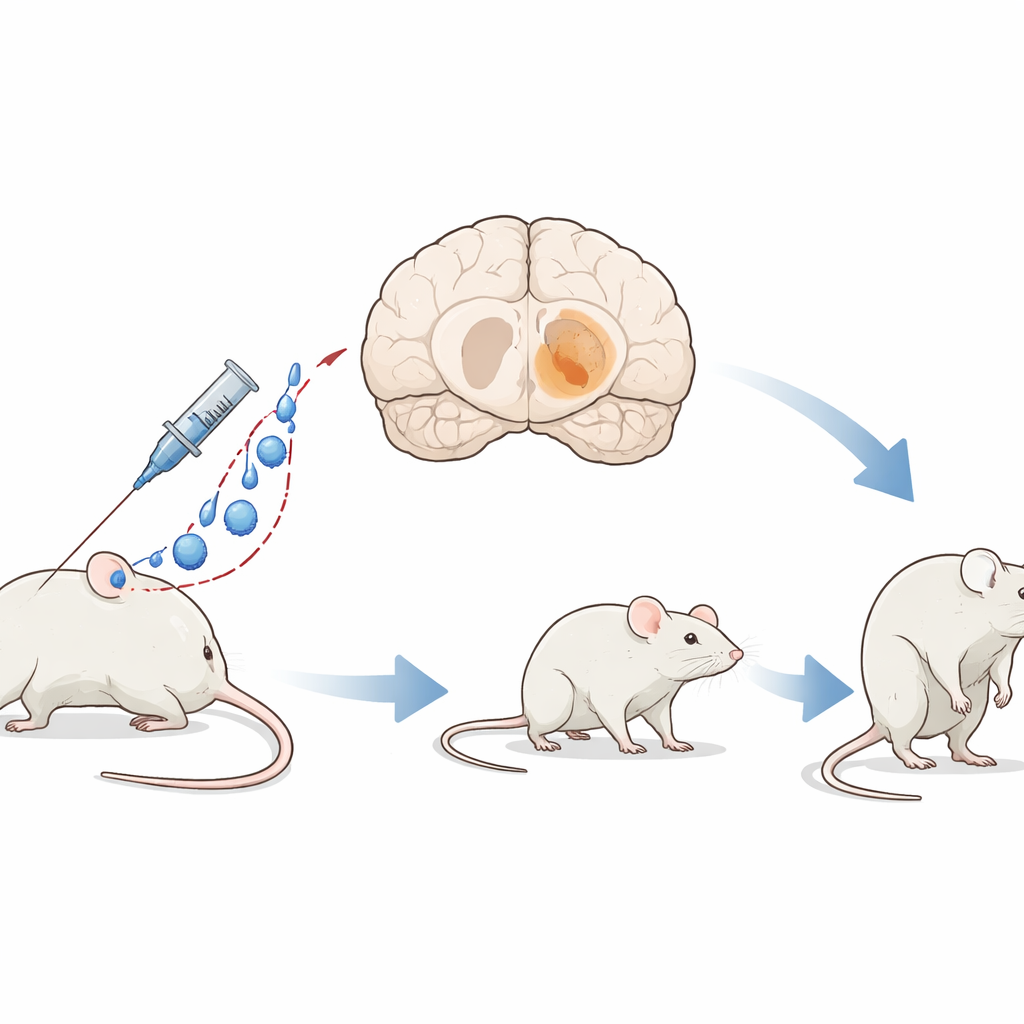
Tworzenie ciemniejszego mózgu bez operacji
Aby stworzyć PIGMO, zespół użył zmodyfikowanego wirusa do dostarczania genów, który potrafi krążyć we krwi, przekraczać barierę krew‑mózg i wnikać do komórek mózgu. Wirus ten przenosi przepis na ludzką tyrozynazę, enzym produkujący neuromelaninę — ciemny pigment występujący w komórkach nerwowych najbardziej dotkniętych chorobą Parkinsona. Zamiast nawiercać czaszkę, badacze wstrzyknięli wirusa do żyły za okiem, pozwalając mu rozprzestrzenić się szeroko i obustronnie w mózgu. To proste, wolne od zabiegu chirurgicznego podejście dało mysz, której głębokie ośrodki ruchu stopniowo ciemnieją i starzeją się w sposób bardzo zbliżony do stanu ludzkiego.
Stopniowe ściemnianie kluczowych ośrodków ruchu
Po dostarczeniu wirusa pigment zaczął pojawiać się w trzech ośrodkach mózgowych kontrolujących ruch i czujność: substancji czarnej (substantia nigra), brzusznej części nakrywki (ventral tegmental area) oraz jądrze sinawym (locus coeruleus). Po miesiącu tylko kilka komórek wykazywało słabe zabarwienie, ale po czterech miesiącach te obszary były widocznie ciemniejsze gołym okiem. Pigment nadal narastał po ośmiu i dwunastu miesiącach, chociaż całkowita liczba pofarbowanych komórek w niektórych rejonach zaczęła spadać, co sugeruje, że najbardziej obciążone komórki zaczynały obumierać. Nie wszystkie neurony były jednakowo dotknięte: konkretne podtypy w substancji czarnej przyjmowały znacznie więcej pigmentu niż inne, co odzwierciedla selektywną podatność obserwowaną u osób z chorobą Parkinsona.
Od pigmentu do grudek i ginących połączeń
Gdy poziom pigmentu przekroczył pewien próg, dotknięte komórki zaczęły tworzyć gęste skupiska białka alfa‑synukleiny — struktury bardzo przypominające ciała Lewy’ego znalezione u pacjentów. Te inkluzje pojawiły się najpierw w substancji czarnej po około czterech miesiącach, a później w pozostałych pofarbowanych regionach, stając się coraz częstsze w czasie. Równocześnie długie wypustki tych komórek do prążkowia, kluczowego przekaźnika dla poleceń ruchowych, stopniowo się przerzedzały. Pomiary wykazały znaczny ubytek włókien bogatych w dopaminę oraz kurczenie się populacji zdrowych komórek dopaminergicznych, szczególnie w substancji czarnej, przy czym „duchy” komórek — pofarbowane, ale funkcjonalnie upośledzone — były szczególnie skłonne do znikania. 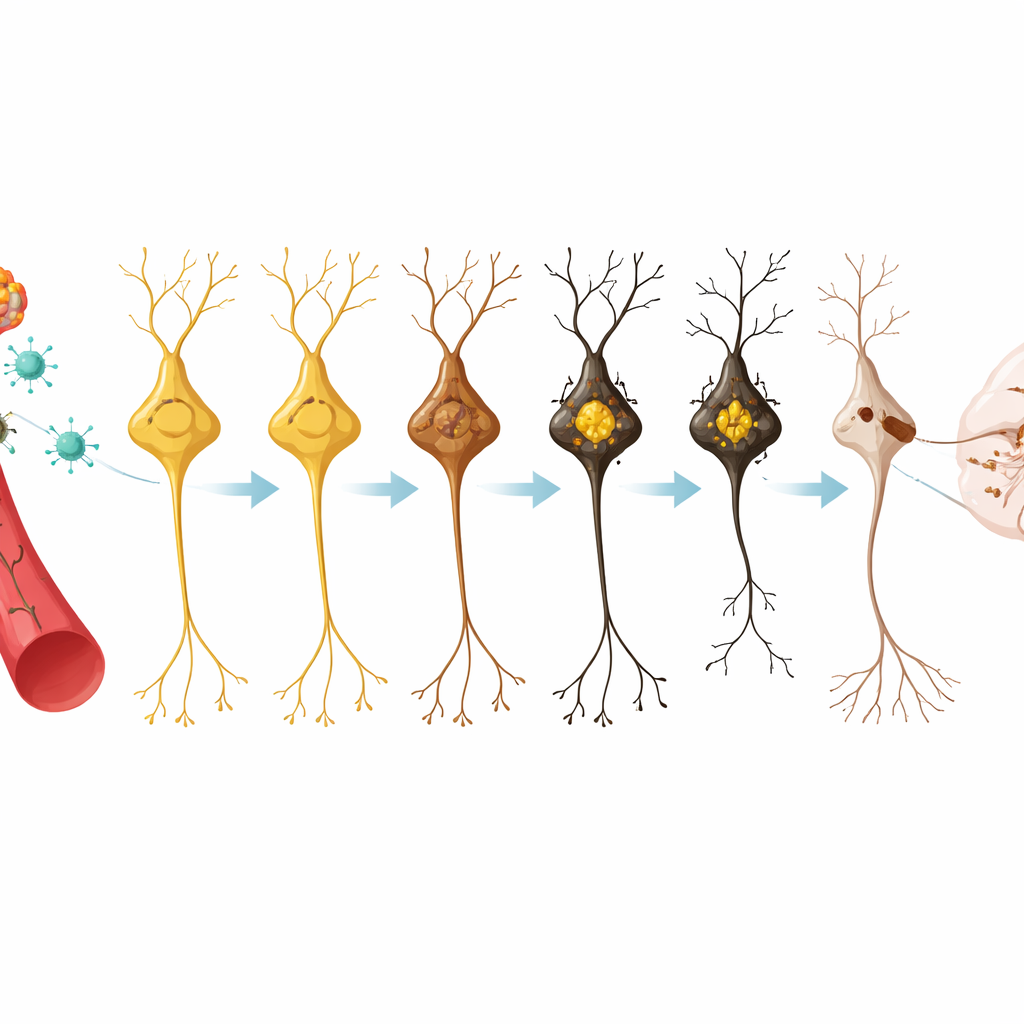
Obserwowanie stopniowego pogorszenia ruchu
Zachowanie na zewnątrz myszy PIGMO odzwierciedlało te wewnętrzne uszkodzenia. Zwierzęta testowano na obracającym się walcu oraz w prostym teście postawy mierzącym sztywność. Na początku ich wyniki były podobne do myszy kontrolnych, ale wraz z upływem miesięcy oraz narastaniem pigmentu, grudek i utraty komórek, myszy PIGMO zaczęły wykazywać wyraźne problemy motoryczne. Po dwunastu miesiącach utrzymywały się na obracającym walcu znacznie krócej i były wyraźnie sztywniejsze, odzwierciedlając stopniowy początek i postęp zaburzeń ruchowych w ludzkiej chorobie Parkinsona.
Nowe pole do testowania spowalniania choroby Parkinsona
Dla osób spoza specjalizacji kluczowy przekaz jest taki: mysz PIGMO przybliża badaczy do realistycznej, progresywnej wersji choroby Parkinsona w laboratorium. Włączając produkcję pigmentu w tych samych komórkach, które zawodzą u pacjentów — i robiąc to w całym mózgu bez operacji — model ten odtwarza narastanie pigmentu, gromadzenie się białka, utratę włókien nerwowych i objawy ruchowe w przewidywalnym czasie. Ten długi okres, od pierwszych drobnych plamek pigmentu do wyraźnej niepełnosprawności, daje istotną szansę na przetestowanie nowych leków lub terapii genowych po cichym rozpoczęciu choroby, lecz zanim szkody staną się nieodwracalne, co może przyspieszyć poszukiwanie terapii naprawdę spowalniających lub zapobiegających postępowi Parkinsona.
Cytowanie: Chocarro, J., Marana, S., Espelosin, M. et al. Introducing PIGMO, a novel PIGmented MOuse model of Parkinson’s disease. npj Parkinsons Dis. 12, 72 (2026). https://doi.org/10.1038/s41531-026-01289-9
Słowa kluczowe: choroba Parkinsona, model zwierzęcy, neuromelanina, terapia genowa, neurony dopaminergiczne