Clear Sky Science · pl
Mapa sensoryczna węchu jest zaburzona w transgenicznym modelu myszy nadekspresującej dzikiego typu ludzki α-synuklein choroby Parkinsona
Dlaczego utrata węchu ma znaczenie w chorobie Parkinsona
Wielu ludzi postrzega chorobę Parkinsona przede wszystkim jako zaburzenie ruchowe, tymczasem u większości pacjentów pierwszym objawem jest utrata węchu. Ten deficyt może pojawić się dziesięciolecia przed drżeniem czy sztywnością, co czyni go silnym wczesnym sygnałem ostrzegawczym. Opisane tutaj badanie stawia podstawowe, wciąż nie do końca rozstrzygnięte pytanie: co dokładnie ulega zmianie w neuronalnych obwodach węchowych, gdy zaczynają się zmiany związane z Parkinsonem? Badając to w starannie zaprojektowanym modelu myszy, autorzy ujawniają, jak kluczowe białko związane z Parkinsonem zaburza wewnętrzną „mapę węchu” mózgu i wskazują na nową, łatwo dostępną źródło wczesnych wskazówek o chorobie.
Mózgowa mapa węchu
W naszym nosie znajdują się miliony wyspecjalizowanych komórek węchowych, z których każda reaguje na określone cząsteczki zapachowe. Komórki te wysyłają długie, cienkie włókna do przedniej części mózgu, gdzie zbiegają się w drobne węzły zwane kłębuszkami w opuszce węchowej. Każdy rodzaj zapachu aktywuje specyficzny wzór kłębuszków, tworząc precyzyjną mapę sensoryczną, która pozwala mózgowi rozróżnić np. kawę od cynamonu czy dym od perfum. U zdrowych myszy komórki niosące receptory jednego typu (oznaczone M72) i drugiego (oznaczone P2) niezawodnie projekcjonują do zaledwie dwóch dobrze zdefiniowanych kłębuszków na każdą opuszke, tworząc wysoce zorganizowaną i powtarzalną mapę.
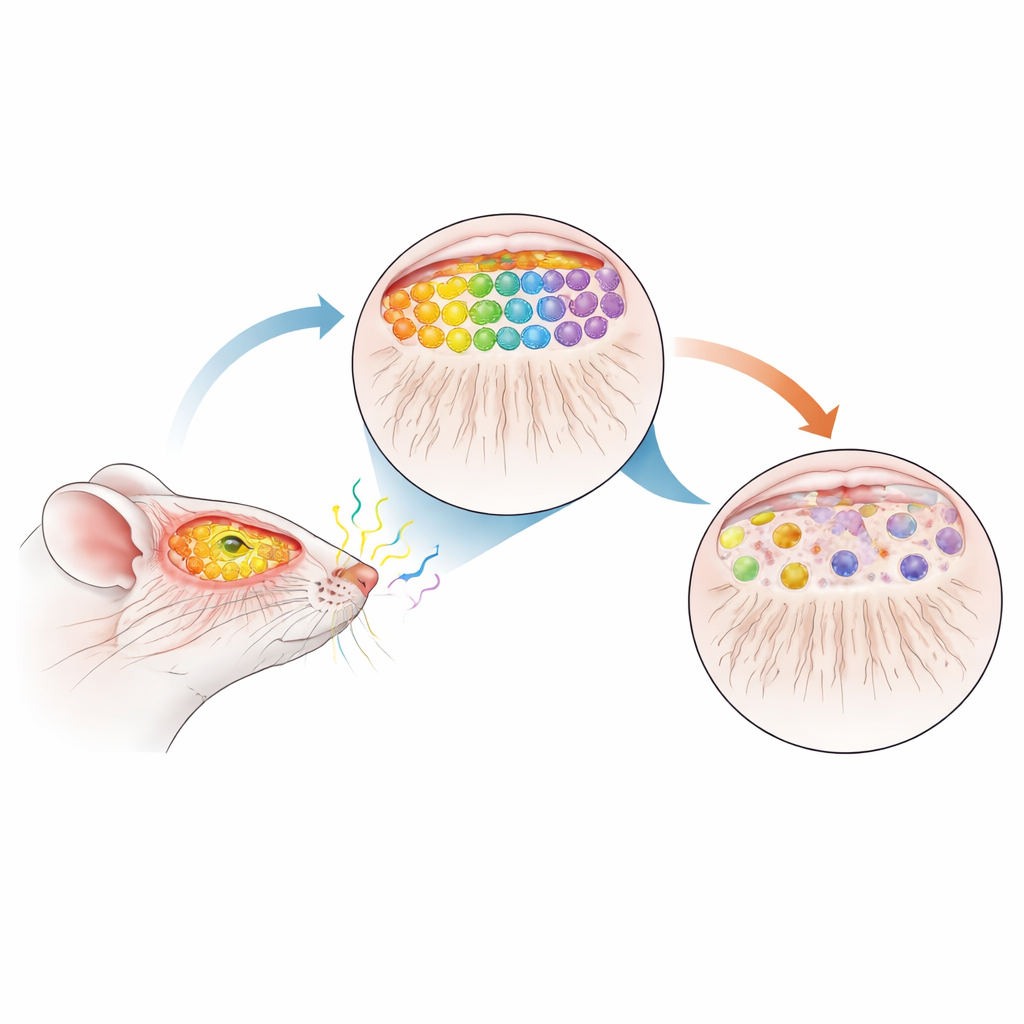
Myszy jako model wczesnego Parkinsona
Aby sprawdzić, jak choroba Parkinsona może zaburzyć tę mapę, zespół użył myszy nadprodukujących ludzkie α-synuklein w postaci dzikiego typu — to samo białko, które tworzy skupiska w mózgach chorych na Parkinsona. Następnie skrzyżowali te zwierzęta z liniami z wyznakowanymi receptorami M72 i P2, by wizualnie śledzić wybrane komórki węchowe i ich połączenia. Istotne jest to, że dodatkowa α-synuklein włącza się dopiero po urodzeniu i stopniowo gromadzi z wiekiem, naśladując powolny, progresywny przebieg choroby u ludzi. W wieku 12 miesięcy — mniej więcej połowa życia myszy i porównywalna do stadium prodromalnego u ludzi — badacze szczegółowo zbadali układ węchowy tych zwierząt.
Gdy mapa węchu się rozpada
Barwiąc wyznakowane neurony i śledząc ich przebieg, naukowcy odkryli uderzające rozbicie mapy węchu u myszy nadekspresujących α-synuklein. Liczba neuronów M72 i P2 w nosie spadła gwałtownie — około trzy czwarte mniej dla M72 i niemal połowa dla P2 — a ich włókna do opuszki były znacznie zredukowane. Zamiast zbiegać się schludnie do dwóch mocnych kłębuszków, pozostałe włókna często tworzyły wiele mniejszych kłębuszków o zróżnicowanym rozmiarze i położeniu. Te „dodatkowe” węzły nie pojawiały się w spójnych lokalizacjach u kolejnych myszy, co wskazuje na utratę normalnej precyzji topograficznej. Szeroki marker zakończeń komórek węchowych, VGLUT2, był również zmniejszony o około 44% w opuszce, co sugeruje, że degeneracja sięgała znacznie dalej niż do dwóch wyznakowanych typów receptorów.
Łączenie uszkodzonych obwodów z utratą węchu
Uszkodzenia strukturalne przekładały się na mierzalne problemy węchowe. Starsze myszy z nadekspresją α-synukleiny potrzebowały więcej czasu, by znaleźć ukryte jedzenie, miały gorszą zdolność rozróżniania zapachów i nie wykazywały preferencji dla terenów oznaczonych własnym zapachem — testy behawioralne, które łącznie ujawniają hiposmię i upośledzoną dyskryminację zapachową. Potrzebowały też dużo silniejszych stężeń odorantów, aby zareagować, co wskazuje na obniżoną czułość. Deficyty te nie występowały u młodszych myszy, u których wyznakowane neurony i ich mapy nadal wyglądały w dużej mierze normalnie, co wiąże czas wystąpienia utraty funkcji z późniejszym rozpadem mapy sensorycznej, a nie z jej wczesnym rozwojem. Co istotne, choć problematyczne białko było obfite w opuszce węchowej, nie wykryto go w nabłonku węchowym nosa, co wskazuje, że to zmiany wewnątrz obwodów opuszki — szczególnie w komórkach mitralnych przekazujących informacje węchowe dalej — prawdopodobnie napędzają zaburzenie mapy.
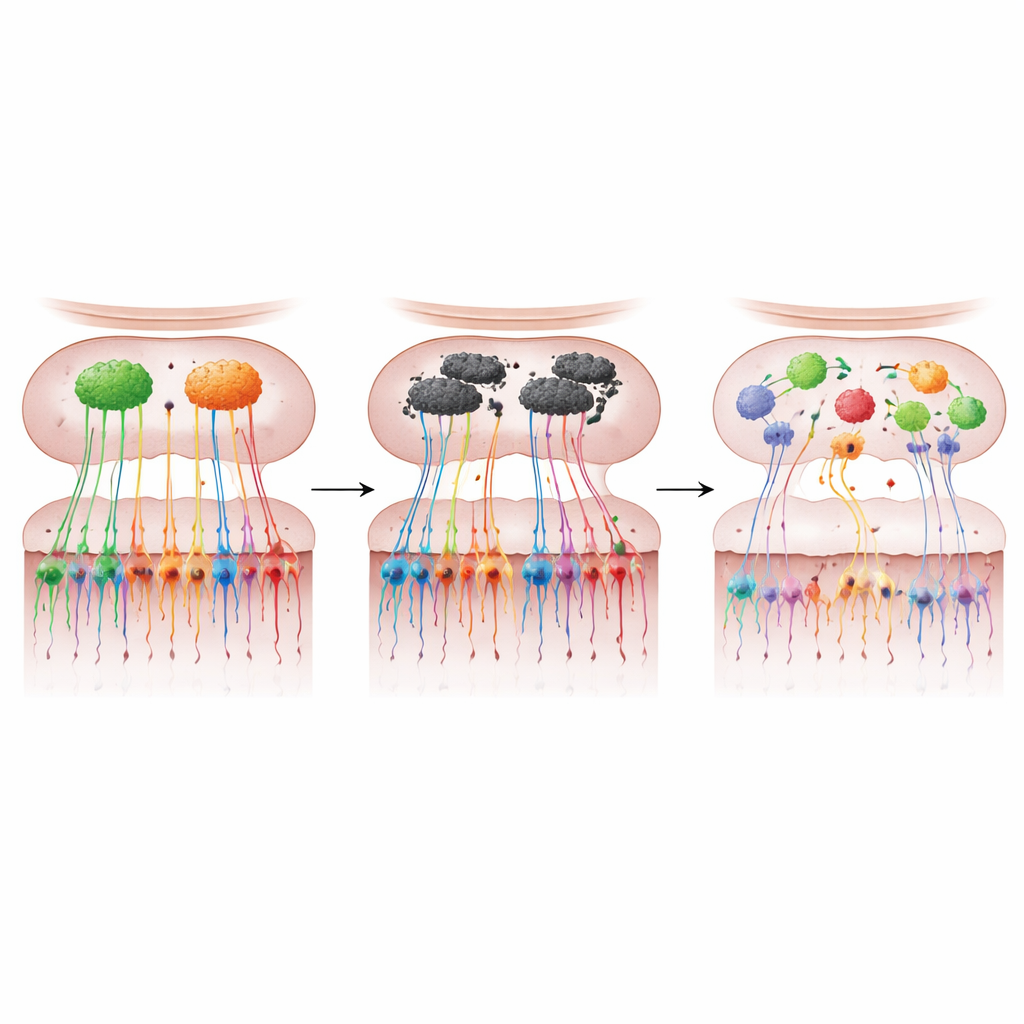
Komórki węchowe jako okno na wczesną chorobę
Podsumowując, praca przedstawia jasny przekaz dla czytelników niezaznajomionych z tematem: w tym mysim modelu przypominającym Parkinsona nadprodukcja α-synukleiny w opuszce węchowej prowadzi zarówno do utraty, jak i niewłaściwego okablowania komórek węchowych, wypaczając mózgową mapę zapachów i wywołując wczesne problemy z węchem. Ponieważ komórki sensoryczne nosa są rozwinięciowo powiązane z mózgiem, a jednocześnie można je pobrać za pomocą minimalnie inwazyjnych wymazów lub biopsji, autorzy sugerują, że podobne zmiany u ludzi mogłyby stać się silnym wczesnym biomarkerem choroby Parkinsona. Mapowanie molekularnych odcisków tych komórek, sugerują, może nie tylko pomóc wykryć osoby zagrożone na wiele lat przed pojawieniem się objawów ruchowych, lecz także dostarczyć nowych informacji o tym, jak choroba się zaczyna, rozprzestrzenia i jak można ją spowolnić lub zapobiec jej rozwojowi.
Cytowanie: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Słowa kluczowe: choroba Parkinsona, zaburzenia węchu, alpha-synuklein, mapa sensoryczna, biomarkery