Clear Sky Science · pl
Mutacja LRRK2R1627P wzmacnia przewlekłe zapalenie i agregację α-synukleiny w jelicie szczurów wywołane czynnikami środowiskowymi
Dlaczego jelito ma znaczenie w chorobie mózgu
Choroba Parkinsona jest najbardziej znana z drżeń i zaburzeń ruchowych, ale coraz więcej dowodów sugeruje, że jej źródła mogą zaczynać się daleko od mózgu, głęboko w jelicie. W tym badaniu analizowano, jak konkretna zmiana genetyczna powiązana z Parkinsonem w populacjach azjatyckich może, w połączeniu ze starzeniem się i narażeniem na toksyny, stopniowo uszkadzać jelito u szczurów. Obserwując, co dzieje się w przewodzie pokarmowym w ciągu życia zwierząt, autorzy śledzą, jak codzienne mechanizmy odpornościowe mogą przejść w przewlekłe zapalenie, tworząc warunki sprzyjające gromadzeniu się białek związanych z chorobą, co ostatecznie może zagrozić mózgowi.
Ryzykowny gen w przewodzie pokarmowym
Naukowcy skupili się na wariancie genu o nazwie LRRK2, od dawna powiązanym z chorobą Parkinsona i niektórymi zapalnymi chorobami jelit. Stworzyli szczury noszące odpowiadającą mutację, nazwaną LRRK2R1627P, i porównywali je ze szczurami normalnymi przez całe życie. Chociaż poziom transkryptu genu LRRK2 w jelicie nie uległ zmianie, całkowita ilość białka LRRK2 i jeden z jego kluczowych markerów aktywności były zmniejszone, co wskazuje, że mutacja osłabia normalną funkcję tego białka w jelicie. Ta subtelna zmiana molekularna nie powodowała dramatycznych wczesnych uszkodzeń, ale cicho zmieniała sposób, w jaki komórki jelitowe odnawiają się i organizują wraz ze starzeniem się zwierząt.
Starzejące się jelito pod wolnym, przewlekłym obciążeniem
Z upływem miesięcy szczury z mutacją zaczęły wykazywać wyraźne oznaki zaburzonej struktury jelita. Ich jelito cienkie stało się krótsze, a drobne, palczaste kosmki i krypty odpowiedzialne za wchłanianie składników odżywczych uległy pomniejszeniu. Pewne wyspecjalizowane komórki wyściełające jelito, produkujące ochronną śluzówkę i substancje przeciwdrobnoustrojowe — komórki kubkowe i Panetha — zostały zredukowane, podczas gdy białka pomagające sąsiednim komórkom tworzyć zwarte, odporne na przeciekanie połączenia również się obniżyły. W mikroskopie połączenia te stały się krótsze lub szersze, co sugeruje osłabioną barierę. Co ważne, ogólna architektura nie rozpadła się; zamiast tego jelito wykazywało bardziej podstępny wzorzec zmniejszonego odnawiania i ochrony, co może uczynić je bardziej podatnym na podrażnienia i infekcje. 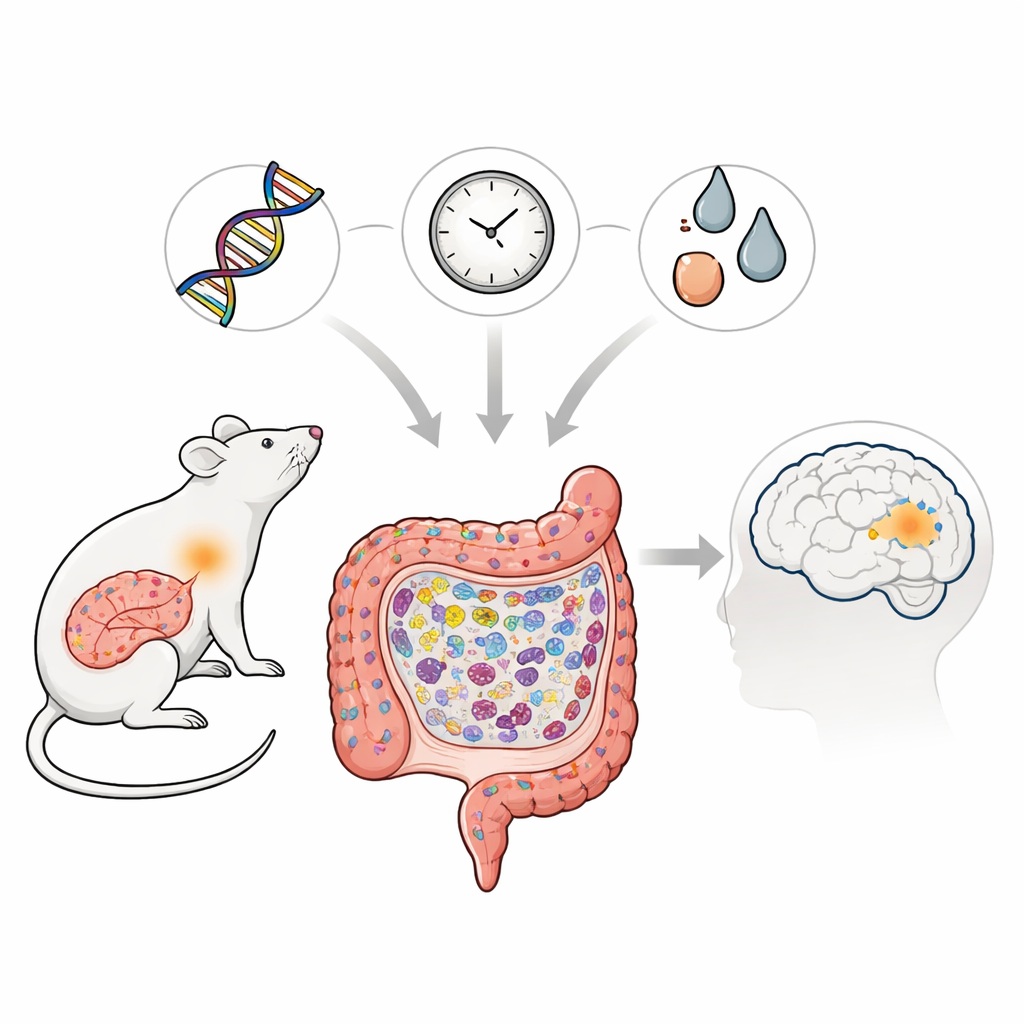
Układ odpornościowy na krawędzi wybuchu
Aby zrozumieć, dlaczego jelito traci równowagę, zespół przeanalizował aktywność genów i komórki odpornościowe w ścianie jelita. Stwierdzili, że szlaki powiązane z sensorem TLR4 i jego partnerem NF-κB były nadaktywne u starszych szczurów z mutacją. Te sensory normalnie pomagają wykrywać szkodliwe drobnoustroje, ale tutaj spowodowały nagromadzenie „walczących najpierw” komórek odpornościowych znanych jako makrofagi M1. Komórki te wydzielały molekuły zapalne, zmieniając jelito w przewlekle podrażnione środowisko. Co uderzające, białko związane z Parkinsonem, α-synukleina, w swojej chorobie związanej formie fosforylowanej, zaczęło gromadzić się nie w neuronach jelitowych, lecz wewnątrz tych aktywowanych makrofagów w jelicie cienkim, szczególnie u starszych zwierząt.
Zwiększona wrażliwość na uderzenia ze środowiska
Mutacja genetyczna sama w sobie nie wyjaśniała wszystkiego. Gdy młode szczury krótko eksponowano na bakteryjne toksyny (LPS), które stymulują TLR4, zwierzęta z mutacją LRRK2 rozwijały znacznie cięższe zapalenie jelit niż osobniki normalne. Ich nabłonek jelitowy złuszczał więcej komórek, białka bariery spadły jeszcze bardziej, a prozapalne makrofagi gwałtownie wzrosły, ponownie gromadząc nieprawidłową α-synukleinę. To sugeruje, że nosiciele podobnych mutacji mogą być szczególnie wrażliwi na czynniki środowiskowe zaburzające jelito, takie jak niektóre infekcje czy toksyny, co potęguje ich długoterminowe ryzyko.
Wyłączanie sygnału alarmowego
Ponieważ TLR4 znajdował się w centrum tej burzy zapalnej, zespół przetestował lek TAK-242, który specyficznie tłumi sygnalizację TLR4. Podawany przez kilka miesięcy szczurom w średnim wieku, inhibitor w dużej mierze przywrócił długość jelita cienkiego, rozmiar kosmków i krypt, liczbę komórek produkujących śluz oraz białka bariery. Zmniejszył nadaktywne makrofagi, obniżył poziomy molekuł zapalnych i zdecydowanie ograniczył gromadzenie się nieprawidłowej α-synukleiny w jelicie. Jednocześnie skorygował zaburzoną społeczność mikrobiologiczną: zwiększyła się różnorodność, ustąpił przerost Lactobacillus, odbudowało się kilka korzystnych grup bakterii, a przewidywane funkcje mikrobiomu przesunęły się z dala od wzorców powiązanych z chorobą. 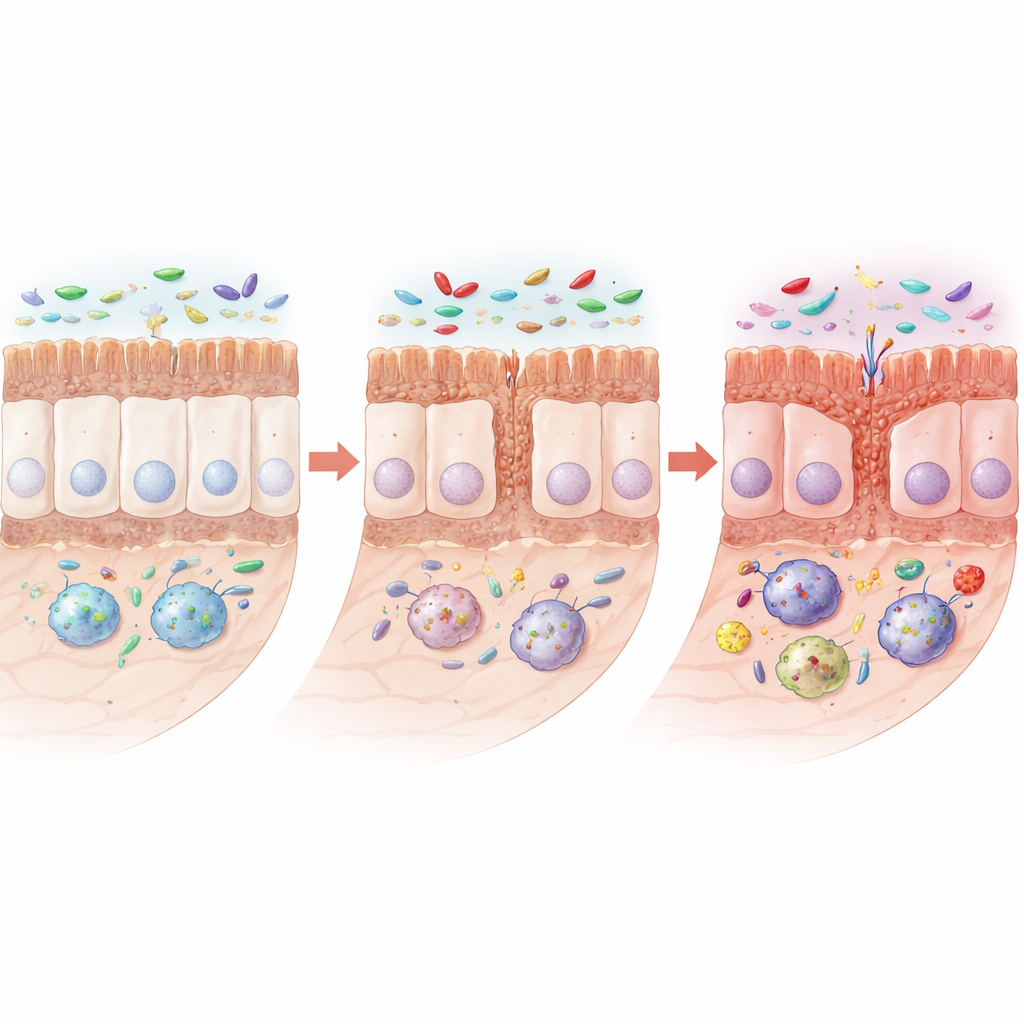
Co to oznacza dla ryzyka Parkinsona
Dla osoby niebędącej specjalistą przesłanie jest takie, że „gen Parkinsona” może po cichu przekształcać obronę immunologiczną jelita w czasie, szczególnie w obecności starzenia się i stresu środowiskowego. U tych szczurów skutkiem jest przewlekłe, niskiego stopnia zapalenie, które osłabia barierę jelitową, zaburza rezydujące mikroby i powoduje akumulację białka powiązanego z Parkinsonem w komórkach odpornościowych — jeszcze nie pełnoobjawowy Parkinson, ale biologiczne środowisko, które może sprzyjać późniejszej chorobie mózgu. Pokazując, że zablokowanie pojedynczej ścieżki odpornościowej w jelicie może odwrócić wiele z tych zmian, badanie wskazuje jelito jako praktyczny wczesny cel: ochrona zdrowia jelit i uspokojenie zapalenia jelitowego mogą pomóc opóźnić lub zapobiec Parkinsonowi u osób obarczonych ryzykiem genetycznym.
Cytowanie: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Słowa kluczowe: Choroba Parkinsona, zapalenie jelit, mutacja LRRK2, mikrobiom, odporność wrodzona