Clear Sky Science · pl
Głębokie neurobehawioralne fenotypowanie ujawnia neuronalne odciski palców deficytów lokomocyjnych w chorobie Parkinsona
Dlaczego problemy z chodzeniem w chorobie Parkinsona mają znaczenie
Dla wielu osób z chorobą Parkinsona jednym z najbardziej przerażających objawów jest uczucie, że stopy nagle przyklejają się do podłogi, albo że chodzenie zwalnia niemal do zatrzymania. Te załamania ruchu, od subtelnego spowolnienia po pełne „zamarzanie” chodu, znacznie zwiększają ryzyko upadków i utraty samodzielności, a jednocześnie obecne leki i stymulacja mózgu często nie zapobiegają im. Badanie miało na celu odkrycie ukrytych wzorców aktywności mózgowej towarzyszących takim problemom z chodzeniem, z długoterminowym celem zaprojektowania bardziej inteligentnych terapii działających doraźnie.
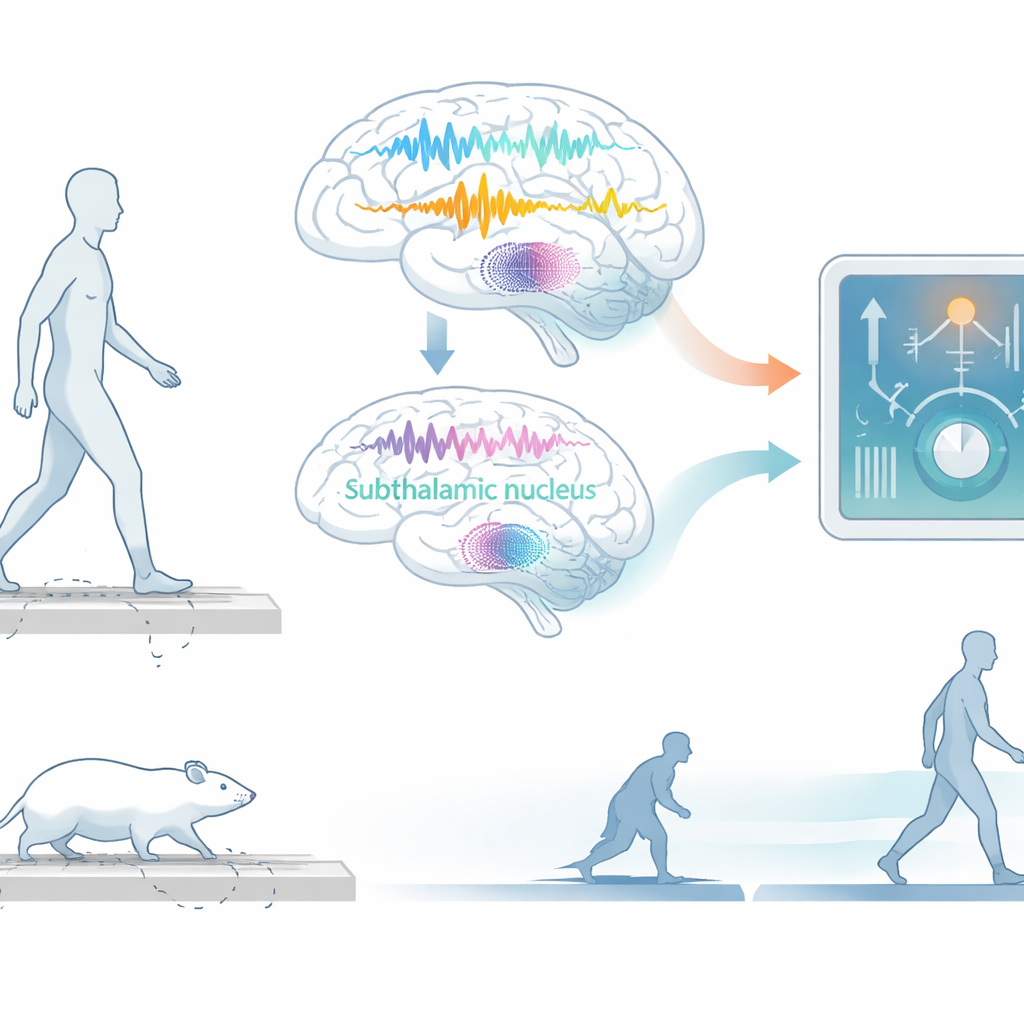
Obserwacja ruchu w najdrobniejszych detalach
Naukowcy rozpoczęli od dobrze ugruntowanego modelu choroby Parkinsona u szczurów. Wyszkolili zwierzęta do chodzenia tam i z powrotem po torze, śledząc każdy drobny ruch tylnych kończyn w trzech wymiarach oraz rejestrując aktywność elektryczną z obszarów mózgu związanych z ruchem. Każdy moment zachowania oznaczono jako jeden z trzech stanów: normalne chodzenie, niewielkie celowe ruchy w miejscu lub akinhezja — niemal całkowite zatrzymanie ruchu przypominające epizody zamarzania obserwowane u pacjentów. Powstał w ten sposób bogaty zestaw danych „neurobehawioralnych”, który zestawiał rytmy mózgowe z tym, co ciało robiło w każdej chwili.
Wyszukiwanie wzorców w falach mózgowych
Aby zrozumieć te wielowymiarowe dane, zespół zastosował zarówno klasyczne metody statystyczne, jak i nowoczesne narzędzia głębokiego uczenia. Najpierw potwierdzili znane sygnatury: szczury z uszkodzeniem przypominającym Parkinsona spędzały więcej czasu w stanie akinhezji niż zwierzęta zdrowe, a ich sygnały mózgowe wykazywały silniejszą aktywność w paśmie częstotliwości związanym z nieprawidłowymi rytmami beta i niskiej gamma. Kiedy jednak naukowcy zapytali, które cechy najlepiej rozróżniają trzy stany ruchu, pojawiły się nowe wskaźniki. Miary zwane złożonością Hjortha i mobilnością Hjortha — podsumowania czasowo‑dziedzinowe tego, jak nieregularnie i jak szybko zmienia się sygnał — okazały się silnymi markerami. W dotkniętej półkuli wyższa złożoność i niższa mobilność były ściśle związane z początkiem akinhezji, podczas gdy inne cechy, takie jak moc w wysokoczęstotliwościowym paśmie gamma, korelowały z aktywnym ruchem.
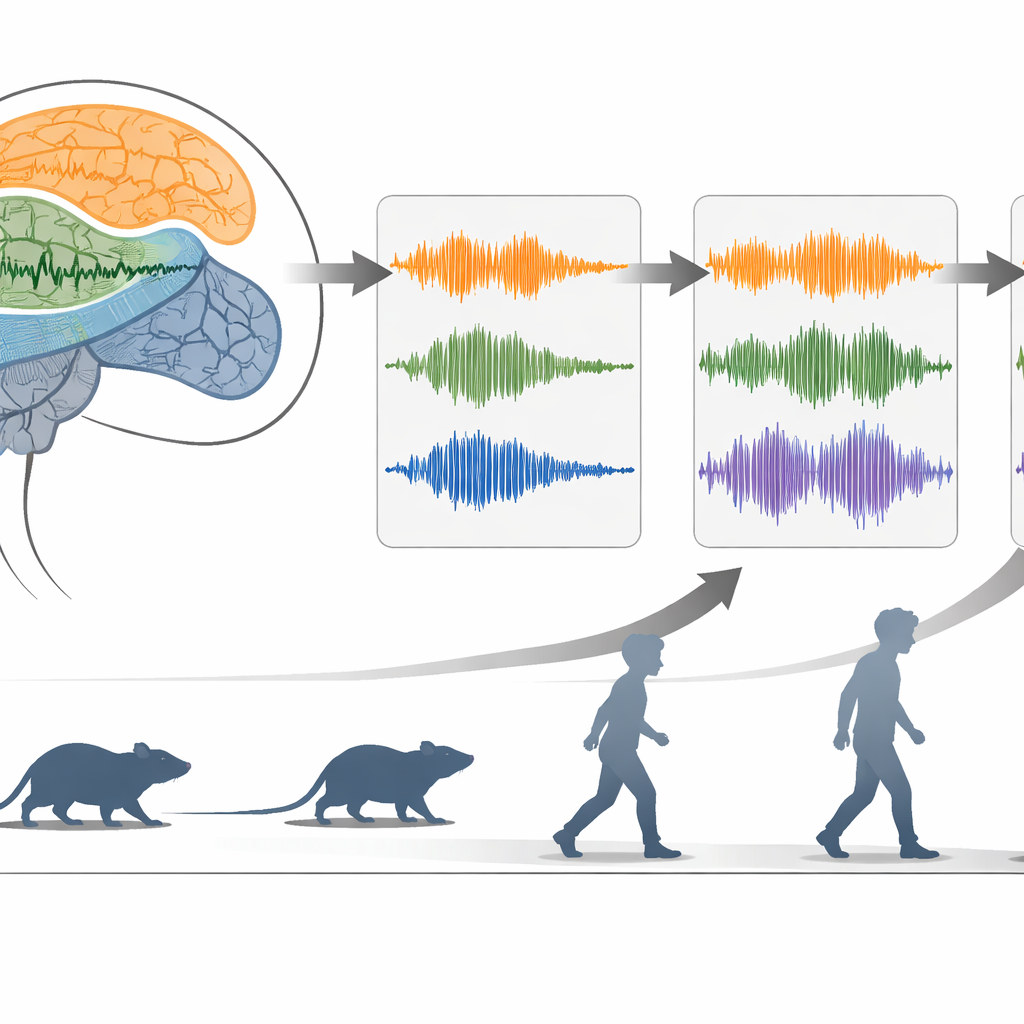
Przyglądanie się momentowi, kiedy ruch ustaje
Wykorzystując sieci neuronowe, które uczą się zwartego „mapowania” danych, badacze mogli umieścić każde krótkie okienko czasowe w niskowymiarowej przestrzeni, gdzie chodzenie, ruch w miejscu i akinhezja zajmowały odrębne obszary. W tej przestrzeni miary Hjortha i nieprawidłowe pasmo beta–niskiej gamma silnie kształtowały położenie epizodów akinezyjnych. Gdy zespół skupił się na sekundach wokół początku epizodu akinhezji, zaobserwowano spójną sekwencję: złożoność i moc przypominająca beta narastały tuż przed i w momencie zatrzymania, podczas gdy mobilność i moc gamma słabły. Co istotne, te miary można policzyć szybko bez ciężkiej analizy częstotliwościowej, co czyni je atrakcyjnymi kandydatami do monitorowania w czasie rzeczywistym.
Od szczurów do ludzi z zamarzaniem chodu
Grupa zapytała następnie, czy podobne neuronalne odciski występują u ludzi. Przeanalizowali szczegółowy zapis ruchu i rejestracje z elektrod wszczepionych w głęboką strukturę mózgu — jądro niskowodne (subthalamiczne) — u dwóch osób z chorobą Parkinsona doświadczających zamarzania chodu. U jednego uczestnika pojawił się ten sam wzorzec, co u szczurów, podczas epizodów zamarzania: zwiększona złożoność Hjortha i moc beta, równocześnie ze zmniejszoną mobilnością Hjortha. Chociaż zachowanie gammy różniło się nieco między gatunkami, zasadniczy sygnał wskazujący, że ruch przesuwa się w kierunku patologicznego stanu, wyglądał uderzająco podobnie w korze szczurów i w jądrze niskowodnym tego pacjenta, co sugeruje wspólny mechanizm w całej sieci ruchowej.
Co to może oznaczać dla przyszłych terapii
Łącząc szczegółowe śledzenie ruchu z zaawansowaną analizą rytmów mózgowych, praca ta identyfikuje proste, obliczeniowo lekkie „odciski” momentu, gdy chodzenie w chorobie Parkinsona jest o krok od załamania. Dla osoby spoza fachu oznacza to, że lekarze i inżynierowie wkrótce mogą zbudować stymulatory mózgu, które będą wyłapywać te odciski w czasie rzeczywistym i reagować tylko wtedy, gdy zajdzie potrzeba, odciągając układ od epizodu zamarzania zanim w pełni się rozwinie. Choć potrzebne są większe badania u ludzi, podejście otwiera obiecującą drogę do spersonalizowanych, zamkniętych pętli terapeutycznych dla uciążliwych zaburzeń chodu w chorobie Parkinsona.
Cytowanie: Garulli, E.L., Merk, T., El Hasbani, G. et al. Deep neurobehavioral phenotyping uncovers neural fingerprints of locomotor deficits in Parkinson’s disease. npj Parkinsons Dis. 12, 65 (2026). https://doi.org/10.1038/s41531-026-01280-4
Słowa kluczowe: choroba Parkinsona, zamarzanie chodu, rytmy mózgowe, głęboka stymulacja mózgu, neurobehawioralne fenotypowanie