Clear Sky Science · pl
Systematyczna ocena regulatorów morfologii mitochondriów w celu złagodzenia neuronalnej α-synukleinopatii
Dlaczego maleńkie elektrownie mają znaczenie w chorobach mózgu
Mitochondria, „elektrownie” komórki, są kluczowe dla utrzymania przy życiu komórek nerwowych i prawidłowego funkcjonowania ich połączeń. W zaburzeniach mózgu, takich jak choroba Parkinsona, te drobne struktury często wyglądają na uszkodzone lub rozdarte, jednak trudno było rozróżnić, które zmiany są szkodliwe, a które można bezpiecznie modyfikować, by je chronić. W badaniu tym systematycznie przetestowano kluczowych „regulatorów kształtu” mitochondriów w modelu laboratoryjnym nagromadzenia białka związanego z Parkinsonem, wykorzystując narzędzie sztucznej inteligencji do mierzenia kształtów mitochondriów w różnych częściach neuronów. Praca wskazuje na jeden konkretny regulator, zwany Fis1, jako obiecujący cel, pozwalający utrzymać mitochondria — i synapsy — zdrowe bez wywoływania nowych skutków ubocznych.
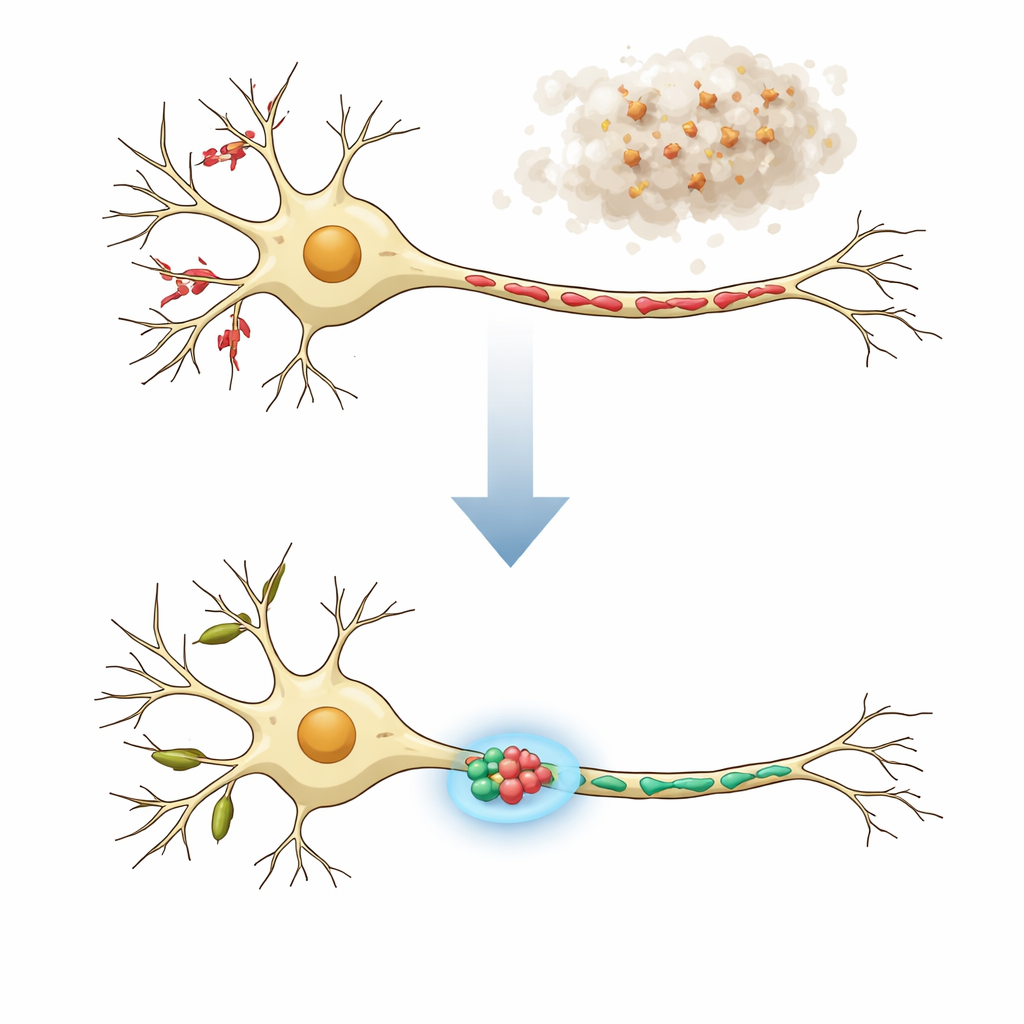
Dwie „dzielnice” komórki nerwowej
Neurony nie są jednorodne: ich rozgałęzione „drzewo” (dendryty) i długie „kable” (aksony) pełnią różne funkcje i zawierają mitochondria o bardzo odmiennych kształtach. W zdrowych komórkach nerwowych dendryty zwykle mają długie, rurkowate mitochondria, które wspierają lokalną syntezę białek i elastyczną komunikację w miejscu odbioru sygnałów, zwanym kolcem dendrytycznym. Aksony, które wysyłają sygnały, zamiast tego zawierają wiele krótkich mitochondriów dostarczających energię i pomagających kontrolować poziom wapnia w zakończeniach presynaptycznych. W chorobach neurodegeneracyjnych zarówno funkcja, jak i struktura tych mitochondriów mogą być zaburzone, objawiając się fragmentacją, obrzękiem lub koralikowatymi nitkami. Autorzy założyli, że naprawdę skuteczne terapie muszą przywrócić mitochondria w dendrytach i aksonach do ich normalnych, specyficznych dla danej „dzielnicy” kształtów.
Budowanie testu stresowego na wzór Parkinsona
Aby naśladować kluczową cechę choroby Parkinsona i pokrewnych zaburzeń, badacze wystawili hodowane neurony kory myszy na wstępnie uformowane fibryle alfa-synukleiny, białka, które może tworzyć szkodliwe agregaty. W ciągu kilku dni te fibryle zainicjowały nieprawidłowe nagromadzenie alfa-synukleiny w komórkach i doprowadziły do wyraźnej fragmentacji mitochondriów zarówno w dendrytach, jak i aksonach. Korzystając z MitoVis, systemu analizy obrazów opartego na głębokim uczeniu, zespół mógł automatycznie rozdzielać dendryty od aksonów na obrazach mikroskopowych i mierzyć długość, pole powierzchni oraz kształt setek mitochondriów na obraz — około dziesięć razy szybciej niż przy ręcznym odwzorowywaniu. To podejście wysokoprzepustowe potwierdziło, że warunek przypominający chorobę skraca mitochondria i zaokrągla je, co zgadza się z obserwacjami w modelach zwierzęcych i tkankach pacjentów.
Testowanie przełączników kształtu mitochondriów
Zespół następnie sprawdził, czy przesunięcie równowagi specyficznych białek odpowiedzialnych za fuzję i podział mitochondriów może zapobiec tym uszkodzeniom. Zwiększenie aktywności dwóch białek fuzji (Mfn1 i Mfn2) lub zmniejszenie poziomu białka rozdzielającego (Mff) rzeczywiście chroniło mitochondria dendrytyczne przed skróceniem wywołanym przez alfa-synukleinę i zapobiegało utracie kolców dendrytycznych. Jednak te same manipulacje powodowały nadmierne wydłużenie mitochondriów w aksonach, co wcześniejsze badania powiązały z problemami w uwalnianiu sygnału i rozgałęzianiu aksonu. Natomiast obniżenie poziomu innego białka rozdzielającego, Fis1, przywróciło długość mitochondriów zarówno w dendrytach, jak i aksonach do wartości zbliżonych do normy, bez nadmiernego wydłużenia. Co ważne, w tym ustawieniu redukcja Fis1 nie powodowała śmierci neuronów, a podobnie jak inne interwencje, zachowała gęstość kolców dendrytycznych, które w przeciwnym razie ulegałyby zmniejszeniu pod stresem wywołanym alfa-synukleiną.
Utrzymanie równowagi wapnia
Ponieważ mitochondria w aksonach pomagają buforować wapń podczas aktywności elektrycznej, badacze sprawdzili, czy zmiana ich kształtu wpływa na tę delikatną równowagę. Użyli fluorescencyjnego czujnika wapnia skierowanego do mitochondriów w przyboutonach presynaptycznych i stymulowali aksony krótkimi seriami potencjałów czynnościowych. W warunku z alfa-synukleiną obsługa wapnia w nieco skróconych mitochondriach aksonalnych wyglądała podobnie jak w normalnych komórkach. Jednak gdy mitochondria aksonalne były nadmiernie wydłużone przez nadekspresję Mfn1 lub spadek Mff, pochłaniały po stymulacji więcej wapnia niż zwykle. To zwiększone wychwytywanie mogło zaburzać funkcję presynaptyczną. Natomiast zmniejszenie poziomu Fis1, które normalizowało, lecz nie przesadzało z długością mitochondriów, zachowało odpowiedzi wapniowe mitochondriów zbliżone do zdrowych kontroli, sugerując mniej ukrytych kompromisów.
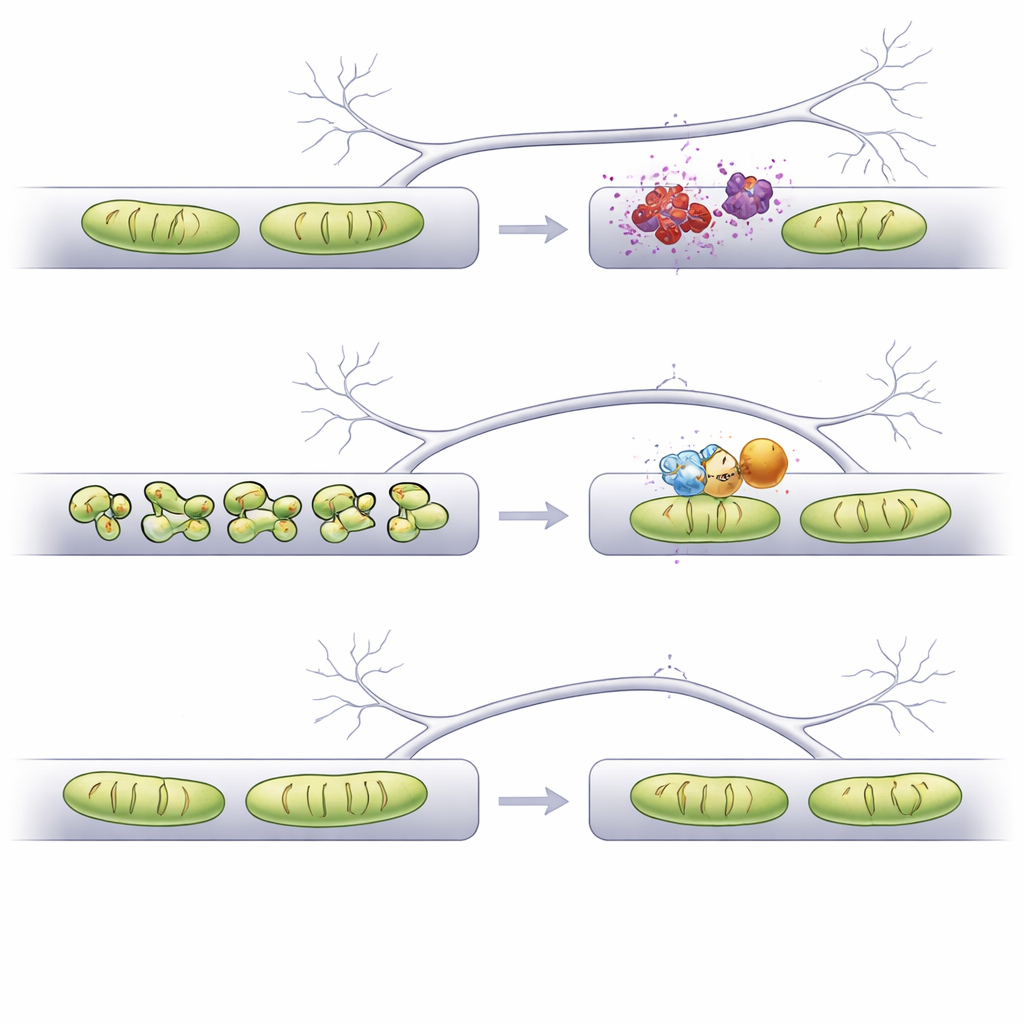
Co to może znaczyć dla przyszłych terapii
Podsumowując, badanie pokazuje, że samo wydłużanie mitochondriów nie wystarczy — kluczowe jest przywrócenie ich kształtu do właściwego rozmiaru w odpowiednich przedziałach komórki. Korzystając z przepływu pracy wspomaganego AI w obrazowaniu, autorzy identyfikują Fis1 jako szczególnie atrakcyjny cel: jego obniżenie utrzymuje stabilność strukturalną mitochondriów zarówno w dendrytach, jak i aksonach, zapobiega utracie kolców dendrytycznych i unika nieprawidłowego gospodarowania wapniem w zakończeniach presynaptycznych. Wyniki te wspierają ideę, że staranne dostrojenie kształtu mitochondriów, potencjalnie za pomocą leków lub cząsteczek antysensowych ukierunkowanych na Fis1, mogłoby pomóc chronić podatne synapsy w związanej z alfa-synukleiną chorobie Parkinsona i być może w innych chorobach mózgu, w których mitochondria ulegają zaburzeniu.
Cytowanie: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Słowa kluczowe: Choroba Parkinsona, mitochondria, alfa-synukleina, dysfunkcja synaptyczna, neurodegeneracja