Clear Sky Science · pl
Przydatność kliniczna potencjałów wywołanych do programowania głębokiej stymulacji podwzgórzowej w chorobie Parkinsona
Dlaczego ta opowieść o „rozruszniku” mózgu ma znaczenie
Dla wielu osób z chorobą Parkinsona leki z czasem przestają działać płynnie. Mogą doświadczać wahnięć między sztywnością a niekontrolowanymi ruchami, a dopracowywanie terapii staje się frustrującym cyklem wizyt w gabinecie. Niniejszy przegląd opisuje, jak lekarze mogą wykorzystać własne elektryczne echa mózgu — zwane potencjałami wywołanymi — do programowania głębokiej stymulacji (DBS) w sposób szybszy i bardziej obiektywny. W istocie pyta, czy można przekształcić DBS z ostrożnych prób i błędów w bardziej oparte na danych, spersonalizowane „rozrusznikowanie” mózgu.
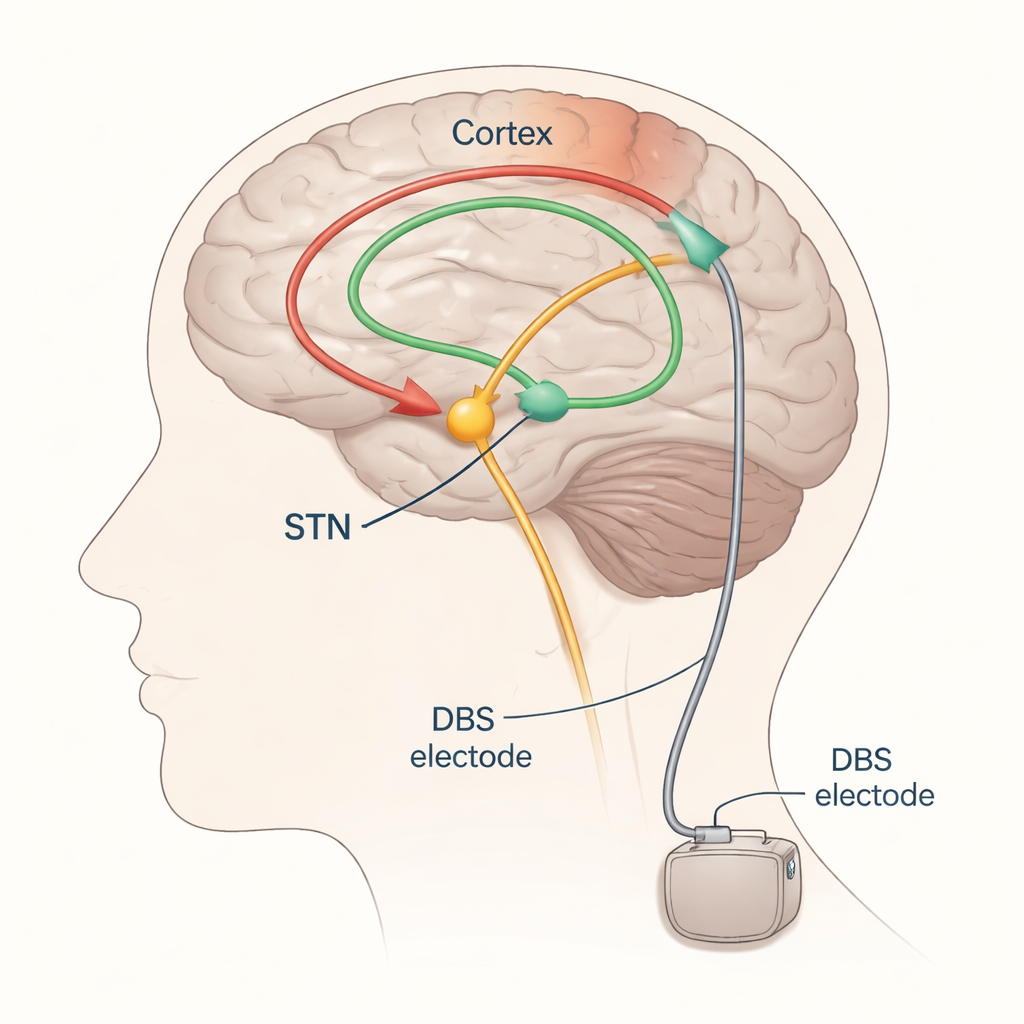
Od prób i błędów do ukierunkowanego strojenia
DBS w chorobie Parkinsona najczęściej celuje w niewielką strukturę położoną głęboko w mózgu zwaną jądrem niskowzgórzowym (subthalamic nucleus, STN). Elektrody wszczepiane są tam i łączone z generatorem impulsów umieszczonym pod skórą klatki piersiowej. Odpowiednio dostrojona stymulacja STN może złagodzić drżenie, spowolnienie ruchów i sztywność, lecz jeśli pole elektryczne rozprzestrzeni się zbyt szeroko, może niechcący pobudzać sąsiednie drogi kontrolujące mięśnie lub czucie, powodując działania niepożądane, takie jak skurcze mięśni czy mrowienie. Obecnie neurolodzy zwykle dostosowują DBS przez stopniowe zmiany ustawień i obserwację ruchów pacjenta oraz działań niepożądanych — podejście czasochłonne, zależne od samopoczucia pacjenta w danym dniu i często wymagające wielu wizyt kontrolnych.
Słuchając elektrycznych ech mózgu
Autorzy koncentrują się na potencjałach wywołanych — drobnych, czasowo powiązanych odpowiedziach elektrycznych w mózgu lub mięśniach po bodźcu — jako potencjalnych drogowskazach dobrych i złych ustawień DBS. Gdy STN jest stymulowane, fale aktywności przemieszczają się wzdłuż dróg nerwowych i mogą być rejestrowane na skórze głowy za pomocą EEG, w aktywności mięśniowej przez EMG, a czasem także przy użyciu pasków rejestrujących bezpośrednio na powierzchni mózgu. Poprzez wielokrotne pobudzanie niskimi częstotliwościami i uśrednianie odpowiedzi, badacze mogą wiarygodnie zobaczyć wyraźne fale pojawiające się w różnych opóźnieniach (w milisekundach) po każdym impulsie. Wczesne fale, pojawiające się w ciągu około dwóch tysięcznych sekundy, głównie odzwierciedlają aktywację szybkich dróg ruchowych przebiegających blisko elektrody. Nieco późniejsze fale, około trzech milisekund (często określane jako komponent „P3”), uważa się za wynik bezpośredniego połączenia między korą czołową a STN, znanego jako droga hiperprosta (hyperdirect pathway). Jeszcze późniejsze fale prawdopodobnie przemieszczają się przez dłuższe, obwodowe obwody obejmujące wzgórze i inne głębokie jądra.
Znajdowanie optymalnego miejsca i unikanie problemów
W wielu badaniach wyłania się spójny obraz: kontakty na prowadnicy DBS, które generują silny, krótkoopóźniony komponent P3, mają tendencję do znajdowania się w najbardziej korzystnej części STN i wiążą się z lepszą poprawą objawów ruchowych choroby Parkinsona oraz szerszym „oknem terapeutycznym” przed wystąpieniem skutków ubocznych. Natomiast bardzo wczesne fale związane z drogami ruchowymi oraz niektóre odpowiedzi w zakresie 8–10 milisekund często wskazują, że stymulacja rozlewa się do sąsiednich struktur, zwiększając ryzyko skurczów mięśni lub innych niepożądanych efektów. Oddzielne pomiary odpowiedzi ruchowych (EMG w mięśniach twarzy i kończyn) oraz somatosensorycznych potencjałów wywołanych (wzory EEG związane z drogami dotykowymi) mogą ujawnić subtelną aktywację torebki wewnętrznej lub pęczka smukłego — włókien przenoszących polecenia ruchowe i informacje sensoryczne. Wykrycie tych zmian wcześnie pozwala klinicystom odsunąć przepływ prądu od obszarów ryzykownych przez wybór innych kontaktów lub dostosowanie kształtu impulsu i polaryzacji.
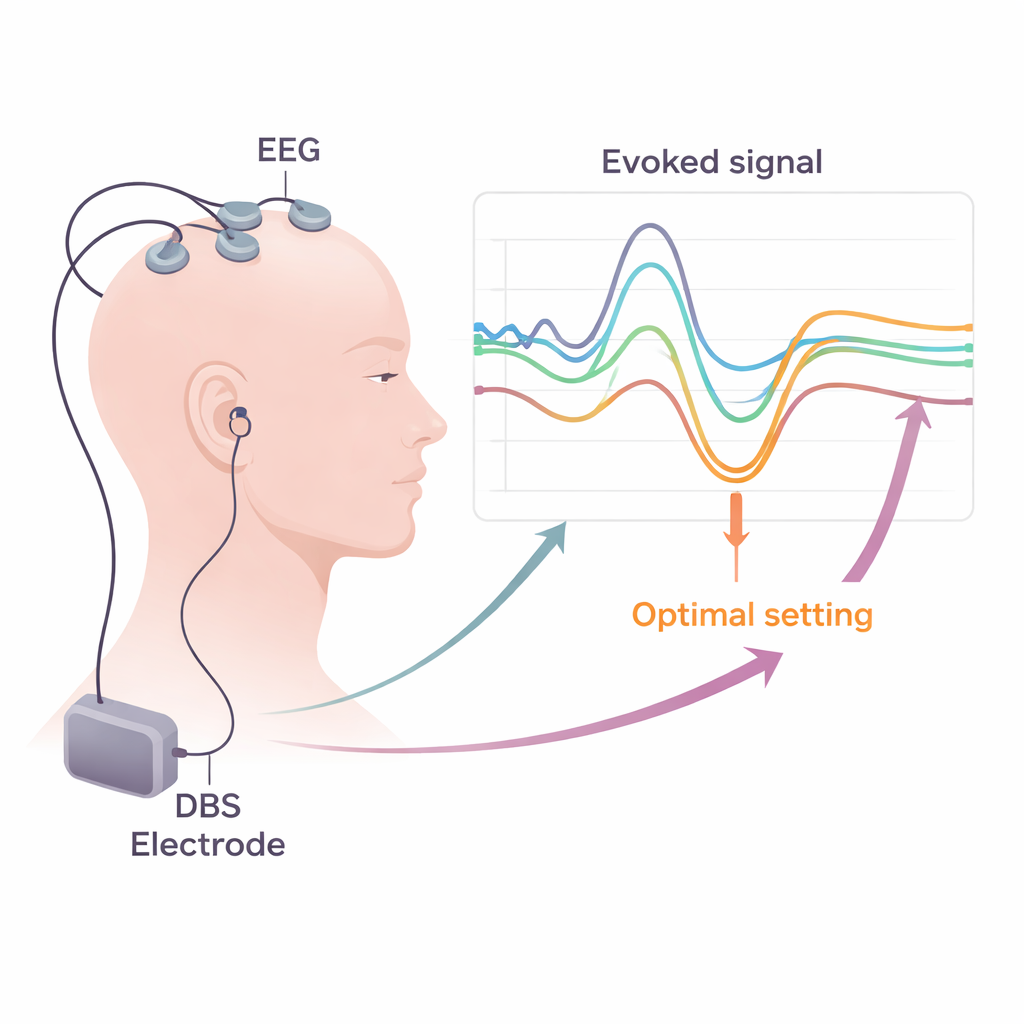
Uczynienie narzędzi laboratoryjnych praktycznymi w klinice
Przekształcenie tych spostrzeżeń w rutynową opiekę wymaga praktycznych rozwiązań. Przegląd wyjaśnia, że standardowe szpitalne systemy EEG i EMG mogą już rejestrować większość potrzebnych sygnałów, pod warunkiem stosowania wysokich częstotliwości próbkowania i starannych metod usuwania elektrycznych „zakłóceń” wywołanych impulsami DBS. Autorzy omawiają strategie redukcji artefaktów, takie jak sprytne przereferencjonowanie, odejmowanie szablonów oraz zaawansowane algorytmy komputerowe oddzielające prawdziwą aktywność mózgu od pozostałości stymulacji. Twierdzą, że krótkie, ustrukturyzowane sesje testowe — łączące krótkie okresy DBS o niskiej częstotliwości, zapisy ze skóry głowy i monitorowanie mięśni podczas spoczynku i lekkiego napięcia — można włączyć w zwykły tydzień programowania pooperacyjnego. Mapy potencjałów wywołanych dla każdego kontaktu mogłyby następnie zostać połączone z obrazowaniem i innymi markerami biologicznymi, by wskazać, które kontakty i ustawienia stosować długoterminowo.
Co to oznacza dla osób z chorobą Parkinsona
Artykuł podsumowuje, że potencjały wywołane są obiecującymi kandydatami do uczynienia programowania DBS bardziej precyzyjnym, wydajnym i przewidywalnym. W szczególności krótkoopóźniona fala P3 wydaje się silnym wskaźnikiem, że stymulacja trafia w odpowiedni obwód łagodzący objawy ruchowe Parkinsona, podczas gdy ruchowe i somatosensoryczne odpowiedzi wywołane mogą ostrzegać, gdy prąd uchodzi do dróg powodujących działania niepożądane. Choć potrzebne są dalsze prace nad standaryzacją technik i udowodnieniem korzyści w praktyce klinicznej, podejście to zmierza ku przyszłości, w której lekarze będą mogli „słuchać” mózgu podczas programowania, szybko namierzać indywidualne optymalne miejsce i zmniejszać ciężar prób i błędów dla osób żyjących z chorobą Parkinsona.
Cytowanie: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Słowa kluczowe: Choroba Parkinsona, głęboka stymulacja mózgu, potencjały wywołane, mapowanie mózgu, neurofizjologia