Clear Sky Science · pl
Odkodowywanie wpływu stanów wzrokowych na sygnały sprzężenia zwrotnego adaptacyjnej stymulacji głębokiej w zaburzeniach ruchu
Dlaczego zamknięcie oczu ma znaczenie dla implantów mózgowych
Dla osób z chorobą Parkinsona lub dystonią głęboka stymulacja mózgu (DBS) może działać jak rozrusznik dla niewłaściwie działających obwodów mózgowych. Nowocześniejsze systemy „adaptacyjne” obiecują automatycznie dostosowywać stymulację w czasie rzeczywistym, „słuchając” sygnałów mózgowych. Badanie pokazuje, że coś tak prostego i naturalnego jak zamknięcie oczu może silnie zmieniać te sygnały, co oznacza, że przyszłe implanty muszą najpierw rozpoznać stan osoby, zanim zdecydują, jak stymulować.
„Rozruszniki mózgu”, które uczą się i adaptują
Tradycyjna DBS dostarcza stałych impulsów elektrycznych do głębokich obszarów mózgu przez całą dobę. Choć może to łagodzić objawy takie jak drżenie czy sztywność, zużywa baterię i czasem powoduje skutki uboczne, ponieważ stymulacja nie zmienia się, gdy zmienia się stan pacjenta. Adaptacyjna DBS ma temu przeciwdziałać, zwiększając lub zmniejszając natężenie prądu na podstawie „potencjałów miejscowych” (local field potentials) — drobnych rytmicznych napięć rejestrowanych z tych samych elektrod, które dostarczają terapię. Te rytmy są najsilniejsze w strukturach zwanych jądrem podwzgórzowym (subthalamic nucleus, STN) i gałką bladą wewnętrzną (globus pallidus internus, GPi), kluczowych węzłach w sieci ruchowej. 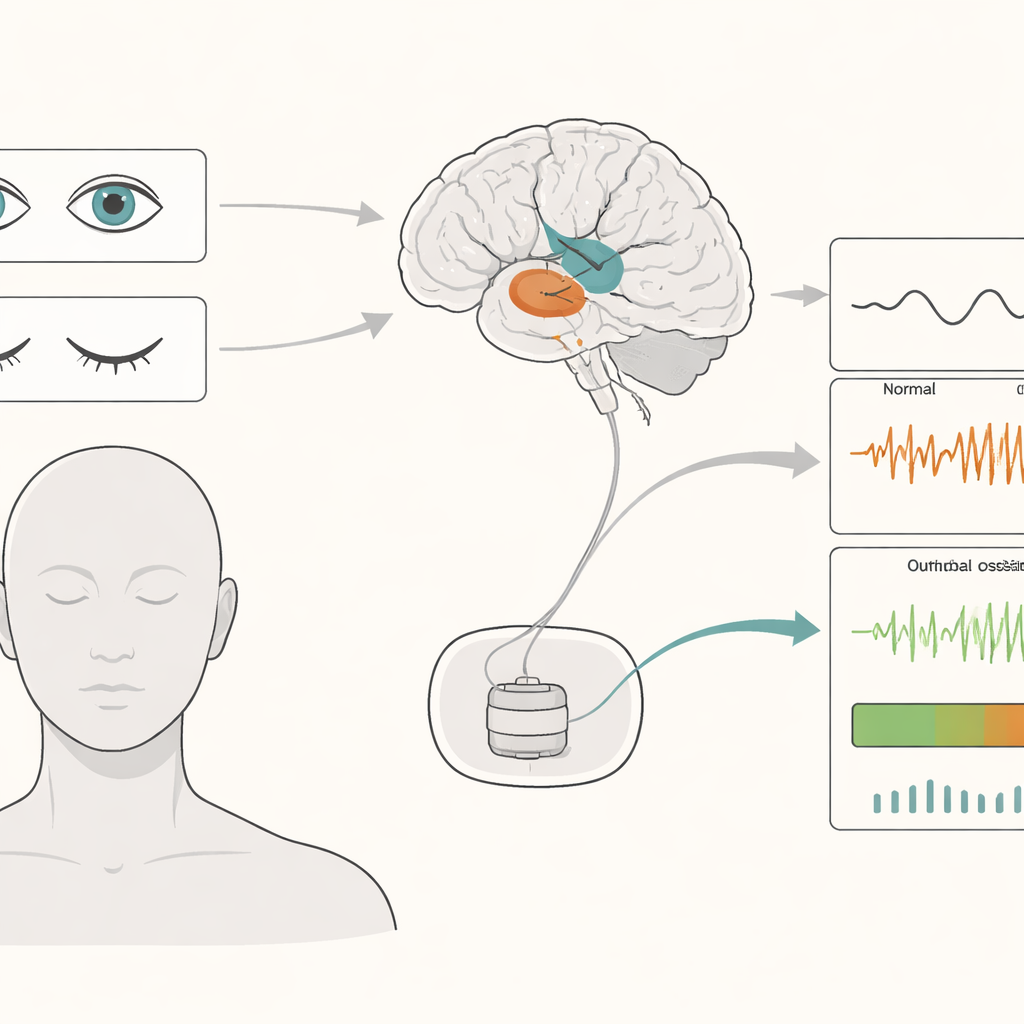
Gdy wzrok odpoczywa, rytmy głębokiego mózgu się przesuwają
Naukowcy śledzili 36 pacjentów — 18 z chorobą Parkinsona i 18 z dystonią — w dniach po operacji DBS. Rejestrowali aktywność mózgu z elektrod w STN lub GPi oraz z powierzchni czaszki, gdy pacjenci odpoczywali z oczami otwartymi, zamkniętymi lub podczas snu. Zamknięcie oczu konsekwentnie wzmacniało wolniejsze rytmy w głębokim mózgu, szczególnie w zakresach theta i alfa, czyli w sygnałach, na które wiele systemów adaptacyjnych zwraca uwagę. Wzrost ten był najsilniejszy w STN, który jest ściśle połączony z zewnętrzną, „myślącą” korą mózgową, i mniej wyraźny w GPi. Sen wykazywał inny wzorzec, z wyjątkowo silnymi bardzo wolnymi falami.
Różne choroby, różne odciski sygnałowe
Choroba Parkinsona i dystonia mają już odrębne rytmiczne „odciski palców”, a badanie wykazało, że zamknięcie oczu zmienia te odciski w nieco różny sposób. W obu schorzeniach moc niskich częstotliwości i alfa spadała po ponownym otwarciu oczu. Jednak w chorobie Parkinsona pojawiał się dodatkowy spadek mocy w paśmie theta, który nie występował w dystonii. W efekcie po otwarciu oczu osoby z dystonią zachowywały więcej aktywności theta niż osoby z Parkinsonem. To podkreśla, że ten sam sygnał z głębokiego mózgu może odzwierciedlać zarówno chorobę, jak i zwykłe zmiany czujności, przez co niebezpieczne jest traktowanie pojedynczej rytmiki jako prostego wskaźnika włączenia/wyłączenia objawów.
Sieci mózgowe komunikują się bardziej, gdy oczy są zamknięte
Ponad samą siłą rytmów zespół badał też, jak ściśle struktury głębokie i kora poruszają się synchronicznie. Używając metody skupiającej się na rzeczywistej komunikacji zamiast wspólnego szumu, stwierdzili, że zamknięcie oczu zwiększa skoordynowaną aktywność niskoczęstotliwościową i alfa między STN a centralnymi obszarami czaszki nad korą czuciowo-ruchową. GPi także wykazywała silniejsze sprzężenie alfa z korą przy zamkniętych oczach, choć skromniej i bez wyraźnych różnic regionalnych. Wyniki te sugerują, że odpoczynek z zamkniętymi oczami zmienia nie tylko lokalną aktywność, ale też szersze wzorce komunikacji w sieci ruchowej.
Nauczanie maszyn rozpoznawania stanów wewnętrznych
Ponieważ przyszłe implanty prawdopodobnie będą używać algorytmów do odczytu sygnałów mózgowych, naukowcy sprawdzili, czy proste modele uczenia maszynowego potrafią odróżnić oczy-otwarte od oczy-zamknięte wyłącznie na podstawie tych rytmów. Podając klasyfikatorom wiele pasm częstotliwości, uzyskali rozpoznanie stanu oczu z około 88-procentową dokładnością przy użyciu sygnałów ze STN i 77-procentową przy użyciu sygnałów z GPi, zarówno w chorobie Parkinsona, jak i w dystonii. Modele nieliniowe, potrafiące wychwycić bardziej złożone wzorce, radziły sobie jeszcze lepiej, a najlepsze dekodowanie pochodziło z regionów czuciowo-ruchowych najbardziej bezpośrednio związanych z ruchem. 
W kierunku sprytniejszej, świadomej kontekstu stymulacji mózgu
Mówiąc prościej, badanie pokazuje, że zwykłe, zdrowe zmiany w poziomie czujności lub zaangażowania wzrokowego osoby mogą silnie zmieniać fale mózgowe, na których opierają się systemy adaptacyjnej DBS. Jeśli implant będzie po prostu reagował, gdy rytm przekroczy ustalony próg, może błędnie odczytać normalne zmiany stanu jako zaostrzenie choroby i przedawkować albo niedostatecznie stymulować. Autorzy postulują, że kolejna generacja DBS powinna najpierw wykrywać kontekst osoby — na przykład oczy otwarte versus zamknięte, sen versus czuwanie — a następnie inaczej interpretować sygnały chorobowe zależnie od tego stanu. Takie „świadome stanu” rozruszniki mózgu mogłyby dostarczać bardziej precyzyjną pomoc, unikać niepotrzebnej stymulacji i lepiej wspierać osoby z zaburzeniami ruchu w codziennym życiu.
Cytowanie: Zhu, GY., Merk, T., Butenko, K. et al. Decoding the impact of visual states on adaptive deep brain stimulation feedback signals in movement disorders. npj Parkinsons Dis. 12, 61 (2026). https://doi.org/10.1038/s41531-026-01273-3
Słowa kluczowe: adaptacyjna stymulacja głęboka mózgu, choroba Parkinsona, dystonia, oscylacje mózgowe, interfejsy mózg–komputer