Clear Sky Science · pl
Hamowanie de novo syntezy ceramidów łagodzi patologię alfa-synukleiny w modelu myszy choroby Parkinsona
Dlaczego tłuszcze w mózgu mają znaczenie dla Parkinsona
Choroba Parkinsona jest najbardziej znana z drżących rąk i spowolnionych ruchów, ale głęboko w mózgu toczy się spokojniejszy, lecz ważny dramat. Komórki nerwowe kontrolujące ruch stopniowo obumierają, gdy białko zwane alfa-synukleiną zbija się w lepkie agregaty. Badanie to pokazuje, że konkretna rodzina tłuszczów — ceramidy — przyczynia się do tego uszkodzenia, i że zablokowanie ich produkcji może chronić komórki mózgowe u myszy oraz w modelach komórek ludzkich. Praca ta wskazuje na niespodziewaną, możliwą do zaatakowania farmakologicznie ścieżkę, która pewnego dnia może spowolnić lub zapobiec Parkinsonowi, zamiast jedynie łagodzić objawy.
Wskazówki z mózgów pośmiertnych
Aby ustalić, czy ceramidy biorą udział w Parkinsonie i pokrewnych schorzeniach, naukowcy najpierw przeanalizowali tkanki mózgowe pobrane po śmierci od osób z otępieniem z ciałami Lewy’ego, chorobą dzielącą te same toksyczne skupiska białkowe co Parkinson. Przy użyciu czułych pomiarów chemicznych stwierdzili, że wiele typów ceramidów było wyraźnie podwyższonych w śródmózgowiu w porównaniu ze zdrowymi mózgami, szczególnie formy o długich ogonach kwasów tłuszczowych. Następnie ponownie przeanalizowali duże zbiory danych genetycznych z ludzkich komórek mózgowych i odkryli, że geny odpowiedzialne za syntezę i przetwarzanie ceramidów były bardziej aktywne w neuronach produkujących dopaminę u pacjentów z Parkinsonem, a także w niektórych komórkach wspierających, takich jak astrocyty i oligodendrocyty. Razem te obserwacje sugerują, że równowaga ceramidów jest zaburzona w kilku typach komórek w chorym mózgu.
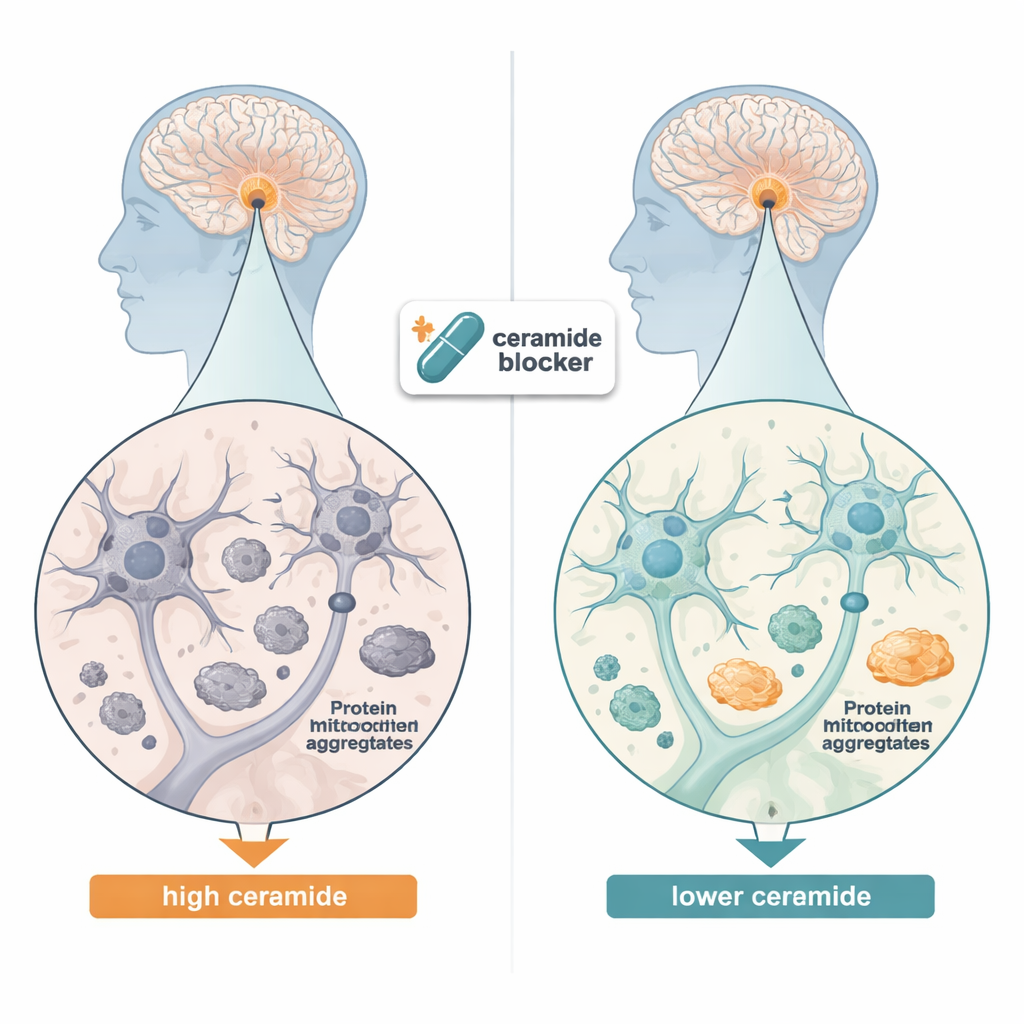
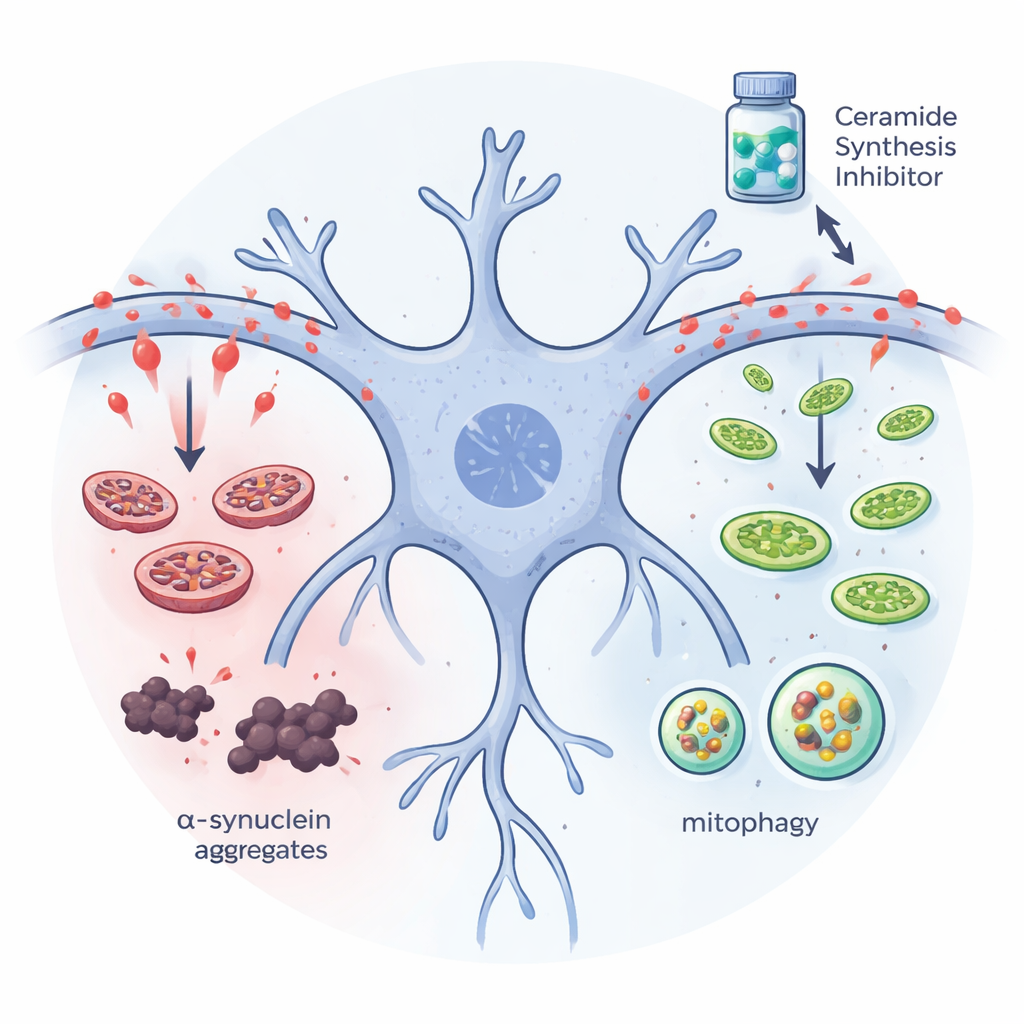
Sprzątanie skupisk białkowych w komórkach
Zespół następnie zapytał, czy obniżenie poziomu ceramidów może zmniejszyć gromadzenie się białka w komórkach neuronopodobnych hodowanych w laboratorium. Użyli ludzkich komórek neuroblastoma zmodyfikowanych tak, by nadprodukowaly zmutowaną formę alfa-synukleiny, która łatwo tworzy agregaty. Gdy zablokowali pierwszy etap produkcji ceramidów — albo przez wyciszenie genu kluczowego enzymu, albo przez dodanie leku myriocyny — ilość nierozpuszczalnych agregatów alfa-synukleiny spadła gwałtownie. Jednocześnie wzrosły markery mitofagii, czyli wyspecjalizowanego systemu komórkowego do wykrywania i recyklingu uszkodzonych mitochondriów, a mechanizmy tagowania niechcianych białek do utylizacji stały się bardziej aktywne. Te zmiany sugerują, że nadmiar ceramidów zwykle blokuje „ekipy sprzątające” komórki, a usunięcie tego lipidowego obciążenia pozwala komórce skuteczniej usuwać wadliwe mitochondria i skupiska białek.
Ochrona funkcji mózgu u myszy
Najważniejszym testem było sprawdzenie, czy ta strategia działa w żywym mózgu. Naukowcy lecili dobrze ugruntowany model myszy, który nadprodukuje zmutowaną ludzką alfa-synukleinę i stopniowo rozwija problemy z ruchem oraz zaburzenia pamięci. Od połowy życia niektóre myszy otrzymywały zastrzyki z myriocyną przez kilka miesięcy, podczas gdy inne dostawały obojętny nośnik. Myriocyna wyraźnie obniżyła poziom ceramidów we krwi i w śródmózgowiu zwierząt. Testy behawioralne wykazały, że myszy poddane leczeniu przemieszczały się dalej i lepiej radziły sobie w prostym labiryncie zależnym od przestrzennej pamięci roboczej. Plastry mózgu tych zwierząt wykazały, że więcej neuronów produkujących dopaminę przeżyło w kluczowych obszarach, a ilość fosforylowanej, podatnej na agregację alfa-synukleiny była zmniejszona. Profilowanie ekspresji genów na dużą skalę w śródmózgowiu dodatkowo pokazało, że myriocyna osłabiła szlaki zapalne, jednocześnie przywracając geny związane z komunikacją synaptyczną i prawidłową konserwacją mitochondriów.
Ludzkie neurony i mini-mózgi potwierdzają wyniki
Aby przybliżyć wyniki do pacjentów, zespół użył neuronów i trójwymiarowych organoidów śródmózgowia hodowanych z indukowanych pluripotentnych komórek macierzystych pochodzących od osób z Parkinsonem. W neuronach pochodzących od pacjentów, wyposażonych w fluorescencyjny sensor mitofagii, leczenie myriocyną wzmocniło sygnał oznaczający dostarczanie uszkodzonych mitochondriów do centrów recyklingu komórkowego i poprawiło architekturę sieci mitochondrialnej. W organoidach śródmózgowia myriocyna chroniła komórki produkujące dopaminę i zmniejszała szkodliwe agregaty alfa-synukleiny. Gdy badacze dodali dodatkowe ceramidy do tych mini-mózgów, następowało odwrotne zjawisko: tworzyło się więcej skupisk białkowych, a neurony dopaminergiczne ginęły, zwłaszcza w organoidach od dawców z chorobą Parkinsona. Eksperymenty te wspierają bezpośrednią, szkodliwą rolę nagromadzenia ceramidów w tkance istotnej dla człowieka.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami, przekaz jest prosty: w wielu modelach Parkinsona nadmiar pewnego tłuszczu mózgowego wydaje się zatruwać komórki, promując tworzenie się skupisk białkowych, uszkodzone mitochondria i przewlekłe zapalenie. Zablokowanie głównej ścieżki wytwarzającej te tłuszcze, przy użyciu eksperymentalnego leku myriocyny, łagodziło te problemy, chroniło wrażliwe neurony i poprawiało zachowanie myszy, a także ratowało ludzkie neurony w hodowli. Autorzy podkreślają, że długoterminowe bezpieczeństwo i dawkowanie u ludzi pozostają nieznane, a przyczyny Parkinsona są wielorakie i wykraczają poza ceramidy. Mimo to praca otwiera nowy kierunek badań: zamiast tylko wzmacniać zanikający sygnał dopaminergiczny, przyszłe terapie mogłyby także normalizować metabolizm lipidów i mechanizmy sprzątające komórki, dając komórkom mózgowym większe szanse, by przeciwstawić się powolnemu marszowi neurodegeneracji.
Cytowanie: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
Słowa kluczowe: Choroba Parkinsona, ceramid, alfa-synukleina, mitofagia, neurodegeneracja