Clear Sky Science · pl
Hamowanie korozji wżerowej stali nierdzewnej przez NaNO3: wgląd mechanistyczny w rozpuszczanie siarczków, depasywację i aktywne rozpuszczanie
Dlaczego drobne plamy rdzy mają znaczenie
Od mostów i wieżowców po samochody i zakłady chemiczne—stal nierdzewna wybierana jest, ponieważ zazwyczaj odporna jest na rdzę. Jednak w określonych warunkach może nagle powstać wiele małych, głębokich ubytków zwanych wżerami, które mogą rozrosnąć się do niebezpiecznych pęknięć. To badanie stawia praktyczne pytanie dla przemysłu: czy powszechny, stosunkowo bezpieczny związek—azotan sodu—może zapobiec powstawaniu tych wżerów i jeśli tak, to w jaki sposób? Odpowiedź może pomóc wydłużyć bezpieczną eksploatację krytycznej infrastruktury przy użyciu dodatków, które są niedrogie i mniej szkodliwe dla środowiska. 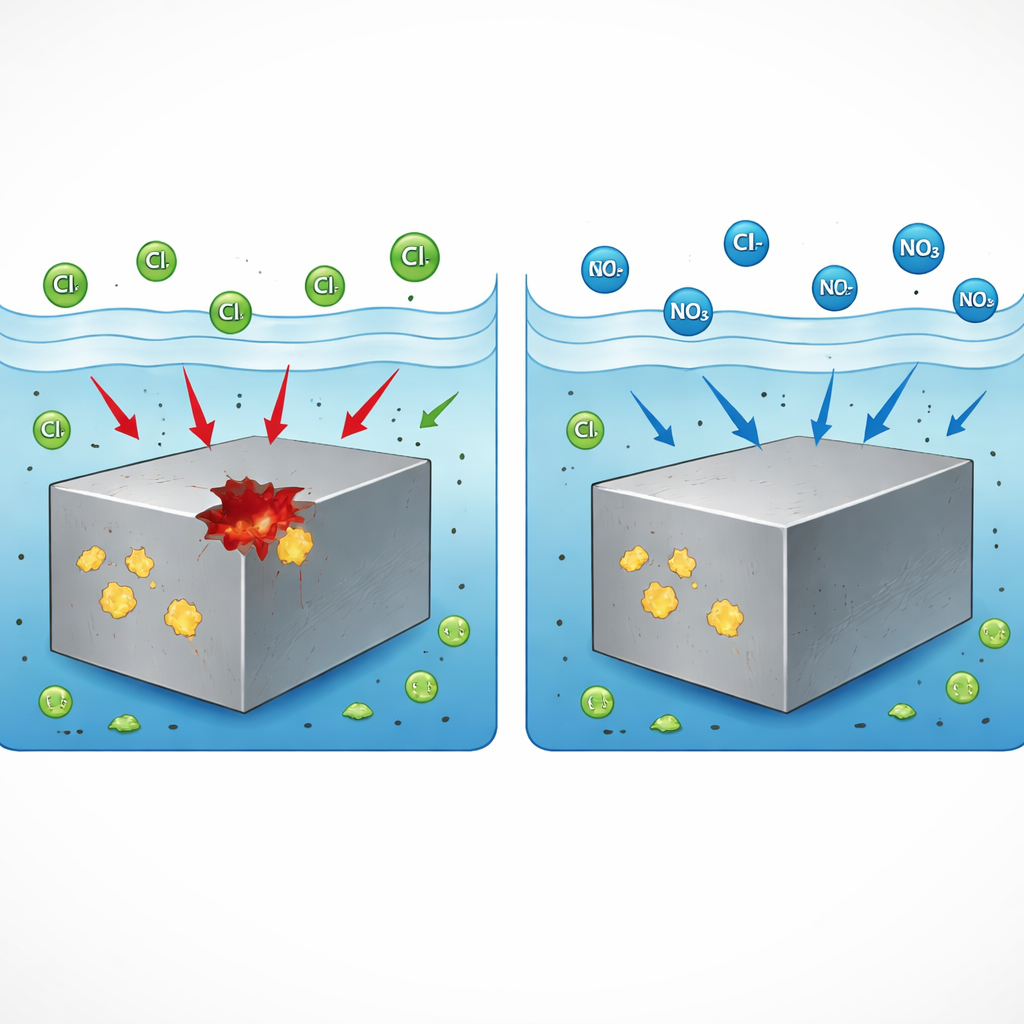
Ukryte słabe punkty w stali nierdzewnej
Nawet najlepsze stale nierdzewne nie są idealnie jednorodne. W ich wnętrzu znajdują się rozproszone, mikroskopijne cząstki bogate w siarkę, znane jako inkluzje siarczkowe. Dwa ważne typy to inkluzje oparte na manganie (MnS) i na wapniu (CaS). Te inkluzje zachowują się jak wbudowane słabe punkty, w których wżery preferencyjnie się rozpoczynają, gdy metal styka się z wodą zawierającą chlorki, taką jak słona mgła czy woda chłodząca. Wcześniejsze prace wykazały, że formowanie się wżerów przebiega według stałego scenariusza: cząstka siarczkowa zaczyna się rozpuszczać, ochronna warstwa na sąsiedniej stali ulega naruszeniu, a następnie otaczający metal zaczyna szybko się rozpuszczać, pogłębiając wżer. Niniejsze badanie porównuje dwa komercyjne gatunki stali typu 304—jeden z inkluzjami dominującymi MnS, drugi z inkluzjami na bazie CaS—by ustalić, czy azotan może przerwać ten scenariusz przy jednym lub obu rodzajach słabych punktów.
Testowanie typowych dodatków w słonej wodzie
Naukowcy zanurzyli próbki stali w prostym roztworze soli i stopniowo doprowadzali metal do bardziej korozyjnych warunków, obserwując moment powstawania stabilnych wżerów. Porównali trzy dodatki w realistycznych stężeniach: amonowy, azotynowy i azotanowy, wszystkie jako sole sodowe lub amonowe. Tylko azotan wykazał uderzający efekt. Zarówno w stali bogatej w MnS, jak i w stali bogatej w CaS, dodanie umiarkowanej ilości azotanu sodu całkowicie zapobiegło tworzeniu się stabilnych wżerów w badanym zakresie, podczas gdy pozostałe dwa dodatki nie przyniosły poprawy. Mikroskopia potwierdziła, że bez azotanu wżery rzeczywiście zaczynały się od inkluzji siarczkowych, podczas gdy w obecności azotanu te inkluzje nie wywoływały już niszczących ubytków. Pokazało to, że azotan jest szeroko skutecznym inhibitorem wżerów dla różnych typów inkluzji siarczkowych, a nie tylko w szczególnych przypadkach. 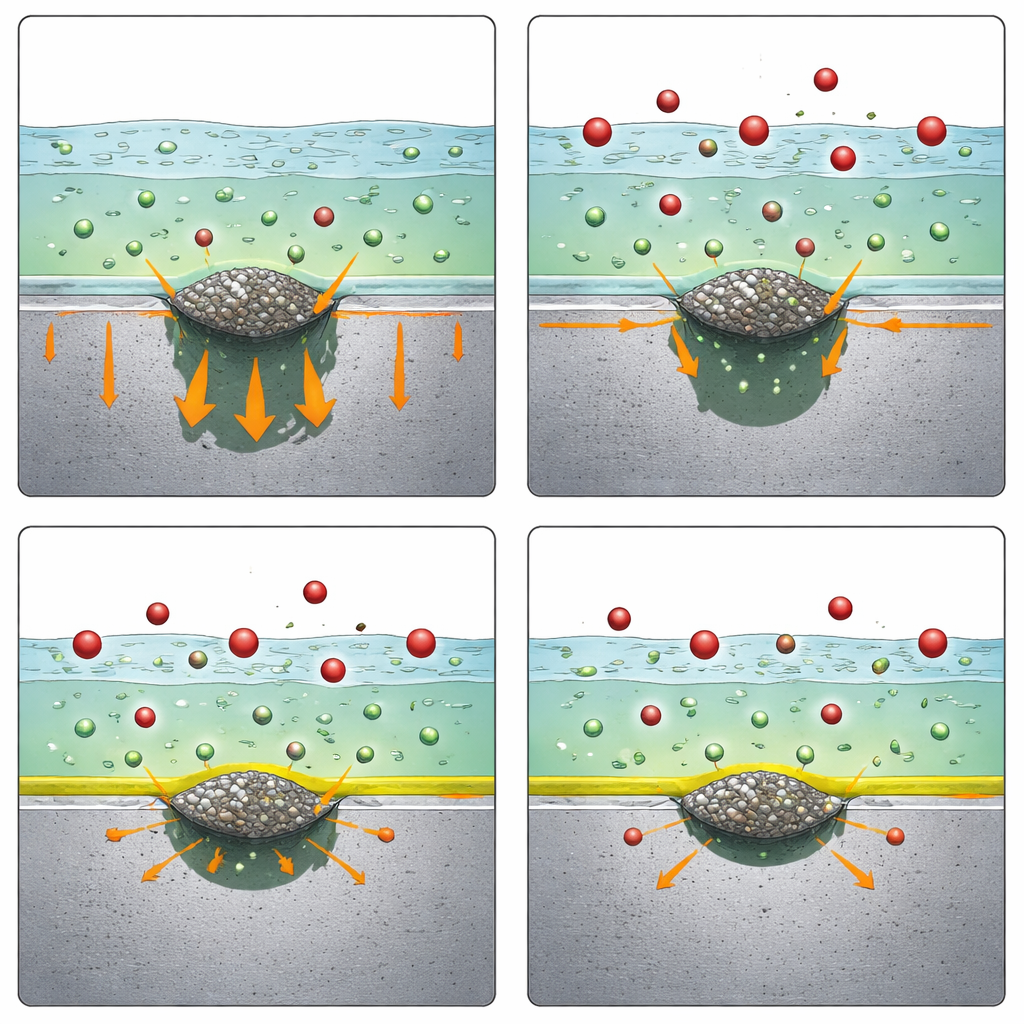
Dokładne przyjrzenie się temu, co azotan zmienia — i czego nie
Aby ustalić mechanizm działania azotanu, zespół skupił się na wczesnych etapach inicjacji wżerów wokół pojedynczych cząstek MnS, używając mikrolektród i obrazowania o wysokiej rozdzielczości. Zaobserwowali, że azotan nie powstrzymywał samych cząstek MnS przed rozpuszczaniem się, ani nie zmieniał małych rowków tworzących się na styku inkluzji z otaczającą stalą. Azotan nie przesunął także wartości kwasowości, przy której ochronna warstwa stali zawodzi w roztworze chlorkowym. Wszystko to wskazywało, że pierwsze kroki inicjacji wżerów—osłabienie i zakłócenie wokół inkluzji—przebiegają w obecności azotanu w zasadzie tak samo jak bez niego.
Spowolnienie końcowego przypływu utraty metalu
Kluczowa różnica ujawniła się, gdy badacze odtworzyli surowe warunki panujące wewnątrz już ukształtowanego wżera: bardzo kwaśne środowisko bogate w chlorki. Używając silnych roztworów kwasowych imitujących chemię głębi wżerów, zauważyli, że stal zwykle wykazuje dwie wyraźne fazy gwałtownego rozpuszczania metalu w miarę wzrostu napięcia. Dodanie azotanu konsekwentnie redukowało pierwszy skok rozpuszczania, zarówno w samym kwasie, jak i w kwasie zawierającym dodatkowo gatunki siarki podobne do tych uwalnianych z rozpuszczającego się MnS. Obserwacje powierzchni wykazały równomierne niszczenie, ale wyraźnie wolniejsze. Dodatkowe testy, zmieniające kwasowość i poziomy chlorków, sugerowały, że efekt azotanu nie wynikał jedynie z rozcieńczenia kwasowości, wypierania chlorków czy stabilizacji skorup solnych. Wyniki wskazywały raczej, że azotan sprzyja tworzeniu stabilizującej warstwy powierzchniowej z chromu w stopie, co z kolei spowalnia wczesną, najbardziej krytyczną fazę aktywnej utraty metalu.
Co to znaczy dla stali stosowanych w praktyce
Mówiąc wprost: azotan nie zapobiega pierwszym chemicznym „gryzkom” w mikroinkluzjach siarczkowych w stali nierdzewnej, ale spowalnia końcową, gwałtowną fazę, w której nieszkodliwa wada przekształca się w niebezpieczny wżer. Tłumiąc ten zryw utraty metalu w kwaśnych, słonych mikrośrodowiskach, azotan sodu utrzymuje stal bliżej stanu pasywnego i samoochronnego, nawet gdy obecne są inkluzje siarczkowe i jony chlorkowe. Ponieważ azotan jest relatywnie tani, mniej toksyczny niż wiele alternatyw i już stosowany w przemysłowych systemach wodnych, zrozumienie tego mechanizmu wzmacnia argumenty za jego rozważnym użyciem jako dodatku do kontroli korozji w celu wydłużenia żywotności konstrukcji i urządzeń ze stali nierdzewnej.
Cytowanie: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Słowa kluczowe: korozja stali nierdzewnej, hamowanie wżerów, azotan sodu, inkluzje siarczkowe, roztwory chlorkowe