Clear Sky Science · pl
Modelowanie jednorodnego zachowania korozyjnego cynku w badaniach mgłą solną
Dlaczego to ma znaczenie dla codziennych części metalowych
Od nadwozi samochodowych po linie energetyczne — wiele elementów metalowych zabezpiecza cienka powłoka cynkowa, która rozpuszcza się zamiast podlegającej jej stali. Inżynierowie szeroko polegają na „testach mgłą solną”, aby oszacować trwałość tych powłok w agresywnych, słonych warunkach przypominających zimowe drogi czy powietrze morskie. Jednak testy te bywają trudne do interpretacji i nie zawsze dają spójne, ilościowe odpowiedzi. Artykuł ten podejmuje ten problem, budując model komputerowy oparty na prawach fizyki, który przewiduje tempo zużywania się powłok cynkowych w warunkach mgły solnej, dążąc do przekształcenia jakościowego testu laboratoryjnego w bardziej niezawodne narzędzie projektowe.
Jak powłoki cynkowe chronią metal
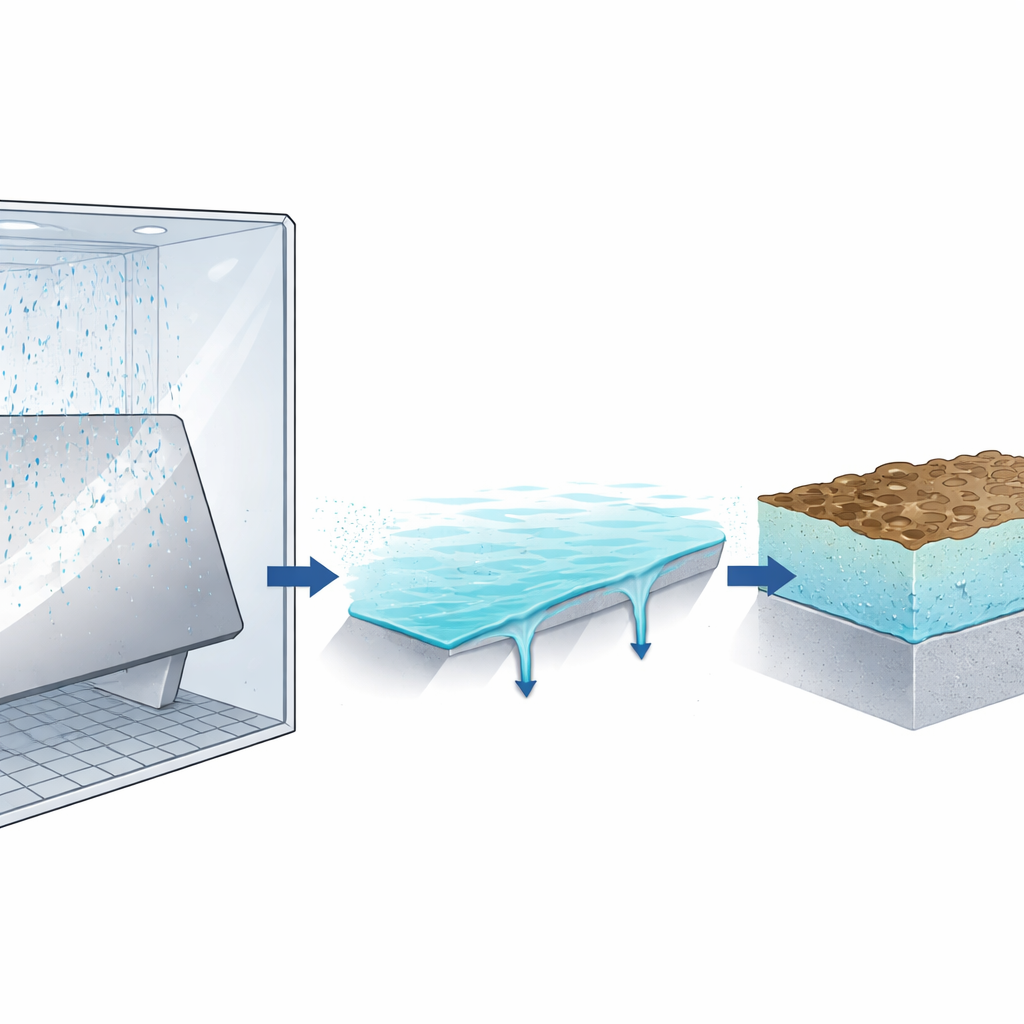
Powłoki cynkowe działają jako ofiarne osłony: korodują najpierw, chroniąc stal pod spodem. W słonej wodzie cynk rozpuszcza się tworząc naładowane cząstki (jony), podczas gdy tlen z powietrza reaguje, tworząc cienką, początkowo nieciągłą warstwę produktów korozji, głównie wodorotlenku cynku i tlenku cynku. Z czasem warstwa ta rośnie i może częściowo spowolnić dalszy atak. W rzeczywistych komorach do badań mgłą solną powierzchnia nie jest zanurzona w basenie wody. Zamiast tego cienka warstwa słonej wilgoci stale powstaje z rozpylanych kropli, pogrubia się, a następnie spływa w cyklach. Ta zmienna warstwa kontroluje, ile tlenu i soli dociera do metalu oraz jak szybko gromadzą się jony cynku, co z kolei reguluje szybkość korozji.
Budowanie modelu korozji od podstaw
Autorzy opracowali model numeryczny łączący trzy kluczowe elementy: reakcje elektrochemiczne rozpuszczające cynk, transport jonów i tlenu przez cienką warstwę wody oraz tworzenie się stałych produktów korozji, które tworzą rosnącą barierę. Ruch jonów opisali standardowym równaniem dyfuzji, uprościli efekty elektryczne i potraktowali korozję jako mieszaninę procesów kontrolowanych reakcją i dyfuzją. Specjalna relacja, równanie Brønsteda–Bjerruma, koryguje szybkość tworzenia się wodorotlenku cynku, gdy stężenie soli w warstwie wodnej staje się bardzo wysokie, co często ma miejsce w cienkiej, powoli spływającej warstwie. Aby model pozostał realistyczny, ale możliwy do obliczenia, autorzy założyli jednorodność korozji na powierzchni i skupili się wyłącznie na warstwie cynku, nie uwzględniając jeszcze późniejszych uszkodzeń stali pod spodem.
Weryfikacja modelu na podstawie rzeczywistych eksperymentów
Aby dostroić model, zespół najpierw zasymulował prostszy przypadek: czysty cynk zanurzony w rozcieńczonym roztworze soli. Dostosowali trzy niepewne wielkości — szybkość wytrącania się wodorotlenku cynku, łatwość ruchu jonów cynku przez film oraz porowatość warstwy tlenkowej — aż symulacje odpowiadały opublikowanym pomiarom głębokości korozji, grubości tlenku i ilości cynku uwolnionego do cieczy. Kalibracja wykazała na przykład, że szybsze strącanie pogrubia warstwę tlenku i spowalnia korozję przez ograniczenie dostępu tlenu. Po skalibrowaniu te same parametry zastosowano do znacznie bardziej realistycznego testu mgłą solną o charakterystyce neutralnej, imitującego wodę morską z Cieśniny Kerczeńskiej. Model odzwierciedlił tu ważne przejście: początkowo korozja jest głównie kontrolowana reakcjami powierzchniowymi, ale w miarę wzrostu warstwy tlenkowej i koncentracji jonów staje się ograniczana tym, jak szybko gatunki mogą dyfundować przez coraz bardziej zatkany „filtr”.
Dlaczego ruch filmu wodnego ma znaczenie
Charakterystyczną cechą testów mgłą solną jest niestabilne zachowanie cienkiego filmu wodnego. Krople rozpylone stopniowo pogrubiają warstwę, aż grawitacja i siły powierzchniowe powodują spływanie części, które zabierają rozpuszczony cynk i krótko cienią film. Autorzy uwzględnili to, pozwalając grubości filmu rosnąć z określoną szybkością, a następnie okresowo resetować ją do mniejszej wartości, bazując na zmierzonych okresach spływu i kątach ustawienia próbek. Symulacje pokazały, że wyższe szybkości rozpylania i większe kąty nachylenia zwykle zwiększają korozję we wczesnej fazie, dostarczając powierzchni świeżego roztworu. Dłuższe odstępy między spływami dają więcej czasu na akumulację jonów cynku, co wzmacnia bariery dyfuzyjne i może później spowalniać korozję. Gdy dynamika filmu jest uwzględniona, a warstwa tlenkowa przyjęta jako umiarkowanie porowata, model odtwarza zmierzone tempo korozji z testów mgłą solną zwykle w granicach około 20 procent.

Co badanie oznacza dla rzeczywistej trwałości
Mówiąc prosto, badanie pokazuje, że to, jak warstwa słonej wody rośnie, koncentruje się i spływa z powierzchni pokrytej cynkiem, jest równie ważne jak chemia samego cynku przy określaniu tempa zanikania powłoki. Film wodny, który jest okresowo odnawiany, zapobiega nadmiernemu nagromadzeniu jonów cynku i może podtrzymywać wyższe tempo korozji, podczas gdy gęsta, nieprzerwana skorupa tlenkowa może spowolnić korozję, choć w końcu może pękać lub odpryskiwać. Uchwycenie tych kompromisów w jednym, relatywnie wydajnym modelu daje podstawę do bardziej ilościowego przewidywania żywotności części pokrytych cynkiem i do rozszerzenia podejścia na bardziej złożone, przemysłowe testy korozyjne obejmujące cykle wysychania, zmiany temperatury i ostatecznie początki korozji stali po zużyciu cynku.
Cytowanie: Chen, C., Hofmann, M. & Wallmersperger, T. Modeling the uniform corrosion behavior of zinc in salt spray testing. npj Mater Degrad 10, 37 (2026). https://doi.org/10.1038/s41529-026-00749-0
Słowa kluczowe: korozja cynku, badanie mgłą solną, powłoki cynkowe, modelowanie korozji, film elektrolitowy